解题方法
1 . 为探究卤族元素单质及其化合物的性质设计了如下实验方案。由下列操作、现象能得出相应结论的是
操作 | 现象 | 结论 | |
| A | 向两份新制氯水中,分别滴加淀粉KI溶液和 溶液 溶液 | 前者溶液变蓝,后者溶液产生白色沉淀 | 氯气与水的反应存在限度 |
| B | 用玻璃棒蘸取“84”消毒液点在pH试纸上 | 试纸变白 | “84”消毒液呈中性 |
| C | 将少量 溶液滴入 溶液滴入 溶液中 溶液中 | 紫色很快褪去 | 氧化能力: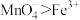 |
| D | 向碘的 溶液中加入等体积KI浓溶液,振荡、静置 溶液中加入等体积KI浓溶液,振荡、静置 | 分层,上层呈棕褐色,下层呈浅红色 | 碘在浓KI溶液中的溶解能力大于在 中的溶解能力 中的溶解能力 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 从废弃的声光器件( ,含Al、Cu、
,含Al、Cu、 杂质)中提取粗碲的工艺流程如图,已知
杂质)中提取粗碲的工艺流程如图,已知 性质与
性质与 相似,氧化沉碲得
相似,氧化沉碲得 ,下列说法错误的是
,下列说法错误的是
 ,含Al、Cu、
,含Al、Cu、 杂质)中提取粗碲的工艺流程如图,已知
杂质)中提取粗碲的工艺流程如图,已知 性质与
性质与 相似,氧化沉碲得
相似,氧化沉碲得 ,下列说法错误的是
,下列说法错误的是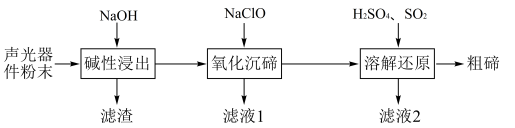
| A.滤渣的主要成分为Cu |
| B.滤液1和滤液2混合可能产生白色沉淀 |
C.“氧化沉碲”中离子方程式为 |
D.“溶解还原”中氧化剂和还原剂的物质的量之比为 |
您最近一年使用:0次
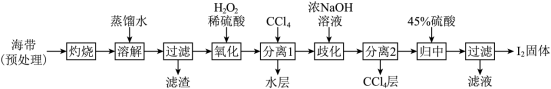
3 . 碘是国防、工业、农业、医药等部门和行业所依赖的重要原料,海水提碘是从海藻中提取元素碘的技术。
Ⅰ.海带提碘(海带中碘元素以I-形式存在)_______ ,设计实验检验氧化后所得溶液是否含I2时,可取样于试管,滴加_______ (填试剂名称)。
(2)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为_______ ;向分离得到的含I-和 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为_______ 。
Ⅱ.获取重要的还原剂-HI
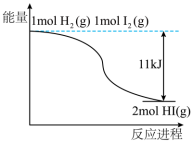
(3)H2和I2反应生成HI过程能量变化如图所示,1molH2(g)、1molHI(g)分子中化学键断裂时分别要吸收能量436kJ、299kJ,则1molI2(g)分子中化学键断裂时需吸收的能量为_______ kJ。
(4)优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为 ,其工作原理如图所示:
,其工作原理如图所示:_______ ;
②放电时,转移0.6×6.02×1023个电子,负极质量减少_______ g。
Ⅰ.海带提碘(海带中碘元素以I-形式存在)
(2)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为
 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为Ⅱ.获取重要的还原剂-HI
(3)H2和I2反应生成HI过程能量变化如图所示,1molH2(g)、1molHI(g)分子中化学键断裂时分别要吸收能量436kJ、299kJ,则1molI2(g)分子中化学键断裂时需吸收的能量为
(4)优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为
 ,其工作原理如图所示:
,其工作原理如图所示: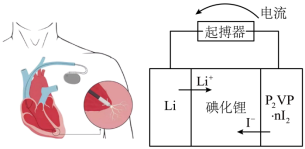
②放电时,转移0.6×6.02×1023个电子,负极质量减少
您最近一年使用:0次
名校
4 . 查阅资料可知:Bi位于周期表的第VA族, 是浅黄色固体;溶液中
是浅黄色固体;溶液中 较稳定呈无色。某实验小组依次进行以下实验操作:
较稳定呈无色。某实验小组依次进行以下实验操作:
①向稀硫酸酸化的 溶液中加入适量
溶液中加入适量 ,溶液变为紫红色。
,溶液变为紫红色。
②继续滴加适量草酸 溶液,溶液紫红色褪去,并有
溶液,溶液紫红色褪去,并有 产生。
产生。
下列说法正确的是
 是浅黄色固体;溶液中
是浅黄色固体;溶液中 较稳定呈无色。某实验小组依次进行以下实验操作:
较稳定呈无色。某实验小组依次进行以下实验操作:①向稀硫酸酸化的
 溶液中加入适量
溶液中加入适量 ,溶液变为紫红色。
,溶液变为紫红色。②继续滴加适量草酸
 溶液,溶液紫红色褪去,并有
溶液,溶液紫红色褪去,并有 产生。
产生。下列说法正确的是
| A.Bi的基态原子中只含一个未成对电子 |
B.由操作①现象可知酸性条件下氧化性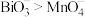 |
C.操作②中每生成标准状况下 ,反应转移1mol电子 ,反应转移1mol电子 |
D.向稀硫酸酸化的 中加入草酸,溶液会变为紫红色 中加入草酸,溶液会变为紫红色 |
您最近一年使用:0次
昨日更新
|
6次组卷
|
2卷引用:江苏省南京市第九中学2023-2024学年高一下学期教学质量调研(二)化学试题
名校
5 . 工业上用 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。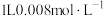 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。
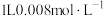 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
A.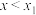 时, 时, 主要被氧化为 主要被氧化为 |
B.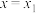 时,生成的 时,生成的 的物质的量为 的物质的量为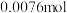 |
C.生成硝氮的离子方程式: |
D. 时,分批加入 时,分批加入 可以降低总氮残余率 可以降低总氮残余率 |
您最近一年使用:0次
名校
解题方法
6 . 用磷铁渣(含Fe、FeP、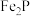 及少量杂质)制备磷酸铁晶体(
及少量杂质)制备磷酸铁晶体( )的工艺流程如下:
)的工艺流程如下:___________ 。
(2)“浸取”时,硝酸浓度过高会较多分解,化学方程式是___________ 。
(3)废气中含有 、NO,直接排放产生的危害主要有
、NO,直接排放产生的危害主要有___________ (写出两项),加入活性炭的目的是吸附氮氧化物;若用NaOH溶液吸收,物质的量比为 的
的 、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为
、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为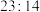 ,其化学式是
,其化学式是___________ 。
(4)若HNO₃的还原产物为NO,与1molFe2P完全反应而生成的NO有___________ mol。
(5)实验室完成操作X中用到的玻璃仪器有:烧杯、___________ 。
(6)“调pH”时,碱性过高产物中含铁量会增大,其原因有可能为___________ 。
(7)最终产品应洗涤,检验是否洗净的试剂是___________ 。
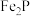 及少量杂质)制备磷酸铁晶体(
及少量杂质)制备磷酸铁晶体( )的工艺流程如下:
)的工艺流程如下:
(2)“浸取”时,硝酸浓度过高会较多分解,化学方程式是
(3)废气中含有
 、NO,直接排放产生的危害主要有
、NO,直接排放产生的危害主要有 的
的 、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为
、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为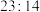 ,其化学式是
,其化学式是(4)若HNO₃的还原产物为NO,与1molFe2P完全反应而生成的NO有
(5)实验室完成操作X中用到的玻璃仪器有:烧杯、
(6)“调pH”时,碱性过高产物中含铁量会增大,其原因有可能为
(7)最终产品应洗涤,检验是否洗净的试剂是
您最近一年使用:0次
7 . 化学反应中伴随着能量变化,探究各种能量变化是一永恒的主题。回答下列问题:
(1)冷敷袋在日常生活中具有保鲜、降温和镇痛等多种用途。常见冷敷袋所盛装的主要物质为 和
和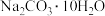 。
。
①写出 和
和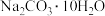 在一定条件下反应生成两种常见气体的化学方程式:
在一定条件下反应生成两种常见气体的化学方程式:______ 。
②该反应中反应物的总能量______ 生成物的总能量(填“大于”或“小于”)。
③某实验小组设计了如图甲中的三套实验装置,其中不能用来证明 和
和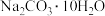 反应的能量变化情况的是
反应的能量变化情况的是______ (填序号)。 。
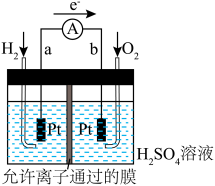
。______ (填“a”或“b”)极,电池工作时,溶液中 移向
移向______ (填“a”或“b”)极。
②若有4g 参加反应,则理论上
参加反应,则理论上 在b极获得电子的物质的量为
在b极获得电子的物质的量为______ 。
(3)已知合成氨反应: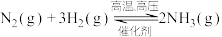 ,在—定温度下,向恒容的密闭容器中充入一定量的
,在—定温度下,向恒容的密闭容器中充入一定量的 和
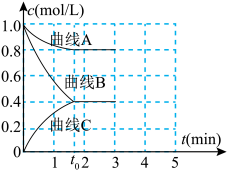
和 发生反应,测得各组分浓度随时间变化如下图所示。
发生反应,测得各组分浓度随时间变化如下图所示。
①表示c(H2)变化的曲线是______ (填“曲线A”、“曲线B”或“曲线C”)。
②下列描述一定能表示上述反应体系达平衡状态的是______ (填字母)。 ,同时生成2 mol的
,同时生成2 mol的
B. 的转化率不变
的转化率不变
C.容器内压强不再发生变化
D. 的百分含量不变
的百分含量不变
E.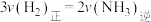
(4)已知: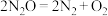 ,不同温度(T)下,恒容容器中
,不同温度(T)下,恒容容器中 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗—半时所需的相应时间),则
消耗—半时所需的相应时间),则
______ (填“>”“=”或“<”) 。当温度为
。当温度为 、起始压强为
、起始压强为 ,反应至
,反应至 min时,此时体系压强
min时,此时体系压强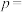
______ (用 表示)。
表示)。
(1)冷敷袋在日常生活中具有保鲜、降温和镇痛等多种用途。常见冷敷袋所盛装的主要物质为
 和
和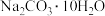 。
。①写出
 和
和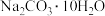 在一定条件下反应生成两种常见气体的化学方程式:
在一定条件下反应生成两种常见气体的化学方程式:②该反应中反应物的总能量
③某实验小组设计了如图甲中的三套实验装置,其中不能用来证明
 和
和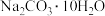 反应的能量变化情况的是
反应的能量变化情况的是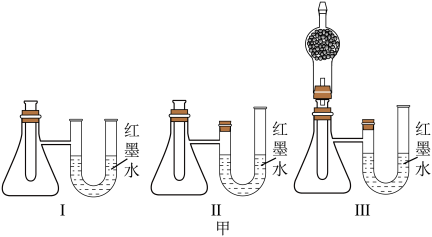
 。
。
 移向
移向②若有4g
 参加反应,则理论上
参加反应,则理论上 在b极获得电子的物质的量为
在b极获得电子的物质的量为(3)已知合成氨反应:
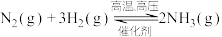 ,在—定温度下,向恒容的密闭容器中充入一定量的
,在—定温度下,向恒容的密闭容器中充入一定量的 和
和 发生反应,测得各组分浓度随时间变化如下图所示。
发生反应,测得各组分浓度随时间变化如下图所示。①表示c(H2)变化的曲线是
②下列描述一定能表示上述反应体系达平衡状态的是
 ,同时生成2 mol的
,同时生成2 mol的
B.
 的转化率不变
的转化率不变C.容器内压强不再发生变化
D.
 的百分含量不变
的百分含量不变E.
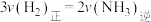
(4)已知:
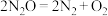 ,不同温度(T)下,恒容容器中
,不同温度(T)下,恒容容器中 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗—半时所需的相应时间),则
消耗—半时所需的相应时间),则
 。当温度为
。当温度为 、起始压强为
、起始压强为 ,反应至
,反应至 min时,此时体系压强
min时,此时体系压强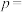
 表示)。
表示)。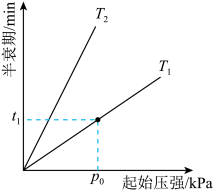
您最近一年使用:0次
名校
8 . Ⅰ.乙醇是重要的有机化工原料。
(1)下列关于乙醇的说法,正确的有___________ (填字母)。
A.将钠投入无水乙醇中,反应开始时,钠沉入液面下
B.钠与乙醇的反应比钠与水的反应更剧烈
C. 乙醇最多消耗
乙醇最多消耗 ,同时产生标准状况下
,同时产生标准状况下
D.可用酸性高锰酸钾溶液鉴别乙醇与乙酸
E.乙醇没有同分异构体
(2)乙醇分子结构中各化学键如图所示,则乙醇在铜催化下和氧气反应时断裂的键为①③。类比该反应断键原理,写出2-丙醇(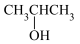 )发生催化氧化反应的化学方程式
)发生催化氧化反应的化学方程式___________ 。
实验步骤:
①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合液;
②按图示连接装置,使产生的蒸气经导管通入b试管所盛的饱和碳酸钠溶液(加入2滴酚酞试液)中:
④待b试管中收集到一定量产物时停止加热。撤下b试管并用力振荡,然后静置;
⑤分离出乙酸乙酯,洗涤,干燥。
回答下列问题:
(3)步骤③中不能用大火加热的原因有:___________ 。
(4)饱和碳酸钠溶液的作用除了提高水溶液的密度以加速乙酸乙酯与水溶液的分层外,还有___________ 。
(5)若现有乙酸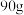 、乙醇
、乙醇 ,发生酯化反应制得
,发生酯化反应制得 乙酸乙酯,试计算该实验中乙酸乙酯的产率为
乙酸乙酯,试计算该实验中乙酸乙酯的产率为___________ (精确到0.1%,产率 )。
)。
(6)树德中学某化学兴趣小组同学利用上述装置进行实验后,取下b试管,振荡,发现红色迅速褪去。该小组同学查阅资料,并对此现象做了如下探究。
资料:酚酞难溶于水,易溶于有机溶剂。
①实验i:取振荡后的下层无色液体,分成两份,分别完成以下实验,根据实验结论完成下表
实验i说明溶液红色褪色的主要原因不是乙酸与碳酸钠发生了反应。
②实验ii:取 饱和碳酸钠溶液,滴入几滴酚酞试剂,溶液先变红,再加入
饱和碳酸钠溶液,滴入几滴酚酞试剂,溶液先变红,再加入 乙酸乙酯(不含乙酸)振荡,振荡后红色消失。根据上述实验i和实验ii现象,可得出的结论:溶液红色褪去的主要原因是
乙酸乙酯(不含乙酸)振荡,振荡后红色消失。根据上述实验i和实验ii现象,可得出的结论:溶液红色褪去的主要原因是___________ 。
③根据所得结论试分析,若取原振荡后的上层液体,加入饱和碳酸钠溶液,振荡,实验现象为:___________ ,振荡、静置分层后,___________ 。
(1)下列关于乙醇的说法,正确的有
A.将钠投入无水乙醇中,反应开始时,钠沉入液面下
B.钠与乙醇的反应比钠与水的反应更剧烈
C.
 乙醇最多消耗
乙醇最多消耗 ,同时产生标准状况下
,同时产生标准状况下
D.可用酸性高锰酸钾溶液鉴别乙醇与乙酸
E.乙醇没有同分异构体
(2)乙醇分子结构中各化学键如图所示,则乙醇在铜催化下和氧气反应时断裂的键为①③。类比该反应断键原理,写出2-丙醇(
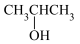 )发生催化氧化反应的化学方程式
)发生催化氧化反应的化学方程式
实验步骤:
①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合液;
②按图示连接装置,使产生的蒸气经导管通入b试管所盛的饱和碳酸钠溶液(加入2滴酚酞试液)中:

④待b试管中收集到一定量产物时停止加热。撤下b试管并用力振荡,然后静置;
⑤分离出乙酸乙酯,洗涤,干燥。
回答下列问题:
(3)步骤③中不能用大火加热的原因有:
(4)饱和碳酸钠溶液的作用除了提高水溶液的密度以加速乙酸乙酯与水溶液的分层外,还有
(5)若现有乙酸
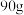 、乙醇
、乙醇 ,发生酯化反应制得
,发生酯化反应制得 乙酸乙酯,试计算该实验中乙酸乙酯的产率为
乙酸乙酯,试计算该实验中乙酸乙酯的产率为 )。
)。(6)树德中学某化学兴趣小组同学利用上述装置进行实验后,取下b试管,振荡,发现红色迅速褪去。该小组同学查阅资料,并对此现象做了如下探究。
资料:酚酞难溶于水,易溶于有机溶剂。
①实验i:取振荡后的下层无色液体,分成两份,分别完成以下实验,根据实验结论完成下表
| 序号 | 实验操作 | 实验现象 |
| 1 | 滴加几滴酚酞试剂 | |
| 2 | 滴入乙酸溶液 |
②实验ii:取
 饱和碳酸钠溶液,滴入几滴酚酞试剂,溶液先变红,再加入
饱和碳酸钠溶液,滴入几滴酚酞试剂,溶液先变红,再加入 乙酸乙酯(不含乙酸)振荡,振荡后红色消失。根据上述实验i和实验ii现象,可得出的结论:溶液红色褪去的主要原因是
乙酸乙酯(不含乙酸)振荡,振荡后红色消失。根据上述实验i和实验ii现象,可得出的结论:溶液红色褪去的主要原因是③根据所得结论试分析,若取原振荡后的上层液体,加入饱和碳酸钠溶液,振荡,实验现象为:
您最近一年使用:0次
名校
9 . 中学教材对Cu与 的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.
的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.
Ⅰ.利用如图装置完成Cu与 制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.
制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.___________ ;
(2)用化学方程式解释C中液面上方为红棕色气体的原理___________ ;
(3)将分液漏斗中液体换为稀硫酸和硝酸钠混合液也出现了溶解现象。此时烧瓶中发生反应的离子方程式为___________ ;
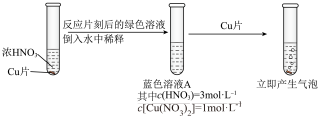
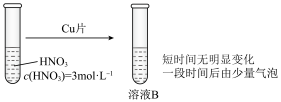
Ⅱ.深入研究时,有同学观察到了以下现象:实验1中蓝色溶液A遇铜片立即产生气泡;而相同条件下实验2中3mol/L硝酸遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。实验操作如下:
分析蓝色溶液A的成分后,学习小组探究蓝色溶液A与铜片能够立即发生反应的原因。
实验验证:
(4)将少量硫酸铜固体加入到 硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证
硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证___________ (填化学式)对该反应是否有催化作用。该同学这样做不能得出该物质不是催化剂的正确结论,还应该考虑___________ 和___________ 的影响;
(5)某同学又提出可能是 对该反应有催化作用。为了得出该结论,应该补充的实验为
对该反应有催化作用。为了得出该结论,应该补充的实验为___________ (写实验操作及现象)。
 的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.
的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.Ⅰ.利用如图装置完成Cu与
 制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.
制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.
(2)用化学方程式解释C中液面上方为红棕色气体的原理
(3)将分液漏斗中液体换为稀硫酸和硝酸钠混合液也出现了溶解现象。此时烧瓶中发生反应的离子方程式为
Ⅱ.深入研究时,有同学观察到了以下现象:实验1中蓝色溶液A遇铜片立即产生气泡;而相同条件下实验2中3mol/L硝酸遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。实验操作如下:
| 实验1 |
|
| 实验2 |
|
实验验证:
(4)将少量硫酸铜固体加入到
 硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证
硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证(5)某同学又提出可能是
 对该反应有催化作用。为了得出该结论,应该补充的实验为
对该反应有催化作用。为了得出该结论,应该补充的实验为
您最近一年使用:0次
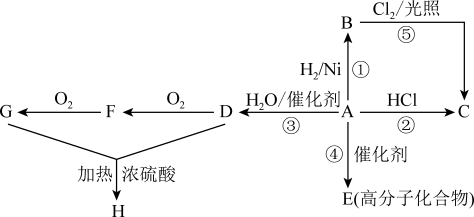
10 . 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂。
(1)写出A、B、D、E的结构简式:A___________ ,B___________ ,D___________ ,F___________ 。
(2)A能发生聚合反应,其产物为E,E的结构简式为___________ 。
(3)写出②反应的化学反应方程式以及反应类型:②___________ ;反应类型___________ 。
(4)D可以在铜或者银的催化下,逐步氧化,请写出D氧化为F的化学反应方程式以及反应类型:D→F___________ ;反应类型___________ 。
(5)写出D和G生成H的化学反应方程式:D+G→H___________ 。
(6)反应②⑤均可制氯乙烷,反应___________ 最好(填反应序号),原因是___________ 。
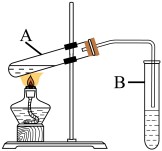
(7)反应D+G→H的实验装置如图所示,试管B中在反应前加入的是___________ 。
(1)写出A、B、D、E的结构简式:A
(2)A能发生聚合反应,其产物为E,E的结构简式为
(3)写出②反应的化学反应方程式以及反应类型:②
(4)D可以在铜或者银的催化下,逐步氧化,请写出D氧化为F的化学反应方程式以及反应类型:D→F
(5)写出D和G生成H的化学反应方程式:D+G→H
(6)反应②⑤均可制氯乙烷,反应
(7)反应D+G→H的实验装置如图所示,试管B中在反应前加入的是
您最近一年使用:0次