1 . 铁及其化合物在生产、生活中有重要用途。
(1)常温下,可用铁质容器盛放浓硫酸。原因是___ 。
(2)鉴别FeCl3溶液和Fe(OH)3胶体,除观察颜色外。还能用到的方法是__ 。
(3)Fe2+和Fe3+可以相互转化,若要证明溶液中的Fe2+被氧化生成了Fe3+,可选用的试剂是___ (填化学式)。
(4)保存1.6mol·L-1的FeSO4溶液时,为确保溶液中不出现浑浊。应调节溶液的pH不超过__ (已知:常温下,Ksp[Fe(OH)2]=1.6×10-16)
(5)在日常生活和生产中,钢铁的腐蚀普遍存在且危害较大。了解钢铁防离蚀的措施意义重大。利用如图所示装置可以模拟铁的电化学防护。其中Y为NaCl为减缓铁的腐蚀。

①着X为锌、开关K置于M处。这一保护方法叫做___ 。
②若X为碳棒、开关K置于N处,此时铁极为___ (填“阴极”或“阳极”),X极的电极反应式为__ 。
(1)常温下,可用铁质容器盛放浓硫酸。原因是
(2)鉴别FeCl3溶液和Fe(OH)3胶体,除观察颜色外。还能用到的方法是
(3)Fe2+和Fe3+可以相互转化,若要证明溶液中的Fe2+被氧化生成了Fe3+,可选用的试剂是
(4)保存1.6mol·L-1的FeSO4溶液时,为确保溶液中不出现浑浊。应调节溶液的pH不超过
(5)在日常生活和生产中,钢铁的腐蚀普遍存在且危害较大。了解钢铁防离蚀的措施意义重大。利用如图所示装置可以模拟铁的电化学防护。其中Y为NaCl为减缓铁的腐蚀。

①着X为锌、开关K置于M处。这一保护方法叫做
②若X为碳棒、开关K置于N处,此时铁极为
您最近一年使用:0次
12-13高一上·广东·期末
名校
解题方法
2 . 有KCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可把它们鉴别出来,这种试剂是
| A.盐酸 | B.烧碱溶液 | C.氨水 | D.KSCN溶液 |
您最近一年使用:0次
2020-08-22更新
|
617次组卷
|
67卷引用:贵州省金沙县金沙中学2017-2018学年高一下学期开学检测化学试题
贵州省金沙县金沙中学2017-2018学年高一下学期开学检测化学试题2016-2017学年山东省烟台第二中学高一下学期开学考试化学试卷安徽省合肥第十一中学2019-2020学年高二上学期入学考试化学试题云南省文山州砚山县一中2020届高三上学期开学考试化学试题贵州省遵义市南白中学2019-2020学年高一上学期第三次月考化学试题四川省自贡市田家炳中学2020-2021学年高一下学期开学考试化学试题(已下线)2011-2012学年广东省实验中学高一上学期期末考试化学试卷(已下线)2011-2012学年云南省玉溪一中高一下学期期中考试化学试卷(已下线)2011-2012学年海南省海南中学高一上学期期末考试化学试卷(已下线)2012-2013学年甘肃省兰州一中高一上学期期末考试化学试卷(已下线)2012-2013学年陕西省宝鸡中学高一上学期期末考试化学试卷(已下线)2012-2013学年黑龙江省集贤县第一中学高一上学期期末考试化学试卷(已下线)2013-2014学年吉林省长春外国语学校高一上学期期末理科化学试卷(已下线)2013-2014江苏省海门市第一学期期末教学质量调研高一化学试卷2014-2015学年湖北省荆门市高二下学期期末质量检测化学试卷2015-2016学年黑龙江省哈尔滨三中高一上期末化学试卷2015-2016学年甘肃省嘉峪关市酒钢三中高一上学期期末化学试卷2015-2016学年福建省莆田市二十五中高一下学期期中化学试卷2015-2016学年山东省济南一中高二下期中文科化学试卷2016-2017学年宁夏育才中学高一上月考二化学卷22016-2017学年湖南省长沙一中高一上阶段测二化学卷2016-2017学年山西省怀仁一中高一上月考三化学卷重庆市第一中学2016-2017学年高一上学期期末考试化学试题2016-2017学年江西省南昌市第十中学高一上学期期末考试化学试卷2016-2017学年山东省淄博市第七中学高一3月月考化学试卷河北省辛集市第一中学2018届高三上学期第一次月考化学试题吉林省长春外国语学校2017-2018学年高一上学期期末考试(理)化学试题内蒙古太仆寺旗宝昌一中2017-2018学年高一上学期期末考试化学试卷吉林省扶余市第一中学2017-2018学年高一上学期期末考试化学试题江西省临川实验学校2017-2018学年高一上学期期末质量检测化学试题湖北省沙市中学2017-2018学年高一上学期期末考试化学试题【全国校级联考】湖北省鄂西南三校合作体2017-2018学年高一下学期期中考试化学试题内蒙古赤峰市宁城县2017-2018学年高一上学期期末考试化学试题河北省承德市第一中学2018-2019学年高一上学期第三次月考化学试题四川省三台中学实验学校2018-2019学年高一上学期12月月考化学试题山西省忻州市实验中学2018-2019学年高一上学期第三次教学质量检测化学试题【全国百强校】湖南省长沙市雅礼中学2018-2019学年高一第一学期12月月考化学试题山西省晋中市平遥县第二中学2018-2019学年高一上学期12月月考化学试题【校级联考】湖南省醴陵二中、醴陵四中2018-2019学年高一上学期期末联考化学试题【校级联考】江西省南昌市八一中学、洪都中学2018-2019学年高一上学期期末考试化学试题(已下线)【走进新高考】(人教版必修一)3.2.2几种重要金属化合物——铁的重要化合物 同步练习01步步为赢 高二化学暑假作业:作业四 金属及其化合物福建省福州市琅岐中学2017-2018学年高二下学期期中考试化学试题山西省晋中市平遥县第二中学2019-2020学年高一12月月考化学试题吉林省长春市榆树市2019-2020学年高一上学期期末考试化学试题河南省开封市五县联考2019-2020学年高一上学期期末考试化学试题山东省临沂市罗庄区2019-2020学年高一下学期期末考试化学试题河北省唐山市第一中学2019-2020学年高一上学期12月质量检测化学试题(已下线)3.1.2 铁及其化合物之间的转化关系练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)陕西省榆林市第十二中学2021届高三上学期第一次月考化学试题陕西省西安市第八十五中学2019-2020学年高一上学期期末考试化学试题(已下线)第三章 铁 金属材料(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)3.2.2 铝的重要化合物(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)(已下线)3.1.2 铁的重要化合物(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)练习5 铁及其化合物2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)(已下线)【浙江新东方】在线化学 (16)(已下线)【浙江新东方】在线化学34广东省广州市广雅中学2020-2021学年高一上学期12月阶段测试化学试题四川省内江市第六中学2020-2021学年高一上学期元月月考化学试题四川宜宾屏山县中学校2020-2021学年高一下学期第一次月考化学试题江西省进贤县第一中学2020-2021学年高一上学期期末考试化学试题吉林省长春市第二中学2021-2022学年高一上学期期末化学试题陕西省西安高级中学2021-2022学年高一上学期期末考试化学试题上海市黄浦区联合体2021-2022学年高二下学期联合体期末模拟考试化学试题重庆市巫山县官渡中学2020-2021学年高一下学期第二次月考化学试题西藏拉萨那曲高级中学2020-2021学年高一下学期期中考试化学试题山西省运城市高中联合体2019-2020高一上学期12月月考化学试题
3 . 有下列物质:①小苏打、②硫酸铝、③氯化铁、④磁性氧化铁、⑤氢氧化铁,其中能通过化合反应制得的是( )
| A.①②④⑤ | B.①③④⑤ | C.②③④⑤ | D.①②③④ |
您最近一年使用:0次
2019-09-29更新
|
144次组卷
|
4卷引用:贵州省桐梓县育才中学2019-2020学年高二上学期开学考试化学试题
4 . 如图所涉及的物质均为中学化学中的常见物质,其中D为黄绿色的气体,E为Fe单质,它们存在如下转化关系,反应中生成的水及次要产物均已略去.
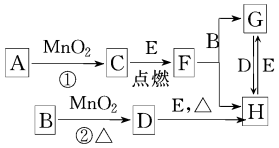
(1)写出有关物质的名称:B__________ ,F______________
(2)写出F与金属铝在高温下的反应化学方程式____________________________
(3)若反应①是在加热条件下进行的,则A是____________ (填化学式);
(4)指出MnO2在相关反应中的作用:反应②中是________ 剂.
(5)写出B与MnO2共热获得D的化学方程式:__________________________ .
(6)实验室检验H中的阳离子的方法是______________________________

(1)写出有关物质的名称:B
(2)写出F与金属铝在高温下的反应化学方程式
(3)若反应①是在加热条件下进行的,则A是
(4)指出MnO2在相关反应中的作用:反应②中是
(5)写出B与MnO2共热获得D的化学方程式:
(6)实验室检验H中的阳离子的方法是
您最近一年使用:0次
名校
5 . 为除去某物质中少量杂质,下列所加试剂及操作方法正确的是(括号内的物质为杂质)( )
| A.NaCl溶液(BaCl2):加过量Na2CO3溶液,过滤 |
| B.KNO3溶液(NaCl):加热蒸发得浓溶液后,降温 |
| C.SO2(CO2):通入过量NaOH溶液,洗气 |
| D.Cl2(HCl):依次通入饱和食盐水、浓硫酸,洗气 |
您最近一年使用:0次
2018-09-05更新
|
132次组卷
|
2卷引用:【全国百强校】贵州省铜仁市第一中学2018-2019学年高二上学期开学考试化学试题
6 . 化学实验装置的科学设计是实验是否取得预期效果的关键。请回答下列有关实验装置的相关问题:
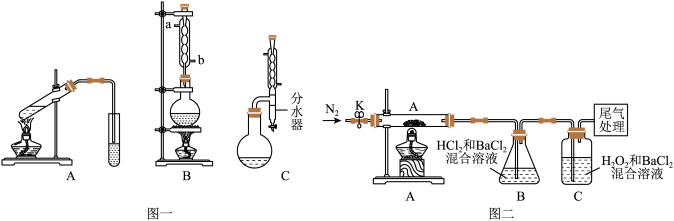
I.图一中A为教材制备乙酸乙酯的实验装置,甲同学认为图一中B装置比A要好,则冷却水应从______ 口进入;乙同学认为图一中C装置效果更好,理由是_______ 。
Ⅱ.“摩尔盐”[(NH4)2Fe(SO4)2•6H2O]是分析化学中的重要试剂。已知:摩尔盐隔绝空气加热至500℃时可完全分解。某学习小组欲探究其分解产物。
(1)[提出猜想]小组同学认为分解产物可能有以下几种情况:
A.Fe2O3、SO2、NH3、H2O B.FeO、SO3、NH3、H2O
C.FeO、SO2、NH3、H2O D.Fe2O3、SO3、SO2、NH3、H2O
根据所学知识,可确定_________ 不成立(填序号)
(2)[药品验纯]甲同学提出可以用湿润的红色石蕊试纸、稀盐酸和_________ 溶液检验出“摩尔盐”中的三种离子;取一定量的“摩尔盐”配成溶液,取少量溶液置于试管中,向其中滴加_______ (填试剂名称和实验现象),则“摩尔盐”未因氧化而变质。
(3)[实验探究]为检验分解产物,甲同学设计了如下实验装置。
①取一定量“摩尔盐”置于加热管A中,加热至分解完全后打开K,再通入N2,目的是________ 。
②实验中观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀.C中发生反应的离子方程式为________ 。
③实验验证取A中残留物少许加入稀硫酸溶解,再滴入KMnO4稀溶液,不褪色证明产物不含______ 。
(4)[实验结论与反思]通过实验现象和认真反思,上述猜想中一定正确的是______ 。(填序号)

I.图一中A为教材制备乙酸乙酯的实验装置,甲同学认为图一中B装置比A要好,则冷却水应从
Ⅱ.“摩尔盐”[(NH4)2Fe(SO4)2•6H2O]是分析化学中的重要试剂。已知:摩尔盐隔绝空气加热至500℃时可完全分解。某学习小组欲探究其分解产物。
(1)[提出猜想]小组同学认为分解产物可能有以下几种情况:
A.Fe2O3、SO2、NH3、H2O B.FeO、SO3、NH3、H2O
C.FeO、SO2、NH3、H2O D.Fe2O3、SO3、SO2、NH3、H2O
根据所学知识,可确定
(2)[药品验纯]甲同学提出可以用湿润的红色石蕊试纸、稀盐酸和
(3)[实验探究]为检验分解产物,甲同学设计了如下实验装置。
①取一定量“摩尔盐”置于加热管A中,加热至分解完全后打开K,再通入N2,目的是
②实验中观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀.C中发生反应的离子方程式为
③实验验证取A中残留物少许加入稀硫酸溶解,再滴入KMnO4稀溶液,不褪色证明产物不含
(4)[实验结论与反思]通过实验现象和认真反思,上述猜想中一定正确的是
您最近一年使用:0次
2019-09-29更新
|
186次组卷
|
7卷引用:贵州省遵义正安县一中2020届高三上学期开学考试化学试题
名校
7 . 下列离子方程式正确的是
| A.向FeCl3溶液中加入过量铁粉:Fe3++Fe===2Fe2+ |
| B.铜溶于稀硝酸:3Cu+8H++2NO3-===3Cu2++2NO↑+4H2O |
| C.向稀硫酸中加入 Ba(OH)2溶液:Ba2++OH-+H++SO42-===BaSO4↓+H2O |
| D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2Na+ |
您最近一年使用:0次
2018-01-13更新
|
554次组卷
|
11卷引用:贵州省正安县第二中学2019-2020学年高二上学期开学考试化学试题
贵州省正安县第二中学2019-2020学年高二上学期开学考试化学试题贵州省剑河县二中2018-2019学年高一上学期期末考试化学试题云南省镇沅县第一中学校2021-2022学年高一下学期开学考试化学试题浙江省东阳市横店高级中学2021-2022学年高一下学期开学考试检测化学试题云南省梁河县第一中学2021-2022学年高一下学期开学考试化学试题山东省昌邑市第一中学2017-2018学年高一1月份期末模拟考试化学试题苏教版高中化学必修1专题二《 从海水中获得的化学物质》测试卷云南省普洱市镇沅县第一中学2019—2020学年高一上学期期末考试化学试题(已下线)【南昌新东方】莲塘二中 2019-2020 高一(上)期末江西省南昌市南昌县莲塘第二中学2019-2020学年高一上学期期末考试化学试题新疆昌吉教育共同体2020-2021学年高一下学期期末质量检测化学试题
14-15高三上·河南焦作·期中
8 . 已知酸性高锰酸钾溶液可以将FeSO4氧化,化学方程式为2KMnO4+10FeSO4+8H2SO4=K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示。则下列有关说法不正确的是( )
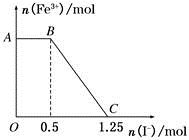

| A.图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C.根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25 mol |
| D.根据OC段的数据可知开始加入的硫酸亚铁的物质的量为1 mol |
您最近一年使用:0次
2016-12-09更新
|
288次组卷
|
5卷引用:贵州省遵义正安县一中2020届高三上学期开学考试化学试题
贵州省遵义正安县一中2020届高三上学期开学考试化学试题(已下线)2015届河南省焦作市高三上学期期中化学试卷云南省河口县第一中学2019届高三上学期期中考试理科综合化学试题江西省南昌市新建县第一中学2020届高三上学期第一次月考化学试题(已下线)上海市奉贤区2014届高三1月调研(期末)测试化学试题
10-11高一·云南玉溪·期末
9 . 要检验久置的FeSO4溶液是否含有Fe2(SO4)3,应选用的试剂是
| A.NH4SCN溶液 | B.KI溶液 | C.氨水 | D.Fe粉 |
您最近一年使用:0次



