19-20高三·浙江·阶段练习
1 . I.无机矿物盐X含五种元素,某学习小组进行了如下实验:
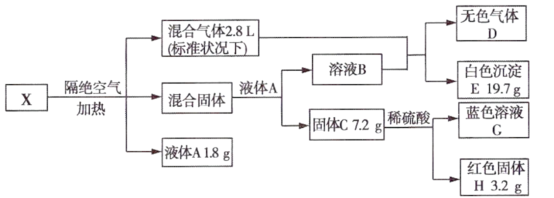
已知:混合固体由两种物质组成,物质的量之比为2:1,总质量为22.5g;通入混合气体后溶液B中溶质恰好反应完全,白色沉淀E可溶于稀盐酸;无色气体D为单一气体,可使带火星木条复燃;固体C为砖红色。
请回答:.
(1)X中5种元素是____________ (用元素符号表示)。
(2)无机矿物盐X的化学式为____________ 。
(3)固体C与稀硫酸反应的离子方程式为____________ 。
II.某学习小组在研究CH4还原Fe2O3的实验中,发现生成的黑色粉末能被磁铁吸引。查阅资料得知:在温度不同、受热不均匀时会生成具有磁性的Fe3O4。为进一步探究黑色粉末的组成,他们进行了如下实验。
(1)往黑色粉末中滴加盐酸,观察到有气泡产生,则黑色粉末中一定有____________ 。
(2)用以下装置可以说明产物中有Fe3O4存在,检查装置的气密性。往装置中添加相应的药品,接下来的一步操作为____________ 。

(3)为进一步证明黑色粉末中是否含有Fe3O4,某同学设计的实验方案为:取少量黑色粉末于试管中,加足量盐酸,充分振荡使黑色粉末完全溶解,滴入KSCN溶液,观察现象。请分析此方案是否可行,并解释原因____________ 。

已知:混合固体由两种物质组成,物质的量之比为2:1,总质量为22.5g;通入混合气体后溶液B中溶质恰好反应完全,白色沉淀E可溶于稀盐酸;无色气体D为单一气体,可使带火星木条复燃;固体C为砖红色。
请回答:.
(1)X中5种元素是
(2)无机矿物盐X的化学式为
(3)固体C与稀硫酸反应的离子方程式为
II.某学习小组在研究CH4还原Fe2O3的实验中,发现生成的黑色粉末能被磁铁吸引。查阅资料得知:在温度不同、受热不均匀时会生成具有磁性的Fe3O4。为进一步探究黑色粉末的组成,他们进行了如下实验。
(1)往黑色粉末中滴加盐酸,观察到有气泡产生,则黑色粉末中一定有
(2)用以下装置可以说明产物中有Fe3O4存在,检查装置的气密性。往装置中添加相应的药品,接下来的一步操作为

(3)为进一步证明黑色粉末中是否含有Fe3O4,某同学设计的实验方案为:取少量黑色粉末于试管中,加足量盐酸,充分振荡使黑色粉末完全溶解,滴入KSCN溶液,观察现象。请分析此方案是否可行,并解释原因
您最近一年使用:0次
2 . 某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如下,请回答下列问题:

(1)步骤①的作用是清洗废铁屑表面的油污,其中加热的目的是____________ 。
(2)写出步骤②中生成 的离子方程式
的离子方程式______________________ 。(写一个即可)
(3)步骤③中“氯气”不引入杂质但有毒,可以用___________ 代替(填化学式)。
(4)若溶液B中只含有 而不含
而不含 ,可证明该事实的实验操作是
,可证明该事实的实验操作是__________ 。
(5)步骤⑤产生金属铜的化学方程式为______________________________ 。

(1)步骤①的作用是清洗废铁屑表面的油污,其中加热的目的是
(2)写出步骤②中生成
 的离子方程式
的离子方程式(3)步骤③中“氯气”不引入杂质但有毒,可以用
(4)若溶液B中只含有
 而不含
而不含 ,可证明该事实的实验操作是
,可证明该事实的实验操作是(5)步骤⑤产生金属铜的化学方程式为
您最近一年使用:0次
11-12高三上·黑龙江牡丹江·期末
3 . 某同学欲在实验室中完成Fe与水蒸气反应的实验,装置如图甲、乙两种。
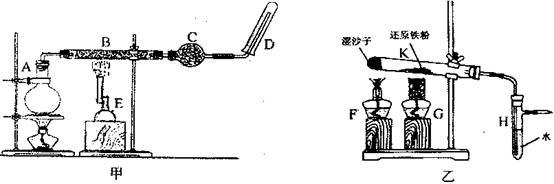
已知B中放入的是铁与石棉绒的混合物,C中放的是干燥剂,E为酒精喷灯,G为带有铁丝网罩的酒精灯。
Ⅰ.对比两装置,回答下列问题:
(1)如何检查乙装置的气密性?_____________________________________ 。
(2)乙装置中湿沙子的作用是________________________________________ 。
(3)B处发生反应的化学方程式:__________________________________________ 。
(4)该同学认为欲在乙装置的尖嘴导管处点燃反应产生的气体,装置H必不可少,H的作用是__________________ 。
(5)对比甲、乙两装置的B和K,B的优点是______________________________ 。
Ⅱ.某同学为了研究一定时间内铁粉的转化率,用上图中的甲装置设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成的气体体积,计算铁粉的转化率。
①用排水法收集并测量气体体积可选下图中的_________________ 装置。
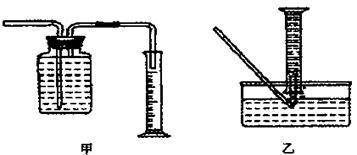
②称取mg铁粉与适量石棉绒混合,然后加热至无气体放出。若收集的气体体积换算为标准状况为VL,铁粉的转化率为(列出计算式即可)________________________ 。
③为了证明反应后的固体混合物中含有+3价的Fe,该同学取出少量混合物于试管中,加入足量的盐酸,溶解后过滤,立即向溶液中滴加KSCN溶液,结果观察到溶液的颜色没变化。经过思考,该同学认为此现象不能说明反应后的固体混合物中不含有+3价Fe。他的理由是:______________ 。

已知B中放入的是铁与石棉绒的混合物,C中放的是干燥剂,E为酒精喷灯,G为带有铁丝网罩的酒精灯。
Ⅰ.对比两装置,回答下列问题:
(1)如何检查乙装置的气密性?
(2)乙装置中湿沙子的作用是
(3)B处发生反应的化学方程式:
(4)该同学认为欲在乙装置的尖嘴导管处点燃反应产生的气体,装置H必不可少,H的作用是
(5)对比甲、乙两装置的B和K,B的优点是
Ⅱ.某同学为了研究一定时间内铁粉的转化率,用上图中的甲装置设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成的气体体积,计算铁粉的转化率。
①用排水法收集并测量气体体积可选下图中的

②称取mg铁粉与适量石棉绒混合,然后加热至无气体放出。若收集的气体体积换算为标准状况为VL,铁粉的转化率为(列出计算式即可)
③为了证明反应后的固体混合物中含有+3价的Fe,该同学取出少量混合物于试管中,加入足量的盐酸,溶解后过滤,立即向溶液中滴加KSCN溶液,结果观察到溶液的颜色没变化。经过思考,该同学认为此现象不能说明反应后的固体混合物中不含有+3价Fe。他的理由是:
您最近一年使用:0次
4 . 将一定量的Fe、 、CuO的混合物放入100mL
、CuO的混合物放入100mL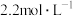 的
的 溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有
溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有 (假设滤液体积仍为100mL)。向滤液中滴加
(假设滤液体积仍为100mL)。向滤液中滴加 NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是
NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是
 、CuO的混合物放入100mL
、CuO的混合物放入100mL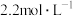 的
的 溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有
溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有 (假设滤液体积仍为100mL)。向滤液中滴加
(假设滤液体积仍为100mL)。向滤液中滴加 NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是
NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是| A.CuO的质量为1.6g |
B.未滴加NaOH溶液前滤液中 的物质的量浓度为 的物质的量浓度为 |
C.溶液中 和 和 消耗铁的物质的量之比为2:1 消耗铁的物质的量之比为2:1 |
| D.Fe在溶液中共参与了三个反应 |
您最近一年使用:0次
解题方法
5 . 某红色粉末样品可能含有 和
和 中的一种或两种,为探究其组成,研究组同学取少量样品加入过量稀硫酸进行实验。(已知:
中的一种或两种,为探究其组成,研究组同学取少量样品加入过量稀硫酸进行实验。(已知: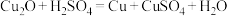 )下列有关说法正确的是
)下列有关说法正确的是
 和
和 中的一种或两种,为探究其组成,研究组同学取少量样品加入过量稀硫酸进行实验。(已知:
中的一种或两种,为探究其组成,研究组同学取少量样品加入过量稀硫酸进行实验。(已知: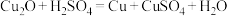 )下列有关说法正确的是
)下列有关说法正确的是A.若固体部分溶解,则样品中一定含有 ,一定不含有 ,一定不含有 |
B.若固体全部溶解,则发生的离子反应只有: |
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红,则样品中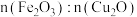 为2∶1 为2∶1 |
D.另取ag样品在空气中充分加热至质量不再变化,称其质量为bg(b>a),则混合物中 的质量分数为 的质量分数为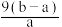 |
您最近一年使用:0次
名校
6 . 钢铁制品经常要进行烤蓝处理,即在铁制品的表面生成一层致密的 。某化学兴趣小组为了研究烤蓝铁片,进行了以下实验操作:
。某化学兴趣小组为了研究烤蓝铁片,进行了以下实验操作:
Ⅰ.把一定量烤蓝铁片加工成均匀粉末;
Ⅱ.取一定量的粉末,放入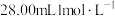 的盐酸中,二者恰好完全反应,生成
的盐酸中,二者恰好完全反应,生成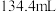 (标况)
(标况) ,再向溶液中滴入KSCN溶液,无现象。
,再向溶液中滴入KSCN溶液,无现象。
已知:①不考虑空气对反应的影响;②杂质不参与反应。
下列说法错误的是
 。某化学兴趣小组为了研究烤蓝铁片,进行了以下实验操作:
。某化学兴趣小组为了研究烤蓝铁片,进行了以下实验操作:Ⅰ.把一定量烤蓝铁片加工成均匀粉末;
Ⅱ.取一定量的粉末,放入
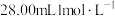 的盐酸中,二者恰好完全反应,生成
的盐酸中,二者恰好完全反应,生成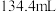 (标况)
(标况) ,再向溶液中滴入KSCN溶液,无现象。
,再向溶液中滴入KSCN溶液,无现象。已知:①不考虑空气对反应的影响;②杂质不参与反应。
下列说法错误的是
A.由实验可知,反应后所得的溶液中一定无 |
B.样品中氧元素的物质的量为 |
| C.样品中铁元素的含量约为70% |
D.若将生成的 恰好全部与灼热的氧化铜反应,最多可得到 恰好全部与灼热的氧化铜反应,最多可得到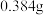 铜单质 铜单质 |
您最近一年使用:0次
2023-01-22更新
|
685次组卷
|
2卷引用:吉林省长春市东北师大附属中学2022-2023学年高一上学期期末考试化学试题
7 . 铁在冷的稀硝酸中反应的主要还原产物为NO,而在热的稀硝酸中反应其主要还原产物为 ,当溶液更稀主要还原产物为
,当溶液更稀主要还原产物为 ,现向一定量的冷的稀硝酸中逐渐加入铁,如图为反应液中
,现向一定量的冷的稀硝酸中逐渐加入铁,如图为反应液中 的浓度与产生的气体量随铁的物质的量的变化情况(假设在任一气体产生曲线段内只有一种还原产物),下列有关说法不正确的是(已知:
的浓度与产生的气体量随铁的物质的量的变化情况(假设在任一气体产生曲线段内只有一种还原产物),下列有关说法不正确的是(已知: )
)
 ,当溶液更稀主要还原产物为
,当溶液更稀主要还原产物为 ,现向一定量的冷的稀硝酸中逐渐加入铁,如图为反应液中
,现向一定量的冷的稀硝酸中逐渐加入铁,如图为反应液中 的浓度与产生的气体量随铁的物质的量的变化情况(假设在任一气体产生曲线段内只有一种还原产物),下列有关说法不正确的是(已知:
的浓度与产生的气体量随铁的物质的量的变化情况(假设在任一气体产生曲线段内只有一种还原产物),下列有关说法不正确的是(已知: )
)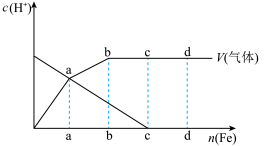
| A.若oa段与ab段铁的物质的量相等,则这两段所产生的气体的物质的量之比为2:1 |
B.bc段发生反应的离子方程式为: |
C.反应到达c点时,溶液中主要阳离子是 |
| D.若反应到达d点时反应完全结束,c、d两点对应的铁的物质的量之比为2:3 |
您最近一年使用:0次
名校
解题方法
8 . 部分氧化的Fe—Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如图处理:

下列说法不正确的是

下列说法不正确的是
| A.样品中Fe元素的质量为2.24 g |
| B.V<896 |
| C.参与反应的n(H2SO4) = 0.04 mol |
| D.滤液A中的阳离子为Fe2+、Cu2+、H+ |
您最近一年使用:0次
9 . 实验室中利用氧化铜和氧化铁混合物进行如图实验。下列说法错误的是

| A.“3.04g固体”一定是铁铜混合物 |
| B.“溶液2”中溶质的物质的量为0.1mol |
| C.混合物中含氧元素的物质的量为0.06mol |
| D.反应②能生成0.04gH2 |
您最近一年使用:0次
2022-04-14更新
|
2007次组卷
|
7卷引用:山东省青岛市2021-2022学年高三下学期第一次模拟考试化学试题
山东省青岛市2021-2022学年高三下学期第一次模拟考试化学试题(已下线)专题讲座(一) 化学计算的常用方法(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第07练 铁及其化合物-2023年高考化学一轮复习小题多维练(全国通用)山东省青岛第三十九中学2022-2023学年高三上学期期中考试化学试题湖北省武汉市第三中学2022-2023学年高一上学期12月月考化学试题(已下线)题型8 利用守恒关系的计算-高考必备50个题型浙江省杭州市西湖高级中学2023-2024学年高一下学期4月期中考试化学试题
10 . 向含xmolHNO3和ymolH2SO4的混合稀溶液中缓慢加入铁粉,其氧化产物与所加铁粉的物质的量关系如图所示:
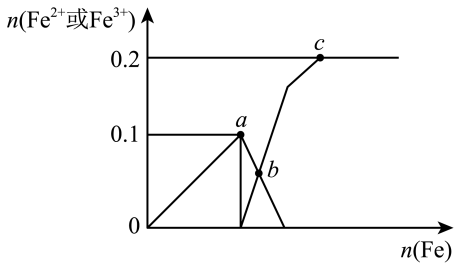
| A.x=0.2,y=0.1 |
B.a点之前的反应离子方程式为3Fe+8H++2NO =3Fe2++2NO↑+4H2O =3Fe2++2NO↑+4H2O |
| C.向b点所得溶液中加入Cu粉,最多可溶解1.92g |
| D.反应至c点,可收集到气体4.48L(标准状况) |
您最近一年使用:0次
2022-01-13更新
|
0次组卷
|
6卷引用:河北省唐山市2021-2022学年高三上学期期末考试化学试题



