解题方法
1 . 除去I中少量的II,所采用的方法正确的是
| 选项 | I | II | 方法 |
| A | 乙酸溶液 | 乙二酸 | 滴加酸性高锰酸钾溶液 |
| B | 氯化铁溶液 | 氯化铜 | 加入铁粉 |
| C | 一氧化氮气体 | 氨气 | 通过盛有氯化钙粉末的干燥管 |
| D | 二氧化硫气体 | 二氧化碳 | 通过盛有饱和亚硫酸氢钠溶液的洗气瓶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 把铁片放入下列溶液中,铁片溶解且溶液的质量增大的是
| A.FeCl3溶液 | B.AgNO3溶液 | C.AlCl3溶液 | D.CuSO4溶液 |
您最近一年使用:0次
3 . 把一定量铁粉放入氯化铁溶液中,完全反应后,已反应的Fe3+和未反应的Fe3+的物质的量之比为1:1,则所得溶液中Fe2+和Fe3+的物质的量之比为
| A.2:1 | B.3:2 | C.1:1 | D.2:3 |
您最近一年使用:0次
4 . 下列离子方程式书写正确的是
A.向稀硝酸中加入足量铁粉: |
B.用 制备84消毒液: 制备84消毒液: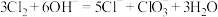 |
C.向碳酸氢铵溶液中加入过量NaOH溶液: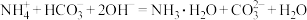 |
D.向双氧水中通入少量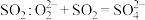 |
您最近一年使用:0次
名校
解题方法
5 . 某工厂以矿石(主要成分为 ,还含Al2O3、CuO、
,还含Al2O3、CuO、 等不溶性杂质)为原料制备绿矾
等不溶性杂质)为原料制备绿矾 ,其生产工艺如图:
,其生产工艺如图:
(1)碱浸时,发生的反应主要有_______ (写离子方程式)和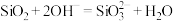 。
。
(2)将矿石变成矿粉的目的是_______ 。
(3)酸浸后的溶液中存在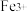 ,检验该离子的操作及现象为
,检验该离子的操作及现象为_______ 。
(4)滤渣2的主要成分是_______ (填化学式)。
(5)配制 溶液时,通常会在
溶液时,通常会在 溶液中加入少量的铁粉,请用离子方程式说明原因:
溶液中加入少量的铁粉,请用离子方程式说明原因:_______ 。
(6)防治缺铁性贫血的有效方法是补充铁剂,常见的补铁剂有硫酸亚铁、葡萄糖酸亚铁、富马酸亚铁等,通常搭配维生素C一起服用,体现了维生素C的_______ (填“氧化性”或“还原性”)。
(7)测定所得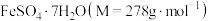 样品的纯度:取
样品的纯度:取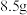 制得的
制得的 样品,将其配制成
样品,将其配制成 溶液,取
溶液,取 配制好的溶液置于锥形瓶中,加入
配制好的溶液置于锥形瓶中,加入 溶液,恰好完全反应(不考虑杂质参与反应,已知发生的反应为
溶液,恰好完全反应(不考虑杂质参与反应,已知发生的反应为 )。
)。
①若配制样品溶液的过程中,容量瓶中有少量蒸馏水残留,则对所配溶液浓度的影响是_______ (填“偏低”“偏高”或“无影响”)。
② 样品的纯度约为
样品的纯度约为_______ (保留三位有效数字)。
 ,还含Al2O3、CuO、
,还含Al2O3、CuO、 等不溶性杂质)为原料制备绿矾
等不溶性杂质)为原料制备绿矾 ,其生产工艺如图:
,其生产工艺如图: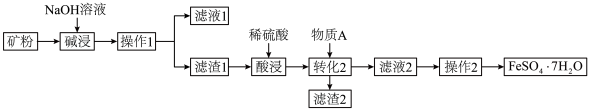
(1)碱浸时,发生的反应主要有
 。
。(2)将矿石变成矿粉的目的是
(3)酸浸后的溶液中存在
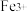 ,检验该离子的操作及现象为
,检验该离子的操作及现象为(4)滤渣2的主要成分是
(5)配制
 溶液时,通常会在
溶液时,通常会在 溶液中加入少量的铁粉,请用离子方程式说明原因:
溶液中加入少量的铁粉,请用离子方程式说明原因:(6)防治缺铁性贫血的有效方法是补充铁剂,常见的补铁剂有硫酸亚铁、葡萄糖酸亚铁、富马酸亚铁等,通常搭配维生素C一起服用,体现了维生素C的
(7)测定所得
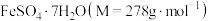 样品的纯度:取
样品的纯度:取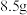 制得的
制得的 样品,将其配制成
样品,将其配制成 溶液,取
溶液,取 配制好的溶液置于锥形瓶中,加入
配制好的溶液置于锥形瓶中,加入 溶液,恰好完全反应(不考虑杂质参与反应,已知发生的反应为
溶液,恰好完全反应(不考虑杂质参与反应,已知发生的反应为 )。
)。①若配制样品溶液的过程中,容量瓶中有少量蒸馏水残留,则对所配溶液浓度的影响是
②
 样品的纯度约为
样品的纯度约为
您最近一年使用:0次
2024-09-03更新
|
109次组卷
|
2卷引用:陕西省西安市临潼区华清中学2023-2024学年高一上学期期末质量监测化学试题
6 . 铁及其化合物在生活、生产中有着重要作用。
(1)某学生欲用下列装置制取纯净 固体。其中A中发生的反应是
固体。其中A中发生的反应是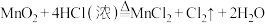 ,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网,F为干燥的空广口瓶,烧杯G为尾气吸收装置。试回答:
,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网,F为干燥的空广口瓶,烧杯G为尾气吸收装置。试回答:_______ 。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液
②该装置中有明显错误是_______ (填字母)。D中所装试剂为_______ ,C装置的作用是_______ 。
③向某无色溶液中加入含 的溶液后,无明显变化,当滴入几滴新制氯水后,混合液变成血红色,则下列结论正确的是
的溶液后,无明显变化,当滴入几滴新制氯水后,混合液变成血红色,则下列结论正确的是_______ 。
A.该溶液中一定含有 B.氧化性:
B.氧化性: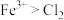
C. 与氯水形成红色物质 D.
与氯水形成红色物质 D. 被氯水还原为
被氯水还原为
④G中发生反应的离子方程式是_______ 。
⑤ 溶液用于刻制印刷铜电路板,发生反应的离子方程式为:
溶液用于刻制印刷铜电路板,发生反应的离子方程式为:_______ 。
若用所制取的 固体制成
固体制成 胶体,区分胶体和溶液常用
胶体,区分胶体和溶液常用_______ ,分离胶体和溶液常用的方法叫_______ 。
(2)高铁酸钾 是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示: 中铁元素的化合价为
中铁元素的化合价为_______ ;
②反应Ⅱ中的还原剂是_______ 。
(3)一定质量的FeO、 混合物,在足量
混合物,在足量 气流中加热充分反应,冷却后称得剩余固体全为铁单质,且比原固体混合物减轻了1.6g;将等质量的原混合物与硫酸反应,欲使之完全溶解,需
气流中加热充分反应,冷却后称得剩余固体全为铁单质,且比原固体混合物减轻了1.6g;将等质量的原混合物与硫酸反应,欲使之完全溶解,需 的硫酸的体积至少为
的硫酸的体积至少为_______ 。
(1)某学生欲用下列装置制取纯净
 固体。其中A中发生的反应是
固体。其中A中发生的反应是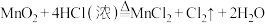 ,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网,F为干燥的空广口瓶,烧杯G为尾气吸收装置。试回答:
,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网,F为干燥的空广口瓶,烧杯G为尾气吸收装置。试回答: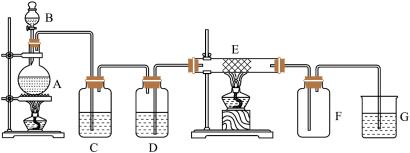
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液②该装置中有明显错误是
③向某无色溶液中加入含
 的溶液后,无明显变化,当滴入几滴新制氯水后,混合液变成血红色,则下列结论正确的是
的溶液后,无明显变化,当滴入几滴新制氯水后,混合液变成血红色,则下列结论正确的是A.该溶液中一定含有
 B.氧化性:
B.氧化性: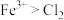
C.
 与氯水形成红色物质 D.
与氯水形成红色物质 D. 被氯水还原为
被氯水还原为
④G中发生反应的离子方程式是
⑤
 溶液用于刻制印刷铜电路板,发生反应的离子方程式为:
溶液用于刻制印刷铜电路板,发生反应的离子方程式为:若用所制取的
 固体制成
固体制成 胶体,区分胶体和溶液常用
胶体,区分胶体和溶液常用(2)高铁酸钾
 是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示: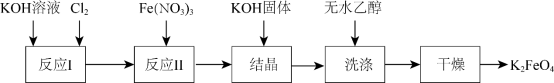
 中铁元素的化合价为
中铁元素的化合价为②反应Ⅱ中的还原剂是
(3)一定质量的FeO、
 混合物,在足量
混合物,在足量 气流中加热充分反应,冷却后称得剩余固体全为铁单质,且比原固体混合物减轻了1.6g;将等质量的原混合物与硫酸反应,欲使之完全溶解,需
气流中加热充分反应,冷却后称得剩余固体全为铁单质,且比原固体混合物减轻了1.6g;将等质量的原混合物与硫酸反应,欲使之完全溶解,需 的硫酸的体积至少为
的硫酸的体积至少为
您最近一年使用:0次
7 . 铁黄 (FeOOH) 难溶于水,可作颜料,也是制备饮水处理剂高铁酸钾的原料。 以烧渣(主要成分为Fe3O4 、CuO 、SiO2等)为原料出产铁黄的流程如图。___________ ,“酸浸”时,使用的酸为 ___________ 。
(2)“滤渣1”的成分为___________ (填化学式)。
(3)“还原””涉及的离子方程式有___________ 、 ___________ 。
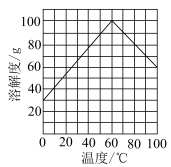
(4)FeSO4·7H2O 的溶解度曲线如图,从滤液2中获得晶体的 另一种方法是___________ 、冷却结晶。___________ 。
(6)以铁黄(FeOOH)等为原料制备高铁酸钾(K2FeO4)的工艺主要有两步:
①利用铁黄、NaClO和浓NaOH溶液反应制备Na2FeO4,该反应的氧化剂和还原剂的物质的量之比为___________ 。
②向Na2FeO4溶液中加入浓KOH制备K2FeO4,该反应涉及原理是相同温度下溶解度:K2FeO4___________ ( 填“>”“<”“=”)Na2FeO4。
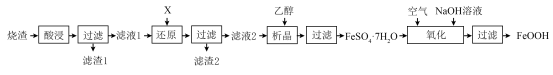
(2)“滤渣1”的成分为
(3)“还原””涉及的离子方程式有
(4)FeSO4·7H2O 的溶解度曲线如图,从滤液2中获得晶体的 另一种方法是
(6)以铁黄(FeOOH)等为原料制备高铁酸钾(K2FeO4)的工艺主要有两步:
①利用铁黄、NaClO和浓NaOH溶液反应制备Na2FeO4,该反应的氧化剂和还原剂的物质的量之比为
②向Na2FeO4溶液中加入浓KOH制备K2FeO4,该反应涉及原理是相同温度下溶解度:K2FeO4
您最近一年使用:0次
8 . 下列化学用语书写不正确 的是
| A.HCl溶于水发生电离:HCl=H++Cl- |
| B.铁和稀硫酸反应:Fe+2H+=Fe3++H2↑ |
| C.氯化铁溶液与铁粉反应:2Fe3++Fe=3Fe2+ |
| D.碳酸钙与稀盐酸:CaCO3+2H+ =Ca2++CO2↑+H2O |
您最近一年使用:0次
解题方法
9 . 将1.12 g铁粉加入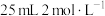 的氯化铁溶液中充分反应(忽略溶液体积的变化),下列相关叙述正确的是
的氯化铁溶液中充分反应(忽略溶液体积的变化),下列相关叙述正确的是
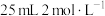 的氯化铁溶液中充分反应(忽略溶液体积的变化),下列相关叙述正确的是
的氯化铁溶液中充分反应(忽略溶液体积的变化),下列相关叙述正确的是A.铁粉完全溶解, 的浓度不变 的浓度不变 |
| B.向溶液中滴加KSCN溶液,溶液变红 |
C.溶液中 和 和 的物质的量之比为5:1 的物质的量之比为5:1 |
| D.氧化产物与还原产物的物质的量之比为2:5 |
您最近一年使用:0次
名校
10 . 硫酸亚铁(俗称绿矾: )主要用于净水,治疗缺铁性贫血,制铁盐、氧化铁颜料、媒染剂、防腐剂、消毒剂等。工业上用某种含铁矿石(主要含Fe、Cu、Al、S元素)制备绿矾的工艺流程如下:
)主要用于净水,治疗缺铁性贫血,制铁盐、氧化铁颜料、媒染剂、防腐剂、消毒剂等。工业上用某种含铁矿石(主要含Fe、Cu、Al、S元素)制备绿矾的工艺流程如下:
(1)“焙烧”前要将含铁矿石粉碎过筛,目的是_______ 。
(2)尾气含有的大气污染成分是_______ ,可用_______ (填物质名称)溶液吸收,写出“碱浸”过程中 溶液参与反应的化学方程式:
溶液参与反应的化学方程式:_______ 。
(3)X试剂为_______ (填化学式),一系列操作名称为隔绝空气_______ 、过滤、洗涤、干燥得到绿矾。
(4)检验绿矾是否变质的试剂是_______ ,实验室可用酸性 溶液测定绿矾的纯度,用高锰酸钾固体配制酸性高锰酸钾溶液时,若定容时俯视刻度线,其他操作均正确,则用此溶液测定的绿矾纯度会偏
溶液测定绿矾的纯度,用高锰酸钾固体配制酸性高锰酸钾溶液时,若定容时俯视刻度线,其他操作均正确,则用此溶液测定的绿矾纯度会偏_______ (填“大”或“小”)。
 )主要用于净水,治疗缺铁性贫血,制铁盐、氧化铁颜料、媒染剂、防腐剂、消毒剂等。工业上用某种含铁矿石(主要含Fe、Cu、Al、S元素)制备绿矾的工艺流程如下:
)主要用于净水,治疗缺铁性贫血,制铁盐、氧化铁颜料、媒染剂、防腐剂、消毒剂等。工业上用某种含铁矿石(主要含Fe、Cu、Al、S元素)制备绿矾的工艺流程如下: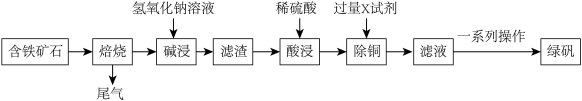
(1)“焙烧”前要将含铁矿石粉碎过筛,目的是
(2)尾气含有的大气污染成分是
 溶液参与反应的化学方程式:
溶液参与反应的化学方程式:(3)X试剂为
(4)检验绿矾是否变质的试剂是
 溶液测定绿矾的纯度,用高锰酸钾固体配制酸性高锰酸钾溶液时,若定容时俯视刻度线,其他操作均正确,则用此溶液测定的绿矾纯度会偏
溶液测定绿矾的纯度,用高锰酸钾固体配制酸性高锰酸钾溶液时,若定容时俯视刻度线,其他操作均正确,则用此溶液测定的绿矾纯度会偏
您最近一年使用:0次
2024-08-14更新
|
82次组卷
|
2卷引用:湖南省益阳市安化县2023-2024学年高一上学期期末考试化学试卷



