名校
解题方法
1 . 用锈蚀了的废铁屑(铁锈主要成分是 )为原料制备
)为原料制备 晶体的流程可简要表示如下:
晶体的流程可简要表示如下:
(1)向“酸溶”“过滤”后的滤液中滴加KSCN溶液无明显现象,“酸溶”过程中发生的主要反应的离子方程式有:① ;②
;②_______ ;③_______ 。
(2)取少量“酸溶”“过滤”后的滤液,向其中滴加NaOH溶液出现白色沉淀,沉淀最终转化为红褐色,写出生成红褐色沉淀的化学方程式_______ 。
(3)“酸溶”时控制温度在40℃左右不宜过高,原因是_______ ,为控制该温度可以采用_______ 进行加热。
(4)“氧化”过程可在如图所示装置中进行。_______
(5)从 溶液制得
溶液制得 晶体的系列操作是蒸发浓缩至有晶膜出现、
晶体的系列操作是蒸发浓缩至有晶膜出现、_______ 、_______ 、洗涤、干燥。
 )为原料制备
)为原料制备 晶体的流程可简要表示如下:
晶体的流程可简要表示如下:
(1)向“酸溶”“过滤”后的滤液中滴加KSCN溶液无明显现象,“酸溶”过程中发生的主要反应的离子方程式有:①
 ;②
;②(2)取少量“酸溶”“过滤”后的滤液,向其中滴加NaOH溶液出现白色沉淀,沉淀最终转化为红褐色,写出生成红褐色沉淀的化学方程式
(3)“酸溶”时控制温度在40℃左右不宜过高,原因是
(4)“氧化”过程可在如图所示装置中进行。

(5)从
 溶液制得
溶液制得 晶体的系列操作是蒸发浓缩至有晶膜出现、
晶体的系列操作是蒸发浓缩至有晶膜出现、
您最近一年使用:0次
2022-12-07更新
|
315次组卷
|
4卷引用:湖南省邵阳市新邵县第三中学2023-2024学年高一上学期12月月考化学试题
名校
2 . 某工业废水中含有大量的Cu2+、Fe3+、Fe2+和 ,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
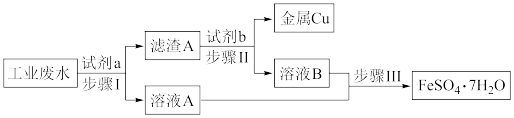
(1)下列叙述正确的是___________。
(2)步骤Ⅰ发生反应的离子方程式为Fe+Cu2+=Fe2++Cu和___________ 。
(3)取2mL溶液A于试管中,滴加少量NaOH溶液,观察到的实验现象是___________ 。
(4)获得的绿矾晶体(FeSO4·7H2O)可能有部分被氧化,请设计检验方案验证(操作、现象、结论)___________ 。
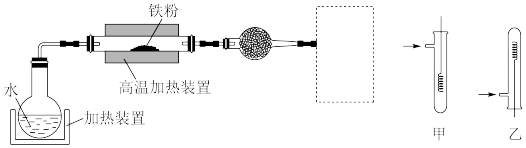
(5)已知:3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是
Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是___________ (填“甲”或“乙”)。
 ,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
(1)下列叙述正确的是___________。
| A.滤渣A为Fe和Cu的混合物 |
| B.试剂b为盐酸 |
| C.步骤Ⅱ可以分离出Cu,并能得到FeSO4溶液 |
| D.步骤Ⅲ为蒸发溶液 |
(3)取2mL溶液A于试管中,滴加少量NaOH溶液,观察到的实验现象是
(4)获得的绿矾晶体(FeSO4·7H2O)可能有部分被氧化,请设计检验方案验证(操作、现象、结论)
(5)已知:3Fe(s)+4H2O(g)
 Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是
Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是
您最近一年使用:0次
2022-02-20更新
|
148次组卷
|
2卷引用:湖南省娄底市第四中学2021-2022学年高一下学期第一次月考化学试题
名校
解题方法
3 . 我国某现代化铜冶炼厂排放的废水中含有较多的 、
、 、
、 、
、 和少量的
和少量的 ,为了减少污染并变废为宝,该铜冶炼厂以该废水为原料制备硫酸钠、硫酸亚铁晶体(
,为了减少污染并变废为宝,该铜冶炼厂以该废水为原料制备硫酸钠、硫酸亚铁晶体( )并回收金属铜,设计了如下流程(流程中加入的试剂均过量)。
)并回收金属铜,设计了如下流程(流程中加入的试剂均过量)。

已知:加入的试剂①为 溶液。回答下列问题:
溶液。回答下列问题:
(1)操作a的名称为_______ ,在实验室进行该操作时需要用到的玻璃仪器有_______ ;溶液A中所含的溶质主要为_______ (填化学式)。
(2)加入的试剂③为_______ (填试剂名称)。
(3)检验溶液D中的金属阳离子的具体操作及现象为_______ ,写出检验过程中属于氧化还原反应的离子方程式并用双线桥法标出电子转移的数目和方向:_______ 。
(4)若取 溶液G加入试管中,然后滴加氢氧化钠溶液,可观察到的现象为
溶液G加入试管中,然后滴加氢氧化钠溶液,可观察到的现象为_______ ,此现象中涉及的氧化还原反应的化学方程式为_______ 。
 、
、 、
、 、
、 和少量的
和少量的 ,为了减少污染并变废为宝,该铜冶炼厂以该废水为原料制备硫酸钠、硫酸亚铁晶体(
,为了减少污染并变废为宝,该铜冶炼厂以该废水为原料制备硫酸钠、硫酸亚铁晶体( )并回收金属铜,设计了如下流程(流程中加入的试剂均过量)。
)并回收金属铜,设计了如下流程(流程中加入的试剂均过量)。
已知:加入的试剂①为
 溶液。回答下列问题:
溶液。回答下列问题:(1)操作a的名称为
(2)加入的试剂③为
(3)检验溶液D中的金属阳离子的具体操作及现象为
(4)若取
 溶液G加入试管中,然后滴加氢氧化钠溶液,可观察到的现象为
溶液G加入试管中,然后滴加氢氧化钠溶液,可观察到的现象为
您最近一年使用:0次
2021-12-19更新
|
258次组卷
|
2卷引用:湖南省部分校2021-2022学年高一上学期12月联考化学试题
名校
4 . 氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2(难溶于稀硫酸)、Al2O3等,用硫酸渣制备铁红(Fe2O3)的过程如图,回答下列问题: 还有
还有___________ (填离子符号),写出Fe2O3与稀硫酸反应的离子方程式:___________ 。
(2)“还原”过程中加入FeS2粉的目的是将溶液中的Fe3+还原为Fe2+,而FeS2自身被氧化为H2SO4,该反应中氧化剂和还原剂的物质的量之比为___________ 。
(3)“滤渣A”是SiO2,SiO2是一种常见的酸性氧化物,与CO2类似,都可与强碱反应,写出SiO2与NaOH溶液反应的化学方程式:___________ 。
(4)“氧化”时,可观察到的实验现象为___________ 。若加入的NaOH溶液过量,则“滤液B”中的溶质除了NaOH外,还含有___________ ;若加入的NaOH溶液不足,则制得的铁红中含有的杂质为___________ (填化学式)。

 还有
还有(2)“还原”过程中加入FeS2粉的目的是将溶液中的Fe3+还原为Fe2+,而FeS2自身被氧化为H2SO4,该反应中氧化剂和还原剂的物质的量之比为
(3)“滤渣A”是SiO2,SiO2是一种常见的酸性氧化物,与CO2类似,都可与强碱反应,写出SiO2与NaOH溶液反应的化学方程式:
(4)“氧化”时,可观察到的实验现象为
您最近一年使用:0次
2022-05-06更新
|
802次组卷
|
15卷引用:湖南省株洲市九方中学2022-2023学年高三上学期第四次月考化学试题
湖南省株洲市九方中学2022-2023学年高三上学期第四次月考化学试题湖南省怀化市沅陵县第一中学2021-2022学年高一下学期期中考试化学试题湖南省长沙市实验中学2021-2022学年高一下学期入学考试化学试题湖南省衡阳市祁东县2021-2022学年高一上学期期末考试化学试题安徽省滁州市定远县育才学校2021-2022学年高一下学期5月月考化学试题湖北省襄阳市第四中学2021-2022学年高一下学期2月考试化学试题湖南省长沙市实验中学2022-2023学年高一上学期期末考试化学试题山西省吕梁市2021-2022学年高一上学期期末考试化学试题河北省秦皇岛市2021-2022学年高一上学期期末统一考试化学试题河北省廊坊市2021-2022学年高一上学期期末统一考试化学试题安徽省宣城中学2021-2022学年高一下学期期中考试化学试题(已下线)第05练 以简单工业流程突破金属及其化合物-2022年【暑假分层作业】高二化学(2023届一轮复习通用)云南省楚雄州2021-2022学年高一上学期期末教育学业质量监测化学试题河北省秦皇岛市青龙满族自治县实验中学2022-2023学年高一上学期期末考试化学试题广东省阳江市江城区部分学校2023-2024学年高一上学期期末联考化学试题
解题方法
5 . 七水合硫酸亚铁( )是一种重要的食品或饲料添加剂、颜料及电子工业的原材料。某同学设计了利用工业烧渣并采用如图流程来制备七水合硫酸亚铁:
)是一种重要的食品或饲料添加剂、颜料及电子工业的原材料。某同学设计了利用工业烧渣并采用如图流程来制备七水合硫酸亚铁:

回答下列问题
(1)工业烧渣与稀硫酸反应的离子反应有: ,②
,②___________ 。
(2)加入的试剂 是:
是:___________ 。
A. B.
B. C.
C. D.
D.
(3)若需检验还原后的 溶液中是否存在有
溶液中是否存在有 ,可选择的方法是取2-3mL试液,在其中滴加
,可选择的方法是取2-3mL试液,在其中滴加___________ 溶液(填化学式),当___________ 时(填实验现象),说明溶液中存在 。
。
(4)利用工业烧渣还可以制得一种重要的净水剂 ,其基本原理是先由烧渣制得氢氧化铁,再将氢氧化铁与
,其基本原理是先由烧渣制得氢氧化铁,再将氢氧化铁与 、烧碱在40℃反应,即可制备
、烧碱在40℃反应,即可制备 ,其中
,其中 被还原成
被还原成 ,此方法称为“湿法”;请写出湿法制备
,此方法称为“湿法”;请写出湿法制备 的化学方程式:
的化学方程式:___________ 。
(5)制备 还有一方法称为“干法”,其反应原理为:
还有一方法称为“干法”,其反应原理为: ;若用
;若用 替代
替代 进行上述反应,当标准状况下产生
进行上述反应,当标准状况下产生 时,则需消耗
时,则需消耗
___________ 
 )是一种重要的食品或饲料添加剂、颜料及电子工业的原材料。某同学设计了利用工业烧渣并采用如图流程来制备七水合硫酸亚铁:
)是一种重要的食品或饲料添加剂、颜料及电子工业的原材料。某同学设计了利用工业烧渣并采用如图流程来制备七水合硫酸亚铁:
回答下列问题
(1)工业烧渣与稀硫酸反应的离子反应有:
 ,②
,②(2)加入的试剂
 是:
是:A.
 B.
B. C.
C. D.
D.
(3)若需检验还原后的
 溶液中是否存在有
溶液中是否存在有 ,可选择的方法是取2-3mL试液,在其中滴加
,可选择的方法是取2-3mL试液,在其中滴加 。
。(4)利用工业烧渣还可以制得一种重要的净水剂
 ,其基本原理是先由烧渣制得氢氧化铁,再将氢氧化铁与
,其基本原理是先由烧渣制得氢氧化铁,再将氢氧化铁与 、烧碱在40℃反应,即可制备
、烧碱在40℃反应,即可制备 ,其中
,其中 被还原成
被还原成 ,此方法称为“湿法”;请写出湿法制备
,此方法称为“湿法”;请写出湿法制备 的化学方程式:
的化学方程式:(5)制备
 还有一方法称为“干法”,其反应原理为:
还有一方法称为“干法”,其反应原理为: ;若用
;若用 替代
替代 进行上述反应,当标准状况下产生
进行上述反应,当标准状况下产生 时,则需消耗
时,则需消耗

您最近一年使用:0次
名校
6 . 炼铁厂的废渣铁矾渣主要含有K2Fe6(SO4)4(OH)12、ZnO Fe2O3及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
Fe2O3及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
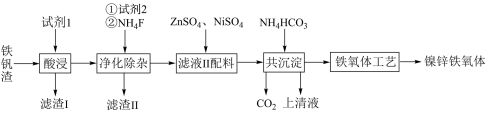
(1)试剂1是过量的______ 。
(2)试剂2为过量的铁粉,加入后可以观察的现象有______________________ 。
(3)NH4F溶液不能放入玻璃器皿中保存,理由是_____________________________ (用离子方程式表示)。已知:25 °C时,Ksp(CaF2)=2.7×10-11、,Ksp(MgF2)=6.4×10-19。加入NH4F溶液沉淀后,c(Mg2+) = 1. 6×10-10mol • L-1,此时Ca2+是否也完全沉淀?写出具体的分析过程:______ (若溶液中某离子浓度小于1.0×10-5mol • L-1时,说明该离子已沉淀完全)。
(4)在Fe2+、Ni2+、Zn2+共沉淀过程中,若以Me代表Fe、Ni、Zn元素,则生成MeCO3•2Me(OH)2•H2O沉淀的化学方程式为________________________________ .
(5)按照上述流程,一座10万吨规模的炼铁厂每年产生铁矾渣约5万吨,Fe3+含量为44.8%,理论上每年至少可制备复合镍锌铁氧体(NiZnFe4O8,M=476 g • mol -1)__________ 万吨。
(6)滤液Ⅱ中加入的ZnSO4溶液,低温烘干后可得到皓矾(ZnSO4• 7H2O) 取28.70 g皓矾加热至不同温度,剩余固体的质量变化如图所示:

①100 °C时所得固体的化学式__________ 。
②680 °C时所得固体的化学式为____
 Fe2O3及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
Fe2O3及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
(1)试剂1是过量的
(2)试剂2为过量的铁粉,加入后可以观察的现象有
(3)NH4F溶液不能放入玻璃器皿中保存,理由是
(4)在Fe2+、Ni2+、Zn2+共沉淀过程中,若以Me代表Fe、Ni、Zn元素,则生成MeCO3•2Me(OH)2•H2O沉淀的化学方程式为
(5)按照上述流程,一座10万吨规模的炼铁厂每年产生铁矾渣约5万吨,Fe3+含量为44.8%,理论上每年至少可制备复合镍锌铁氧体(NiZnFe4O8,M=476 g • mol -1)
(6)滤液Ⅱ中加入的ZnSO4溶液,低温烘干后可得到皓矾(ZnSO4• 7H2O) 取28.70 g皓矾加热至不同温度,剩余固体的质量变化如图所示:

①100 °C时所得固体的化学式
②680 °C时所得固体的化学式为
您最近一年使用:0次
名校
解题方法
7 . 烟道灰中含有 等,分离回收其中的金属资源可有效缓解矿藏资源不足的问题。分离回收时的流程如下:
等,分离回收其中的金属资源可有效缓解矿藏资源不足的问题。分离回收时的流程如下:

已知:
①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀时的pH如下表所示。
② 的化学性质与
的化学性质与 相似。常温下,水溶液中不同形式含锌微粒物质的量浓度的对数(lgc)与pH的关系如图所示。
相似。常温下,水溶液中不同形式含锌微粒物质的量浓度的对数(lgc)与pH的关系如图所示。

回答下列问题:
(1)基态Fe原子、Mn原子核外未成对电子数之比为___________ 。
(2)试剂X可能为___________。
(3)步骤M的目的是___________ ;
(4)步骤M后应调节 的范围为
的范围为___________ ;不同 ,含
,含 微粒在体系中的存在形式不同,依据图a数据,求该温度下
微粒在体系中的存在形式不同,依据图a数据,求该温度下 的
的 为
为___________ 。
(5) 在空气中易被氧化为
在空气中易被氧化为 ,反应的化学方程式为
,反应的化学方程式为___________ 。
(6)某实验室设计了如图b所示装置,通过通入 来制备
来制备 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。石墨电极反应式为
并可分别通过阴、阳膜定向移动。石墨电极反应式为___________ 。

 等,分离回收其中的金属资源可有效缓解矿藏资源不足的问题。分离回收时的流程如下:
等,分离回收其中的金属资源可有效缓解矿藏资源不足的问题。分离回收时的流程如下:
已知:
①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀时的pH如下表所示。
| 金属离子 |  |  |  |
| 开始沉淀的pH | 7.0 | 1.9 | 8.1 |
| 完全沉淀的pH | 9.0 | 3.2 | 10.1 |
 的化学性质与
的化学性质与 相似。常温下,水溶液中不同形式含锌微粒物质的量浓度的对数(lgc)与pH的关系如图所示。
相似。常温下,水溶液中不同形式含锌微粒物质的量浓度的对数(lgc)与pH的关系如图所示。
回答下列问题:
(1)基态Fe原子、Mn原子核外未成对电子数之比为
(2)试剂X可能为___________。
A. 溶液 溶液 | B.氨水 | C. 溶液 溶液 | D.稀 |
(3)步骤M的目的是
(4)步骤M后应调节
 的范围为
的范围为 ,含
,含 微粒在体系中的存在形式不同,依据图a数据,求该温度下
微粒在体系中的存在形式不同,依据图a数据,求该温度下 的
的 为
为(5)
 在空气中易被氧化为
在空气中易被氧化为 ,反应的化学方程式为
,反应的化学方程式为(6)某实验室设计了如图b所示装置,通过通入
 来制备
来制备 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。石墨电极反应式为
并可分别通过阴、阳膜定向移动。石墨电极反应式为
您最近一年使用:0次
名校
解题方法
8 . 以废铁屑、低品位软锰矿[主要成分有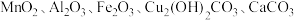 、
、 等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
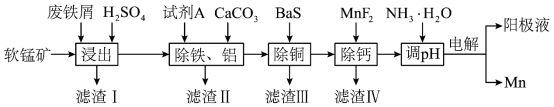
已知:I.部分金属阳离子以氢氧化物沉淀时的 如表:
如表:
Ⅱ.几种化合物的溶解性或溶度积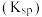 如表:
如表:
(1)基态 的价层电子排布式为
的价层电子排布式为__________ 。
(2)为去除废铁屑表面的油污可采用的方法为__________ ;“浸出”后浸出液中的 价金属阳离子有
价金属阳离子有 、
、__________ 。
(3)锰的浸出率结果如图所示。

由图可知,影响锰浸出率的因素有__________ 。
(4)“除铁、铝”过程中,浸出液需要先用试剂 处理,然后加入
处理,然后加入 ,反应后溶液的
,反应后溶液的 。试剂
。试剂 的作用是
的作用是__________ 。
(5)“除铜”过程中,当铜离子恰好完全沉淀(当离子浓度小于或等于 时视为完全沉淀)时,溶液中
时视为完全沉淀)时,溶液中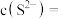
__________  。
。
(6)用惰性电极电解中性 溶液可以制得金属
溶液可以制得金属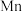 。装置如图所示。
。装置如图所示。
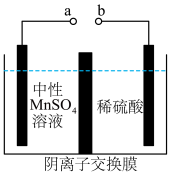
若生成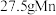 ,右室溶液中最终
,右室溶液中最终 的变化为
的变化为__________ (填“增加”或“减少”) 。
。
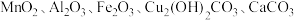 、
、 等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
已知:I.部分金属阳离子以氢氧化物沉淀时的
 如表:
如表:| 金属阳离子 |  |  |  |  |  |
开始沉淀的 | 6.8 | 1.8 | 3.7 | 8.6 | 5.2 |
沉淀完全的 | 8.3 | 2.8 | 4.7 | 10.1 | 6.7 |
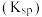 如表:
如表:| 化合物 |  |  |  |  |  |
溶解性或溶度积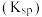 | 溶于水 | 溶于水 | 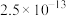 |  |  |
(1)基态
 的价层电子排布式为
的价层电子排布式为(2)为去除废铁屑表面的油污可采用的方法为
 价金属阳离子有
价金属阳离子有 、
、(3)锰的浸出率结果如图所示。

由图可知,影响锰浸出率的因素有
(4)“除铁、铝”过程中,浸出液需要先用试剂
 处理,然后加入
处理,然后加入 ,反应后溶液的
,反应后溶液的 。试剂
。试剂 的作用是
的作用是(5)“除铜”过程中,当铜离子恰好完全沉淀(当离子浓度小于或等于
 时视为完全沉淀)时,溶液中
时视为完全沉淀)时,溶液中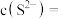
 。
。(6)用惰性电极电解中性
 溶液可以制得金属
溶液可以制得金属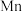 。装置如图所示。
。装置如图所示。
若生成
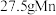 ,右室溶液中最终
,右室溶液中最终 的变化为
的变化为 。
。
您最近一年使用:0次
9 . 工业上以铬铁矿(FeCr2O4,含Al、Si氧化物等杂质)为主要原料制备红矾钠(Na2Cr2O7•2H2O)的工艺流程如图。回答下列问题:___ ;冷却结晶所得母液中,除Na2Cr2O7外,可在上述流程中循环利用的物质还有____ 。
(4)利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7的总反应方程式为:4Na2CrO4+4H2O 2Na2Cr2O7+4NaOH+2H2↑+O2↑。则Na2Cr2O7在
2Na2Cr2O7+4NaOH+2H2↑+O2↑。则Na2Cr2O7在___ (填“阴”或“阳”)极室制得,电解时通过膜的离子主要为___ 。

(1)焙烧的目的是将FeCr2O4转化为Na2CrO4并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
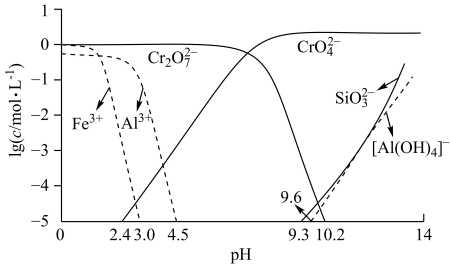
中和时pH的理论范围为
(4)利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7的总反应方程式为:4Na2CrO4+4H2O
 2Na2Cr2O7+4NaOH+2H2↑+O2↑。则Na2Cr2O7在
2Na2Cr2O7+4NaOH+2H2↑+O2↑。则Na2Cr2O7在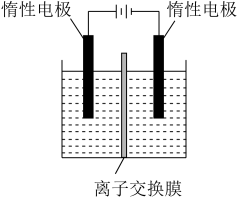
您最近一年使用:0次
2021-06-29更新
|
14322次组卷
|
22卷引用:湖南省邵阳市邵东市创新高级中学2023-2024学年高三上学期第四次月考化学试题
湖南省邵阳市邵东市创新高级中学2023-2024学年高三上学期第四次月考化学试题江苏省华罗庚中学2023-2024学年高三上学期12月阶段检测化学试卷2021年新高考山东化学高考真题(已下线)微专题32 化学工艺流程题——核心反应与条件控制-备战2022年高考化学考点微专题(已下线)专题16 工艺流程综合题-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)专题讲座(六)化工流程的解题策略(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)2021年山东高考化学试题变式题11-20(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题27 无机化工流程-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)押新高考卷14题 工艺流程综合题-备战2022年高考化学临考题号押题(新高考通版)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)微专题17 热点金属及其化合物制备流程(V、Cr、Mn、Co、Ni)-备战2023年高考化学一轮复习考点微专题(已下线)微专题25 化学工艺流程题-----原料的预处理-备战2023年高考化学一轮复习考点微专题(已下线)微专题27 化学工艺流程题-----物质的分离与提纯-备战2023年高考化学一轮复习考点微专题山东省济宁市邹城市孟子湖中学2021-2022学年高三下学期开学考试化学试题第二部分 热点专项突破——解题能力稳提升 专项3 结合理论的综合类工艺流程(已下线)题型39 其他过渡金属及其化合物的转化流程(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
10 . 工业上以黄铜矿(主要成分CuFeS2)为原料制备CuS04.5H2O的主要流程如下:

(1)下列装置不能用于吸收气体X的是___________ 。(填代号)。

(2)熔渣Y的成分为Fe203和Fe0,选用提供的试剂,设计实验验证熔渣中含有FeO。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMn04溶液、NaOH溶液、氯水。
①从上述提供的试剂中选择实验验证所需药品____________________ 。
②写出验证过程中所发生的氧化还原反应的离子方程式____________________ 。
(3)向粗铜中加入硫酸和硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中HNO3与H2S04的最佳物质的量之比为__________ 。

(1)下列装置不能用于吸收气体X的是

(2)熔渣Y的成分为Fe203和Fe0,选用提供的试剂,设计实验验证熔渣中含有FeO。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMn04溶液、NaOH溶液、氯水。
①从上述提供的试剂中选择实验验证所需药品
②写出验证过程中所发生的氧化还原反应的离子方程式
(3)向粗铜中加入硫酸和硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中HNO3与H2S04的最佳物质的量之比为
您最近一年使用:0次



