解题方法
1 . 回答下列问题。
(1)氢氧化亚铁与氧气、水的反应方程式为:___________ 。
(2)钠通常保存在___________ 中,加热时,钠可以在空气中燃烧发出___________ 火焰,生成___________ 色固体。
(3)写出氯气和水反应的化学方程式:___________ 。
(4)电离:电解质溶于水或受热熔化时,形成___________ 的过程。
(5) 、
、 、
、 、
、 、
、 、
、 中,
中,___________ 和___________ 互为同位素,___________ 和___________ 的中子数相等,但质子数不等,所以不是同一种元素。
(6)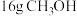 的物质的量是
的物质的量是___________ ,含H原子的数目为___________ 。
(1)氢氧化亚铁与氧气、水的反应方程式为:
(2)钠通常保存在
(3)写出氯气和水反应的化学方程式:
(4)电离:电解质溶于水或受热熔化时,形成
(5)
 、
、 、
、 、
、 、
、 、
、 中,
中,(6)
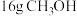 的物质的量是
的物质的量是
您最近一年使用:0次
名校
2 . 已知A常温常压下为无色液体,A为气体时与R反应生成B和E,M、R是两种常见的金属,M是地壳中含量最多的金属元素的单质,T是淡黄色固体,B. C是无色无味的气体,E是具有磁性的黑色晶体,H是红褐色固体。
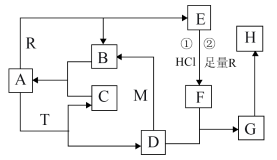
(1)物质T的化学式为___________ 。15.6g T与足量的A反应电子转移数为___________ 个(已知:阿伏伽德罗常数为NA)。
(2)D和M在溶液中反应生成B的离子反应方程式为___________ 。
(3)G在潮湿空气中转化为H的化学方程式为___________ 。
(4)T和F反应只生成C、H和一种盐,其离子反应方程式为_________ 。
(5)若向E和R的混合物中加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,放出448mL(标准状况)气体,向所得溶液中加入KSCN溶液,无血红色出现。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为___________ g。

(1)物质T的化学式为
(2)D和M在溶液中反应生成B的离子反应方程式为
(3)G在潮湿空气中转化为H的化学方程式为
(4)T和F反应只生成C、H和一种盐,其离子反应方程式为
(5)若向E和R的混合物中加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,放出448mL(标准状况)气体,向所得溶液中加入KSCN溶液,无血红色出现。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为
您最近一年使用:0次
2023-12-15更新
|
411次组卷
|
2卷引用:新疆乌鲁木齐八一中学2023-2024学年高一上学期1月月考化学试卷
解题方法
3 . I.Na2CO3和NaHCO3是厨房中常见的两种盐。回答下列问题:
(1)与酸反应的差异进行鉴别。甲组进行了如图4组实验。
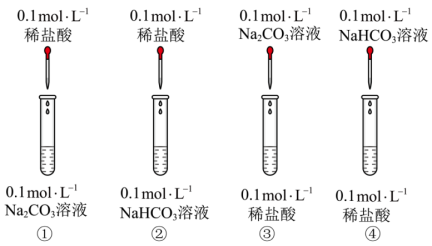
其中实验___________ 和___________ (填实验序号)可以鉴别Na2CO3和NaHCO3。
(2)利用如图实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为___________ 。
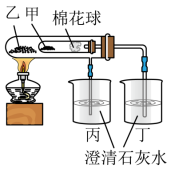
取某碳酸钠和碳酸氢钠混合物2.74g,加热到质量不再变化时,剩余固体的质量为2.12g,则混合物中碳酸钠的质量为___________ 克。
Ⅱ.如图所示,此装置可用来制备Fe(OH)2并验证其还原性,填写下列空白:
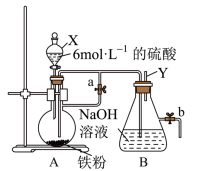
(3)制备Fe(OH)2:
仪器X的名称为___________ ,实验开始时先将止水夹“a”打开,滴入H2SO4和铁粉反应。一段时间后关闭止水夹a,使A中溶液流入B中进行反应。
(4)验证Fe(OH)2还原性:
实验完毕,打开b处止水夹,充入一部分空气,此时B瓶中发生的反应为(写化学方程式)________ ,现象:___________ 。
(5)某同学欲用36.5%浓盐酸(密度1.2g/mL)配制480mL上述实验所需盐酸。
配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果___________ (填写“偏大”、“偏小”、“不变”)。
(1)与酸反应的差异进行鉴别。甲组进行了如图4组实验。

其中实验
(2)利用如图实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为

取某碳酸钠和碳酸氢钠混合物2.74g,加热到质量不再变化时,剩余固体的质量为2.12g,则混合物中碳酸钠的质量为
Ⅱ.如图所示,此装置可用来制备Fe(OH)2并验证其还原性,填写下列空白:

(3)制备Fe(OH)2:
仪器X的名称为
(4)验证Fe(OH)2还原性:
实验完毕,打开b处止水夹,充入一部分空气,此时B瓶中发生的反应为(写化学方程式)
(5)某同学欲用36.5%浓盐酸(密度1.2g/mL)配制480mL上述实验所需盐酸。
配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果
您最近一年使用:0次
名校
解题方法
4 . 下列实验现象与氧化还原反应无关 的是
| A.过氧化钠放置于空气中逐渐变白 |
B.将生石灰投入 溶液中,产生白色沉淀 溶液中,产生白色沉淀 |
C. 通入硝酸酸化的 通入硝酸酸化的 溶液中,产生白色沉淀 溶液中,产生白色沉淀 |
D.将 溶液滴入 溶液滴入 溶液中,产生白色沉淀,最终变为红褐色 溶液中,产生白色沉淀,最终变为红褐色 |
您最近一年使用:0次
2023-04-27更新
|
203次组卷
|
3卷引用:新疆实验中学2023-2024学年高一上学期第二次月考化学试题
名校
解题方法
5 . 下列有关铁和铁的化合物的叙述中,正确的是
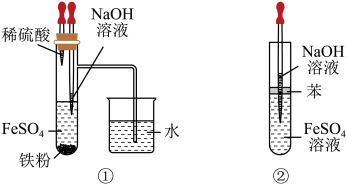
| A.铁的化学性质比较活泼,它能与许多物质发生化学反应,因此铁在自然界中只能以化合态存在 |
| B.Fe3O4是一种红棕色粉末,俗称铁红,常用作油漆、涂料、油墨和橡胶的红色颜料 |
| C.Fe(OH)2在空气中容易被氧化,如图①②都能较长时间看到Fe(OH)2白色沉淀 |
| D.往某溶液中先加入氯水,再加入KSCN溶液,发现溶液变成红色,证明原溶液中含有Fe3+ |
您最近一年使用:0次
2023-04-06更新
|
378次组卷
|
4卷引用:新疆乌鲁木齐市第四中学2022-2023学年高一下学期期中阶段诊断测试化学试题
新疆乌鲁木齐市第四中学2022-2023学年高一下学期期中阶段诊断测试化学试题云南省玉溪第一中学2022-2023学年高一上学期第一月考化学试题 (已下线)第14讲 铁的氢氧化物和铁盐、亚铁盐-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)(已下线)第13讲 铁的氧化物和铁的氢氧化物-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)
解题方法
6 . 已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M。
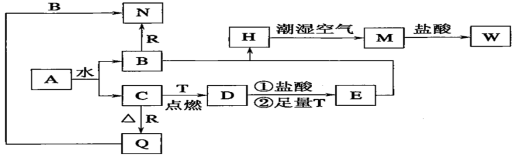
(1)写出下列物质的化学式:A:_______ ,D:_______ ,R:_______ 。
(2)按要求写下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:_______ ;
②B和R反应生成N的离子方程式:_______ ;
③D与盐酸反应的离子方程式:_______ 。

(1)写出下列物质的化学式:A:
(2)按要求写下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:
②B和R反应生成N的离子方程式:
③D与盐酸反应的离子方程式:
您最近一年使用:0次
7 . 已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。
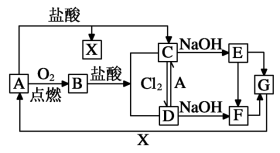
(1)写出X、B、D、F的化学式:X_____ 、B_____ 、D____ 、E_____ 、 G_____ 。
(2)写出A与水反应的化学方程式_____ 。
(3)检验D中阳离子的操作方法__________________________ 。
(4)①写出下列转化的离子方程式D→C:_____ 。
②E转化为F时的现象_____________ ,当有1molF生成时转移电子数为____ 。

(1)写出X、B、D、F的化学式:X
(2)写出A与水反应的化学方程式
(3)检验D中阳离子的操作方法
(4)①写出下列转化的离子方程式D→C:
②E转化为F时的现象
您最近一年使用:0次
8 . 食盐是日常生活的必需品,也是重要的化工原料。
I.海水中含有大量的NaCl,以及少量的 、
、 、
、 等离子。
等离子。
(1)①为得到纯净的饱和NaCl溶液,进行了如下操作,请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中加入过量氢氧化钡溶液,过滤;
c.向滤液中加入过量_______ 溶液,过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
②步骤b中反应的离子方程式是_______ 。
(2)加入足量的稀盐酸的目的是:_______ 。
II.某透明溶液中可能大量存在 、
、 、
、 、
、 、
、 中的几种离子。
中的几种离子。
(3)取少量原溶液,向其中加入过量NaOH溶液,有白色沉淀生成,迅速变为灰绿色,最后变成红褐色,说明原溶液中肯定存在的离子是_______ ,有关反应的离子方程式为_______ 、_______ 。
(4)检验原溶液中是否存在 的实验方法是
的实验方法是_______ 。
I.海水中含有大量的NaCl,以及少量的
 、
、 、
、 等离子。
等离子。(1)①为得到纯净的饱和NaCl溶液,进行了如下操作,请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中加入过量氢氧化钡溶液,过滤;
c.向滤液中加入过量
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
②步骤b中反应的离子方程式是
(2)加入足量的稀盐酸的目的是:
II.某透明溶液中可能大量存在
 、
、 、
、 、
、 、
、 中的几种离子。
中的几种离子。(3)取少量原溶液,向其中加入过量NaOH溶液,有白色沉淀生成,迅速变为灰绿色,最后变成红褐色,说明原溶液中肯定存在的离子是
(4)检验原溶液中是否存在
 的实验方法是
的实验方法是
您最近一年使用:0次
9 . 部分物质间的转化关系如下图所示(部分物质已省略。已知A→B是实验室制取黄绿色气体的主要方法之一,H的焰色呈黄色,请完成下列填空。
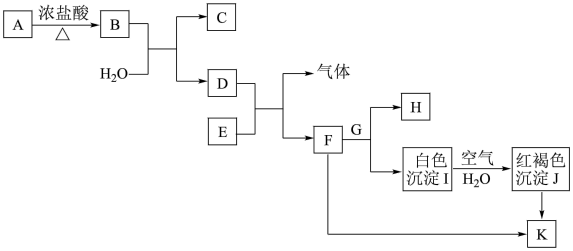
(1)检验F溶液中阳离子的试剂是_______ 。若Cu2+中含有F中阳离子的杂质,应加入_______ (填化学式)除杂。
(2)Ⅰ转化为J的化学方程式为_______ 。
(3)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_______(填字母序号)。
(4)当前,新冠病毒变异毒株奥密克戎来势汹汹,化学消毒剂在疫情防控中起着重要作用。
①目前,很多自来水厂用黄绿色气体来杀菌、消毒。A→B的离子反应方程式为_______ 。
②C可以杀菌、消毒,但不稳定,难以保存,原因是_______ (用化学方程式表示)。
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,写出相关离子方程式_______ 。
④ClO2为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(NaClO2)固体与B反应可得到ClO2和NaCl,该反应中,氧化剂与还原剂的物质的量之比为_______ 。

(1)检验F溶液中阳离子的试剂是
(2)Ⅰ转化为J的化学方程式为
(3)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_______(填字母序号)。
| A.胶体L具有丁达尔效应 | B.胶体L的分散质粒子直径为 |
| C.胶体L是均一的分散系 | D.胶体L比K的饱和溶液颜色深 |
①目前,很多自来水厂用黄绿色气体来杀菌、消毒。A→B的离子反应方程式为
②C可以杀菌、消毒,但不稳定,难以保存,原因是
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,写出相关离子方程式
④ClO2为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(NaClO2)固体与B反应可得到ClO2和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
10 . 用如图装置可以制备 沉淀,下列说法不正确的是
沉淀,下列说法不正确的是
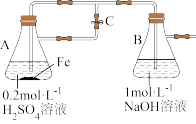
 沉淀,下列说法不正确的是
沉淀,下列说法不正确的是
| A.该实验应该先打开C,一段时间后再关闭C |
| B.实验完成时,在A容器中得到白色沉淀 |
C.如果将NaOH溶液直接滴入 溶液中,最终得到红褐色沉淀 溶液中,最终得到红褐色沉淀 |
| D.本实验制备的氢氧化亚铁可以相对较长时间保持白色状态 |
您最近一年使用:0次
2022-07-15更新
|
826次组卷
|
5卷引用:新疆实验中学2023-2024学年高一上学期第二次月考化学试题
新疆实验中学2023-2024学年高一上学期第二次月考化学试题河北省邯郸市2021-2022学年高一下学期期末考试化学试题(已下线)第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)(已下线)第13讲 铁的氧化物和铁的氢氧化物-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)湖南省永州市蓝山县第二中学2023-2024学年高一上学期第三次月考化学试卷



