1 . 已知甲、乙、丙物质分别由H、C、Na、O、Cl、Fe元素中的一种或几种组成。
(1)若甲物质俗称为小苏打,则甲的化学式为_______ 。
(2)若乙物质在空气中迅速变成灰绿色,最后变成红褐色,,则该反应的化学方程式为_______ 。
(3)若丙物质在常温常压下为黄绿色气体,则实验室制取丙的化学方程式为:_______ 。
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂( )。
)。 的一种制备方法如下。
的一种制备方法如下。

① 中,铁元素的化合价为
中,铁元素的化合价为_______ 价。
②将反应Ⅰ的离子方程式配平:_______ 。
_______ _______
_______ _______
_______ _______
_______ _______
_______
(1)若甲物质俗称为小苏打,则甲的化学式为
(2)若乙物质在空气中迅速变成灰绿色,最后变成红褐色,,则该反应的化学方程式为
(3)若丙物质在常温常压下为黄绿色气体,则实验室制取丙的化学方程式为:
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(
 )。
)。 的一种制备方法如下。
的一种制备方法如下。
①
 中,铁元素的化合价为
中,铁元素的化合价为②将反应Ⅰ的离子方程式配平:
_______
 _______
_______ _______
_______ _______
_______ _______
_______
您最近一年使用:0次
21-22高一·全国·课后作业
解题方法
2 . 制备Fe(OH)2的实验探究
(1)向新制的FeSO4溶液中滴加NaOH溶液。实验现象是_______ 。解释产生该现象的原因_______ ,Fe(OH)2转化为Fe(OH)3的化学方程式为_______ 。
(2)用长胶头滴管吸取几滴经煮沸并冷却的的NaOH溶液,将胶头滴管末端伸入FeSO4溶液液面下,慢慢挤出NaOH溶液。实验现象是:_______ 。
(1)向新制的FeSO4溶液中滴加NaOH溶液。实验现象是
(2)用长胶头滴管吸取几滴经煮沸并冷却的的NaOH溶液,将胶头滴管末端伸入FeSO4溶液液面下,慢慢挤出NaOH溶液。实验现象是:
您最近一年使用:0次
21-22高一·全国·课后作业
解题方法
3 . 制备Fe(OH)2的反应中需要控制的条件
(1)Fe(OH)2的性质
Fe(OH)2很不稳定,容易被_______ 氧化。
(2)制备Fe(OH)2反应中条件的控制
①反应的原料必须是_______ 、不含_______ 的亚铁盐溶液与不含_______ 的NaOH溶液。
②反应过程中防止反应混合物与_______ 或_______ 接触。
(1)Fe(OH)2的性质
Fe(OH)2很不稳定,容易被
(2)制备Fe(OH)2反应中条件的控制
①反应的原料必须是
②反应过程中防止反应混合物与
您最近一年使用:0次
解题方法
4 . 完成下列方程式
(1)Na2O2+CO2_______
(2)Na2O2+H2O_______
(3)Fe+H2O(高温)_______
(4)Na+H2O_______
(5)NaOH和过量的二氧化碳_______
(6)氯化铁溶液中通入硫化氢气体_______
(7)氢氧化亚铁和氧气和水反应生成氢氧化铁_______
(8)饱和食盐水中通入氨气和二氧化碳(工业制碱法)_______
(1)Na2O2+CO2
(2)Na2O2+H2O
(3)Fe+H2O(高温)
(4)Na+H2O
(5)NaOH和过量的二氧化碳
(6)氯化铁溶液中通入硫化氢气体
(7)氢氧化亚铁和氧气和水反应生成氢氧化铁
(8)饱和食盐水中通入氨气和二氧化碳(工业制碱法)
您最近一年使用:0次
2022-05-08更新
|
228次组卷
|
2卷引用:上海市奉贤区曙光中学2021-2022学年高一下学期期中检测化学试题
名校
5 . 含氮化合物在工农业生产中有重要应用。
(1)向培养皿中NaOH固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_______ ,检验白烟溶于水后溶液中所含阳离子的操作和现象是_______ 。 液滴中先出现灰绿色沉淀,过一段时间后变成培养皿红褐色,发生的反应有
液滴中先出现灰绿色沉淀,过一段时间后变成培养皿红褐色,发生的反应有 和
和_______ 。

(2)一种新型催化剂能使NO和CO发生反应: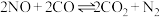 ,某同学设计了三组实验,部分实验条件已经填在下表中。已知增大催化剂的比表面积可提高该反应速率。
,某同学设计了三组实验,部分实验条件已经填在下表中。已知增大催化剂的比表面积可提高该反应速率。
①请将表中数据补充完整:A_______ ;B_______ 。
②能验证温度对化学反应速率影响规律的实验是_______ (填实验编号)。
(1)向培养皿中NaOH固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
 液滴中先出现灰绿色沉淀,过一段时间后变成培养皿红褐色,发生的反应有
液滴中先出现灰绿色沉淀,过一段时间后变成培养皿红褐色,发生的反应有 和
和
(2)一种新型催化剂能使NO和CO发生反应:
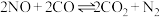 ,某同学设计了三组实验,部分实验条件已经填在下表中。已知增大催化剂的比表面积可提高该反应速率。
,某同学设计了三组实验,部分实验条件已经填在下表中。已知增大催化剂的比表面积可提高该反应速率。| 实验 编号 | t(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| I | 280 |  |  | 82 |
| II | 280 |  | B | 124 |
| III | 350 | A |  | 82 |
②能验证温度对化学反应速率影响规律的实验是
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题:
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的化学方程式为____ ,反应后得到的溶液呈____ 色。用此溶液进行以下实验:
(2)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为_____ 。
(3)另取少量原溶液于试管中,滴入KSCN溶液,则溶液呈____ 色,离子方程式为____ 。
(4)另取少量原溶液于试管中加入足量的铁粉,溶液变为浅绿色,取浅绿色溶液于试管中,加入NaOH溶液得到白色沉淀,露置在空气中所观察到的现象为____ ,产生该现象的化学方程式为____ 。
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的化学方程式为
(2)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为
(3)另取少量原溶液于试管中,滴入KSCN溶液,则溶液呈
(4)另取少量原溶液于试管中加入足量的铁粉,溶液变为浅绿色,取浅绿色溶液于试管中,加入NaOH溶液得到白色沉淀,露置在空气中所观察到的现象为
您最近一年使用:0次
名校
7 . 回答下列问题
(1)以下物质中属于电解质的是(填序号):_______
A.硝酸钾固体B.纯醋酸C.胆矾(CuSO4∙5H2O)晶体D.熔融的BaCl2E.乙醇F.蔗糖G.氯气H.干冰I.铝J.漂白粉固体K.硫酸钾溶液L.氨水
(2)①向磁性的黑色金属氧化物中加入盐酸,写出发生的离子反应方程式:_______ ;再滴入几滴硫氰化钾溶液,溶液变红原因(用反应方程式表示)_______
②已知在坩埚中灼烧Fe(OH)3最后得到Fe2O3,写出灼烧Fe(OH)2最后得到的固体物质化学式:_______
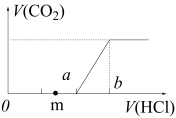
③向含等物质的量的Na2CO3和NaOH混合溶液中逐滴加入盐酸,加入盐酸体积和生成的气体关系如图,写出m点处发生的化学反应方程式_______
(3)对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有SO 、Na+、CO
、Na+、CO 、H+、NO
、H+、NO 、HCO
、HCO 、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2mL该溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。请回答下列问题:
原溶液中一定存在的离子是_______ 一定不存在的离子是_______ 。
(1)以下物质中属于电解质的是(填序号):
A.硝酸钾固体B.纯醋酸C.胆矾(CuSO4∙5H2O)晶体D.熔融的BaCl2E.乙醇F.蔗糖G.氯气H.干冰I.铝J.漂白粉固体K.硫酸钾溶液L.氨水
(2)①向磁性的黑色金属氧化物中加入盐酸,写出发生的离子反应方程式:
②已知在坩埚中灼烧Fe(OH)3最后得到Fe2O3,写出灼烧Fe(OH)2最后得到的固体物质化学式:
③向含等物质的量的Na2CO3和NaOH混合溶液中逐滴加入盐酸,加入盐酸体积和生成的气体关系如图,写出m点处发生的化学反应方程式

(3)对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有SO
 、Na+、CO
、Na+、CO 、H+、NO
、H+、NO 、HCO
、HCO 、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。①用石蕊试液检测该溶液时,溶液显红色。
②取2mL该溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。请回答下列问题:
原溶液中一定存在的离子是
您最近一年使用:0次
解题方法
8 . 回答下列问题:
(1)下列物质中不属于铁合金的是___________(填选项序号)。
(2)铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉淀至质量不再发生变化为止,得到红棕色残渣。”上述沉淀和残渣分别是___________ 、___________ 。
(3)将Na、 、
、 、
、 分别投入盛有足量盐酸的四支试管中,不产生气体的是
分别投入盛有足量盐酸的四支试管中,不产生气体的是___________ (填化学式)。
(4)HClO的结构式为___________ 。
(5)已知质量数为A的某阳离子Rn+,核外有X个电子,则核内中子数为___________ 。
(1)下列物质中不属于铁合金的是___________(填选项序号)。
| A.不锈钢 | B.生铁 | C.碳素钢 | D.氧化铁 |
(3)将Na、
 、
、 、
、 分别投入盛有足量盐酸的四支试管中,不产生气体的是
分别投入盛有足量盐酸的四支试管中,不产生气体的是(4)HClO的结构式为
(5)已知质量数为A的某阳离子Rn+,核外有X个电子,则核内中子数为
您最近一年使用:0次
名校
9 . 铁及其化合物的转化关系如下图所示(图中 、
、 、
、 各代表一种物质)。回答下列问题:
各代表一种物质)。回答下列问题:

(1) 与物质
与物质 反应的化学方程式为
反应的化学方程式为___________ 。
(2) 溶液与铁粉反应的离子方程式为
溶液与铁粉反应的离子方程式为___________ 。
(3) 溶液→Fe(OH)3浊液的过程中,观察到的实验现象是
溶液→Fe(OH)3浊液的过程中,观察到的实验现象是___________ ,此过程中发生反应的化学方程式为___________ 。
 、
、 、
、 各代表一种物质)。回答下列问题:
各代表一种物质)。回答下列问题:
(1)
 与物质
与物质 反应的化学方程式为
反应的化学方程式为(2)
 溶液与铁粉反应的离子方程式为
溶液与铁粉反应的离子方程式为(3)
 溶液→Fe(OH)3浊液的过程中,观察到的实验现象是
溶液→Fe(OH)3浊液的过程中,观察到的实验现象是
您最近一年使用:0次
解题方法
10 . 物质分类与转化是学习化学的重要方法,如图为铁及其化合物的“价一类”二维图,请回答:
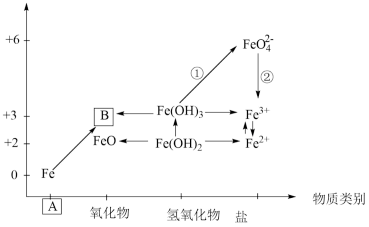
(1)填写二维图中缺失的类别A___________ 和化学式B___________ ,物质B的颜色为___________ 。
(2)利用下述反应可实现转化①:2Fe(OH)3+3ClO-+4OH-=2 +3Cl-+5H2O,用单线桥法标注电子转移情况
+3Cl-+5H2O,用单线桥法标注电子转移情况___________ ,并指明氧化剂:___________ (填化学式) 。
(3)结合二维图中信息推测在转化②中 表现的性质为
表现的性质为_______ (填“还原性”或“氧化性”)
(4)向FeCl2溶液试管底部加入NaOH溶液,放置一段时间后。观察到的实验现象为_______ 。

(1)填写二维图中缺失的类别A
(2)利用下述反应可实现转化①:2Fe(OH)3+3ClO-+4OH-=2
 +3Cl-+5H2O,用单线桥法标注电子转移情况
+3Cl-+5H2O,用单线桥法标注电子转移情况(3)结合二维图中信息推测在转化②中
 表现的性质为
表现的性质为(4)向FeCl2溶液试管底部加入NaOH溶液,放置一段时间后。观察到的实验现象为
您最近一年使用:0次



