1 . 健康人体内含铁元素大约 ,人体内铁元素以
,人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:_______ ,试剂2的化学式为_______ 。
(2)加入新制氯水,溶液中发生的氧化还原反应的离子方程式是_______ 。
(3)加入试剂2时溶液为淡红色,说明“速力菲”中的 已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_______ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:_______ ,现象为_______ 。
 ,人体内铁元素以
,人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验: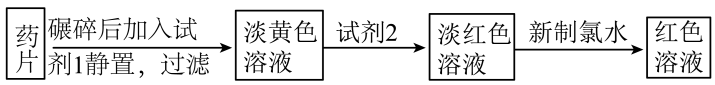
(2)加入新制氯水,溶液中发生的氧化还原反应的离子方程式是
(3)加入试剂2时溶液为淡红色,说明“速力菲”中的
 已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:
您最近半年使用:0次
2 . 铁及其化合物在生产、生活中有着广泛的应用。
(1)刻制铜印刷电路板时,要用FeCl3溶液作为“腐蚀液”,发生反应的离子方程式为_______ ,为了将反应后溶液中的Cu2+回收利用,并得到含有一种溶质的溶液,进行的具体操作是_______ 。
(2)高温时16.8g铁与足量水蒸气反应,生成气体的体积是_______ L(标准状况下)。
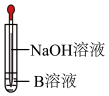
(3)如图,在胶头滴管挤出NaOH溶液的瞬间可观察到生成白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色,请写出上述现象中白色沉淀转化成红褐色沉淀的化学方程式_______ 。_______ 。
②酸浸时,Fe3O4与硫酸反应的化学方程式为_______ ;通入O2的目的是_______ 。
③滤渣的成分是_______ (填化学式)。
④“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+,再用酸性K2Cr2O7标准溶液测定Fe2+的量( 被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是
被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是_______ 。
(1)刻制铜印刷电路板时,要用FeCl3溶液作为“腐蚀液”,发生反应的离子方程式为
(2)高温时16.8g铁与足量水蒸气反应,生成气体的体积是
(3)如图,在胶头滴管挤出NaOH溶液的瞬间可观察到生成白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色,请写出上述现象中白色沉淀转化成红褐色沉淀的化学方程式
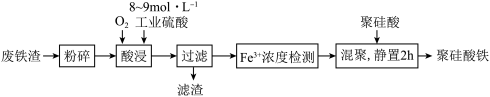
②酸浸时,Fe3O4与硫酸反应的化学方程式为
③滤渣的成分是
④“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+,再用酸性K2Cr2O7标准溶液测定Fe2+的量(
 被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是
被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是
您最近半年使用:0次
名校
解题方法
3 . 采用氧化沉淀法可以利用绿矾制取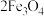 ,其制取流程如图所示:
,其制取流程如图所示:___________ (填写化学式),由溶液 获得该副产品的操作是:蒸发浓缩→
获得该副产品的操作是:蒸发浓缩→___________ →过滤洗涤 晶体加热至完全失去结晶水。
晶体加热至完全失去结晶水。
(2)某兴趣小组模仿如图流程制取 ,在实验前要测定绿矾的含量:称取
,在实验前要测定绿矾的含量:称取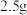 工业绿矾,配制成
工业绿矾,配制成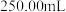 溶液。量取
溶液。量取 溶液于锥形瓶中,用
溶液于锥形瓶中,用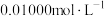 酸性
酸性 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的平均体积为
溶液的平均体积为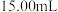 。(滴定时发生反应的离子方程式为
。(滴定时发生反应的离子方程式为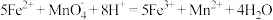 )则绿矾的质量分数为
)则绿矾的质量分数为___________ (计算结果保留三位小数)。
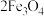 ,其制取流程如图所示:
,其制取流程如图所示:
 获得该副产品的操作是:蒸发浓缩→
获得该副产品的操作是:蒸发浓缩→ 晶体加热至完全失去结晶水。
晶体加热至完全失去结晶水。(2)某兴趣小组模仿如图流程制取
 ,在实验前要测定绿矾的含量:称取
,在实验前要测定绿矾的含量:称取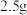 工业绿矾,配制成
工业绿矾,配制成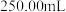 溶液。量取
溶液。量取 溶液于锥形瓶中,用
溶液于锥形瓶中,用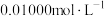 酸性
酸性 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的平均体积为
溶液的平均体积为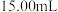 。(滴定时发生反应的离子方程式为
。(滴定时发生反应的离子方程式为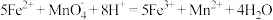 )则绿矾的质量分数为
)则绿矾的质量分数为
您最近半年使用:0次
解题方法
4 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。日常生活中可通过食物摄入铁元素,例如黑木耳中就含有比较丰富的铁元素。某研究性学习小组为测定某地黑木耳中铁的含量,开展了如下研究与实践活动。
【研究与实践活动一】
研究黑木耳中含铁物质的水溶性:称取 黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
【研究与实践活动二】
研究黑木耳中铁的含量:称取 黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。
黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。
(1)浸泡液中未能检测到铁元素,说明黑木耳中的含铁物质___________ (填“难”或“易”)溶于水。
(2)取少量滤液于试管中,滴入 溶液,溶液变红。则滤液中铁元素的存在形式有
溶液,溶液变红。则滤液中铁元素的存在形式有 、
、___________ (填离子符号)。
(3)滤液与Fe生成A的离子方程式为___________ 。
(4)由A转化为B可加入的试剂X可以是___________ (填标号)。
a.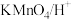 b.
b. c.
c.
(5)由C转化成D的现象:白色沉淀迅速变为灰绿色,最终变为___________ 。C转化成D的化学方程式为___________ 。
(6)将 黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到
黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到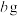 红棕色固体。若流程中加入的铁反应掉
红棕色固体。若流程中加入的铁反应掉 ,则该黑木耳中铁元素的质量分数为
,则该黑木耳中铁元素的质量分数为___________ (用含a、b、c的代数式表示)。
【研究与实践活动一】
研究黑木耳中含铁物质的水溶性:称取
 黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。【研究与实践活动二】
研究黑木耳中铁的含量:称取
 黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。
黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。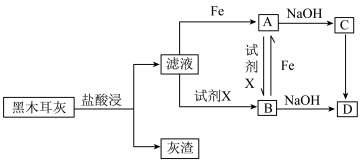
(1)浸泡液中未能检测到铁元素,说明黑木耳中的含铁物质
(2)取少量滤液于试管中,滴入
 溶液,溶液变红。则滤液中铁元素的存在形式有
溶液,溶液变红。则滤液中铁元素的存在形式有 、
、(3)滤液与Fe生成A的离子方程式为
(4)由A转化为B可加入的试剂X可以是
a.
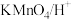 b.
b. c.
c.
(5)由C转化成D的现象:白色沉淀迅速变为灰绿色,最终变为
(6)将
 黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到
黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到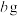 红棕色固体。若流程中加入的铁反应掉
红棕色固体。若流程中加入的铁反应掉 ,则该黑木耳中铁元素的质量分数为
,则该黑木耳中铁元素的质量分数为
您最近半年使用:0次
解题方法
5 . 某同学为了获取在 制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。
制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。
Ⅰ.向三颈瓶中加入饱和 溶液,按图示连接装置(夹持装置已略去,气密性已检查);
溶液,按图示连接装置(夹持装置已略去,气密性已检查);
Ⅱ.打开磁力搅拌器,立即加入 溶液;
溶液;
Ⅲ.采集三颈瓶内空气中 体积分数和溶液中
体积分数和溶液中 浓度的数据。
浓度的数据。
实验现象:
三颈瓶中生成白色絮状沉淀,沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
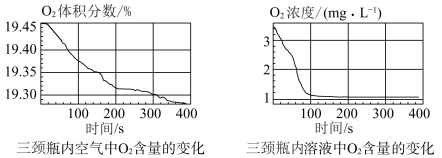
实验数据:
(1)搅拌的目的是___________ 。
(2)生成白色絮状沉淀的离子方程式为___________ 。
(3)沉淀由白色变为红褐色发生反应的化学方程式为___________ 。
(4)通过上述实验,可得到“在 制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是___________ 。
(5)结合上述实验,提出制备 过程中应注意的事项
过程中应注意的事项___________ (回答一项即可)。
 制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。
制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。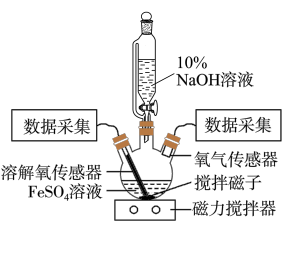
Ⅰ.向三颈瓶中加入饱和
 溶液,按图示连接装置(夹持装置已略去,气密性已检查);
溶液,按图示连接装置(夹持装置已略去,气密性已检查);Ⅱ.打开磁力搅拌器,立即加入
 溶液;
溶液;Ⅲ.采集三颈瓶内空气中
 体积分数和溶液中
体积分数和溶液中 浓度的数据。
浓度的数据。实验现象:
三颈瓶中生成白色絮状沉淀,沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
实验数据:
(1)搅拌的目的是
(2)生成白色絮状沉淀的离子方程式为
(3)沉淀由白色变为红褐色发生反应的化学方程式为
(4)通过上述实验,可得到“在
 制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是(5)结合上述实验,提出制备
 过程中应注意的事项
过程中应注意的事项
您最近半年使用:0次
6 . 健康人体内含铁元素大约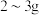 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:_____ ;试剂2的化学式为_____ 。
(2)加入新制氯水,溶液中发生反应的离子方程式是_____ 。
(3)加入试剂2时溶液为淡红色说明“速力非”中的 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_____ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:______ 。
(5) 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入______ ,防止 被氧化。
被氧化。
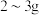 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:
(2)加入新制氯水,溶液中发生反应的离子方程式是
(3)加入试剂2时溶液为淡红色说明“速力非”中的
 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:(5)
 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入 被氧化。
被氧化。
您最近半年使用:0次
名校
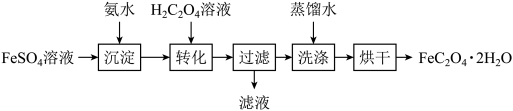
7 . 草酸亚铁晶体(FeC2O4·2H2O)可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如图:_______ 。
(2)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是_______ 。
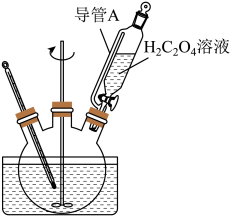
(3)“转化”在图所示的装置中进行。导管A的作用是_______ 。_______ 。
(5)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓H2SO4、磷酸,用0.04500mol·L-1KMnO4标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO2),消耗KMnO4标准溶液18.00mL。计算样品中FeC2O4·2H2O的纯度_______ (写出计算过程)。
(2)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是
(3)“转化”在图所示的装置中进行。导管A的作用是
(5)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓H2SO4、磷酸,用0.04500mol·L-1KMnO4标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO2),消耗KMnO4标准溶液18.00mL。计算样品中FeC2O4·2H2O的纯度
您最近半年使用:0次
8 . Fe(OH)2具有较强的还原性,新制的白色Fe(OH)2会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色Fe(OH)2,某实验小组做了如下探究实验。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、___________ 、___________ 。
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是___________ 。
(3)甲同学按如图a所示操作制备Fe(OH)2 (溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:___________ 。___________ (用离子方程式表示)。
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:___________ 。
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
①由以上实验可得到的规律是___________ 。
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为___________ (填“1.0”“1.5”或“2.0”)mol/L。
(6)实验创新:
延长Fe(OH)2沉淀的稳定时间还可以采取的措施为___________ (任写一条)。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是
(3)甲同学按如图a所示操作制备Fe(OH)2 (溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:

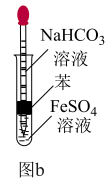
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
c(NaHCO3)/(mol/L) c(FeSO4)/(mol/L) | 1.0 | 1.5 | 2.0 | |
| 1.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 3.5 min | 9 min | 24 min | |
| 1.5 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 13 min | 15 min | 22 min | |
| 2.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率加快 | 常温下无现象,加热后产生白色沉淀 |
| 稳定时间 | 3 min | 8 min | 30 min | |
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为
(6)实验创新:
延长Fe(OH)2沉淀的稳定时间还可以采取的措施为
您最近半年使用:0次
2024-04-16更新
|
266次组卷
|
2卷引用:广东省湛江市2024届高三下学期第二次模拟测试化学试题
名校
9 . 铁黄(FeOOH)是一种重要的化工产品.由生产钛白粉废渣(主要成分为FeSO4∙H2O,含少量TiOSO4和不溶物)制备铁黄的过程如下:
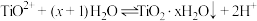
ii)Fe2+生成Fe(OH)2沉淀的pH:开始沉淀时pH=6.3,完全沉淀时pH=8.3;
Fe3+生成FeOOH沉淀的pH;开始沉淀时pH=1.5,完全沉淀时pH=2.8.
(1)纯化:加入过量铁粉的作用有:①__________ ;②__________ .
(2)制备晶种:为制备高品质铁黄产品,需先制备少量铁黄晶种.过程和现象是:向一定浓度FeSO4溶液中加入氨水,产生白色沉淀,并很快变成灰绿色.滴加氨水至pH为6.0时开始通空气并记录pH变化(如图).pH≈4时制得铁黄晶种.__________ .
②0~t2时段,Fe(OH)2和Fe2+转化为FeOOH制得铁黄晶种.
0~t1时段,发生化学反应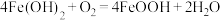 ,pH几乎不变;
,pH几乎不变;
t1~t2时段,pH明显降低.用离子方程式 解释pH明显降低的原因:__________ .
(3)产品纯度测定:铁黄(FeOOH)纯度可以通过产品的耗酸量确定,实验过程如下:
wg铁黄 溶液X
溶液X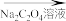 溶液Y
溶液Y 滴定
滴定
资料: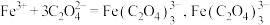 不与稀碱溶液反应;
不与稀碱溶液反应;
①用NaOH标准溶液测定溶解过程中剩余的酸,当溶液中的酸恰好被NaOH完全中和时,酚酞由无色变为浅粉色(pH在8~10范围),消耗b mol∙L-1的NaOH标准溶液V2mL,则所得铁黄样品的纯度为__________ ;(写出必要的计算过程)
②若Na2C2O4过量,会使测定结果__________ (填“偏大”“偏小”或“不受影响”);

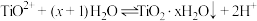
ii)Fe2+生成Fe(OH)2沉淀的pH:开始沉淀时pH=6.3,完全沉淀时pH=8.3;
Fe3+生成FeOOH沉淀的pH;开始沉淀时pH=1.5,完全沉淀时pH=2.8.
(1)纯化:加入过量铁粉的作用有:①
(2)制备晶种:为制备高品质铁黄产品,需先制备少量铁黄晶种.过程和现象是:向一定浓度FeSO4溶液中加入氨水,产生白色沉淀,并很快变成灰绿色.滴加氨水至pH为6.0时开始通空气并记录pH变化(如图).pH≈4时制得铁黄晶种.
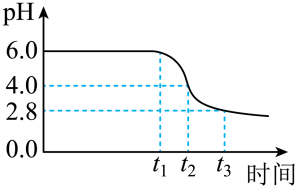
②0~t2时段,Fe(OH)2和Fe2+转化为FeOOH制得铁黄晶种.
0~t1时段,发生化学反应
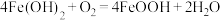 ,pH几乎不变;
,pH几乎不变;t1~t2时段,pH明显降低.用
(3)产品纯度测定:铁黄(FeOOH)纯度可以通过产品的耗酸量确定,实验过程如下:
wg铁黄
 溶液X
溶液X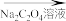 溶液Y
溶液Y 滴定
滴定资料:
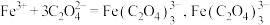 不与稀碱溶液反应;
不与稀碱溶液反应;①用NaOH标准溶液测定溶解过程中剩余的酸,当溶液中的酸恰好被NaOH完全中和时,酚酞由无色变为浅粉色(pH在8~10范围),消耗b mol∙L-1的NaOH标准溶液V2mL,则所得铁黄样品的纯度为
②若Na2C2O4过量,会使测定结果
您最近半年使用:0次
名校
解题方法
10 . 某小组同学为了获取在 制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图1所示装置进行了如下实验(夹持装置已略去,气密性已检验)。
制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图1所示装置进行了如下实验(夹持装置已略去,气密性已检验)。

【进行实验】
实验步骤:
I.向瓶中加入饱和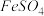 溶液,按图1所示连接装置;
溶液,按图1所示连接装置;
II.打开磁力搅拌器,立即加入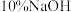 溶液;
溶液;
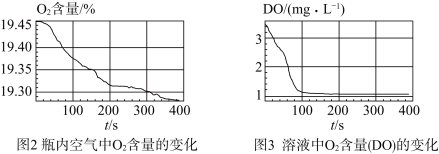
III.采集瓶内空气中 含量和溶液中
含量和溶液中 含量(DO)的数据。
含量(DO)的数据。
实验现象:生成白色絮状沉淀,白色沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
实验数据:
【解释与结论】
(1)盛放 的仪器为
的仪器为_________________ 。
(2)搅拌的目的是_________________ 。
(3)生成白色沉淀的离子方程式是_________________ 。
(4)红褐色沉淀是_________________ 。
(5)通过上述实验,可得到“在 制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是_________________ 。
(6)结合上述实验,提出制备 过程中应注意的事项
过程中应注意的事项_________________ (回答一项即可)。
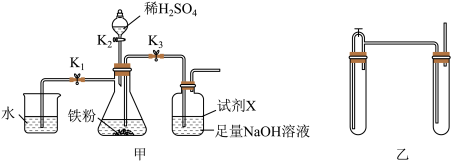
(7)某实验小组用如图甲所示装置制备 。下列说法正确的是( )
。下列说法正确的是( )
 制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图1所示装置进行了如下实验(夹持装置已略去,气密性已检验)。
制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图1所示装置进行了如下实验(夹持装置已略去,气密性已检验)。
【进行实验】
实验步骤:
I.向瓶中加入饱和
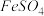 溶液,按图1所示连接装置;
溶液,按图1所示连接装置;II.打开磁力搅拌器,立即加入
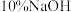 溶液;
溶液;III.采集瓶内空气中
 含量和溶液中
含量和溶液中 含量(DO)的数据。
含量(DO)的数据。实验现象:生成白色絮状沉淀,白色沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
实验数据:

【解释与结论】
(1)盛放
 的仪器为
的仪器为(2)搅拌的目的是
(3)生成白色沉淀的离子方程式是
(4)红褐色沉淀是
(5)通过上述实验,可得到“在
 制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是(6)结合上述实验,提出制备
 过程中应注意的事项
过程中应注意的事项(7)某实验小组用如图甲所示装置制备
 。下列说法正确的是( )
。下列说法正确的是( )
| A.甲装置在使用前需检查气密性 |
B.实验时打开旋塞的顺序依次为 |
| C.试剂X可选用植物油,其主要作用是隔绝空气 |
D.甲选用装置中除水外的药品,可用乙装置代替甲装置制备 |
您最近半年使用:0次



