名校
1 . 某学习小组为认识铁及其化合物的性质和分散系的性质做了如下一系列综合实验。运用所学知识,回答下列问题:
(1)可利用___________ 来区分 胶体和
胶体和 溶液。
溶液。
(2)向盛有 溶液的试管中滴加
溶液的试管中滴加 溶液,请描述发生的现象
溶液,请描述发生的现象___________ 。
(3)铁粉与水蒸气在高温条件下反应的化学方程式是___________ 。
(4)电子工业中,人们常用 溶液腐蚀覆铜板来制作印刷电路板。现欲配制
溶液腐蚀覆铜板来制作印刷电路板。现欲配制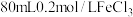 溶液,回答下列问题:
溶液,回答下列问题:
①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需___________ 。
②使用托盘天平称量 的质量为
的质量为___________ g。
③定容时,若仰视容量瓶刻度线会使配制的 溶液浓度
溶液浓度________ (填“偏大”“偏小”或“不变”)。
(5)实验室模拟用 溶液腐蚀铜板并从废液中回收
溶液腐蚀铜板并从废液中回收 和
和 溶液流程如图所示:
溶液流程如图所示:
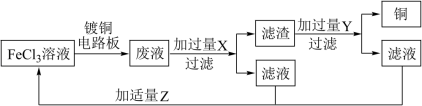
①请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式___________ 。
②试剂 在反应中体现
在反应中体现___________ (填“氧化性”或“还原性”)。
③Z可选用的试剂有___________ (填序号)。
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
(1)可利用
 胶体和
胶体和 溶液。
溶液。(2)向盛有
 溶液的试管中滴加
溶液的试管中滴加 溶液,请描述发生的现象
溶液,请描述发生的现象(3)铁粉与水蒸气在高温条件下反应的化学方程式是
(4)电子工业中,人们常用
 溶液腐蚀覆铜板来制作印刷电路板。现欲配制
溶液腐蚀覆铜板来制作印刷电路板。现欲配制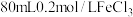 溶液,回答下列问题:
溶液,回答下列问题:①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需
②使用托盘天平称量
 的质量为
的质量为③定容时,若仰视容量瓶刻度线会使配制的
 溶液浓度
溶液浓度(5)实验室模拟用
 溶液腐蚀铜板并从废液中回收
溶液腐蚀铜板并从废液中回收 和
和 溶液流程如图所示:
溶液流程如图所示:
①请写出
 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式②试剂
 在反应中体现
在反应中体现③Z可选用的试剂有
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
您最近一年使用:0次
2023-08-03更新
|
364次组卷
|
5卷引用:甘肃省天水市第一中学2023-2024学年高一下学期开学化学试题
甘肃省天水市第一中学2023-2024学年高一下学期开学化学试题湖南省株洲市南方中学2022-2023学年高一上学期期末考试化学试题(已下线)巩固测试卷02-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)湖南省娄底市新化县2023-2024学年高一上学期期末考试化学试题山东省滨州市惠民县第二中学2023-2024学年高一上学期12月月考化学试题
2 . 铁及其化合物在生产生活中有重要用途。某化学兴趣小组同学设计以下实验探究铁及其化合物性质。
I.“铁与水反应”的实验,并检验产物的性质:
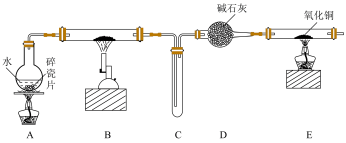
(1)A装置的作用是___________ 。
(2)B中反应的化学方程式为___________ 。
(3)点燃E处酒精灯之前应进行的操作是___________ 。
Ⅱ.制备氢氧化亚铁:设计如下实验能较长时间观察到白色Fe(OH)2沉淀,选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。
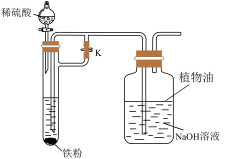
(4)植物油的作用是___________ 。
(5)实验时,先___________ (填“打开”或“关闭”)止水夹K,然后打开分液漏斗的玻璃塞和活塞,使稀硫酸与铁粉反应,一段时间后,___________ (填“打开”或“关闭”)止水夹K,制得白色Fe(OH)2沉淀,且沉淀能持续一段时间不变色。
Ⅲ.制备FeCl3:已知无水FeCl3在空气中遇水易潮解,加热易升华,实验装置如图。
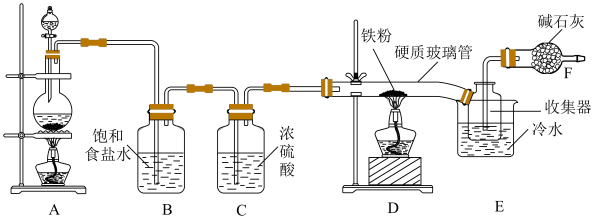
(6)饱和食盐水的作用是___________ 。
(7)装置D发生反应的化学方程式为___________ 。
(8)硬质玻璃管直接接入收集器的优点是___________ 。
(9)F装置的两个作用是___________ 、___________ 。
I.“铁与水反应”的实验,并检验产物的性质:

(1)A装置的作用是
(2)B中反应的化学方程式为
(3)点燃E处酒精灯之前应进行的操作是
Ⅱ.制备氢氧化亚铁:设计如下实验能较长时间观察到白色Fe(OH)2沉淀,选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。

(4)植物油的作用是
(5)实验时,先
Ⅲ.制备FeCl3:已知无水FeCl3在空气中遇水易潮解,加热易升华,实验装置如图。

(6)饱和食盐水的作用是
(7)装置D发生反应的化学方程式为
(8)硬质玻璃管直接接入收集器的优点是
(9)F装置的两个作用是
您最近一年使用:0次
2023-07-24更新
|
455次组卷
|
3卷引用:甘肃省天水市第一中学2023-2024学年高一上学期12月月考化学试题
解题方法
3 . 电子工业中常用覆铜板为材料,利用FeCl3溶液做“腐蚀液”制作印刷电路板。从废腐蚀液(含FeCl3,FeCl2和CuCl2)中回收Cu并实现FeCl3溶液循环再利用,其工艺流程如下:

回答下列问题:
(1)工业上制作印刷电路板时发生的化学反应方程式为_______ 。
(2)操作方法①为_______ ,固体A的成分为_______ (填化学式)。
(3)实验室检验溶液A中是否含有FeCl3的试剂为_______ 溶液(填化学式)。
(4)溶液A中加入NaOH溶液时产生的实验现象为_______ 。
(5)若回收过程中取废腐蚀液V L,回收到a g Cu,则废腐蚀液中Cu2+的物质的量浓度为_______ mol/L(用含a和V的表达式表示)。

回答下列问题:
(1)工业上制作印刷电路板时发生的化学反应方程式为
(2)操作方法①为
(3)实验室检验溶液A中是否含有FeCl3的试剂为
(4)溶液A中加入NaOH溶液时产生的实验现象为
(5)若回收过程中取废腐蚀液V L,回收到a g Cu,则废腐蚀液中Cu2+的物质的量浓度为
您最近一年使用:0次
名校
解题方法
4 . 如图所示为部分物质(或其溶液)间的转化关系(除水外,其他反应物、生成物均已列出)。已知 为紫红色金属单质,
为紫红色金属单质, 为能使带火星的木条复燃的气体,
为能使带火星的木条复燃的气体, 为红褐色沉淀,
为红褐色沉淀, 的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。
的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。

(1)写出下列物质的化学式:A___________ 、G___________ 。
(2)I加热分解产生的固体产物俗称___________ ,写出其一种用途:___________ 。
(3)F与H作用生成I的化学方程式为___________ ; 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(4)除去D溶液中混有的J,最好使用的方法是___________ (用离子方程式表示)。
 为紫红色金属单质,
为紫红色金属单质, 为能使带火星的木条复燃的气体,
为能使带火星的木条复燃的气体, 为红褐色沉淀,
为红褐色沉淀, 的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。
的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。
(1)写出下列物质的化学式:A
(2)I加热分解产生的固体产物俗称
(3)F与H作用生成I的化学方程式为
 与
与 反应的离子方程式为
反应的离子方程式为(4)除去D溶液中混有的J,最好使用的方法是
您最近一年使用:0次
5 . 某小组同学为了获取在 制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图1所示装置进行了如下实验(夹持装置已略去,气密性已检验)。
制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图1所示装置进行了如下实验(夹持装置已略去,气密性已检验)。

【进行实验】
实验步骤:I.向瓶中加入饱和 溶液,按图1所示连接装置;
溶液,按图1所示连接装置;
II.打开磁力搅拌器,立即加入10% NaOH溶液;
III.采集瓶内空气中 含量和溶液中
含量和溶液中 含量(DO)的数据。
含量(DO)的数据。
实验现象:生成白色絮状沉淀,白色沉淀迅速变为灰绿色,一段时间后部分变为红褐色。实验数据:

【解释与结论】
(1)搅拌的目的是_______ 。
(2)生成白色沉淀的离子方程式是_______ 。
(3)红褐色沉淀是_______ ;生成红褐色沉淀的化学方程式是_______ 。
(4)通过上述实验,可得到“在 制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是_______ 。
 制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图1所示装置进行了如下实验(夹持装置已略去,气密性已检验)。
制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图1所示装置进行了如下实验(夹持装置已略去,气密性已检验)。
【进行实验】
实验步骤:I.向瓶中加入饱和
 溶液,按图1所示连接装置;
溶液,按图1所示连接装置;II.打开磁力搅拌器,立即加入10% NaOH溶液;
III.采集瓶内空气中
 含量和溶液中
含量和溶液中 含量(DO)的数据。
含量(DO)的数据。实验现象:生成白色絮状沉淀,白色沉淀迅速变为灰绿色,一段时间后部分变为红褐色。实验数据:

【解释与结论】
(1)搅拌的目的是
(2)生成白色沉淀的离子方程式是
(3)红褐色沉淀是
(4)通过上述实验,可得到“在
 制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
您最近一年使用:0次
名校
解题方法
6 . 现有常见金属单质A、B和气体甲、乙、丙及物质C、D、E、F它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。
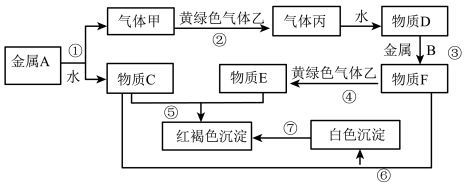
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A_______ 、F_______ 。
(2)写出由物质E制备氢氧化铁胶体反应的方程式:_______ 。
(3)写出气体乙跟水反应的离子方程式:_______ ;
反应①离子方程式_______ ;
反应③离子方程式_______ ;
反应⑦化学方程式_______ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A
(2)写出由物质E制备氢氧化铁胶体反应的方程式:
(3)写出气体乙跟水反应的离子方程式:
反应①离子方程式
反应③离子方程式
反应⑦化学方程式
您最近一年使用:0次
2023-01-04更新
|
525次组卷
|
2卷引用:甘肃省武威市天祝藏族自治县第一中学2022-2023学年高一下学期开学考试化学试题
解题方法
7 . 某实验小组对制备 产生了浓厚的兴趣,其探究制备
产生了浓厚的兴趣,其探究制备 的过程如下(实验所用溶液均由去氧蒸馏水配制)。首先该小组的同学制备氢氧化亚铁的装置如图1。
的过程如下(实验所用溶液均由去氧蒸馏水配制)。首先该小组的同学制备氢氧化亚铁的装置如图1。

(1)图1中制备氢氧化亚铁时观察到的现象为___________ ,该现象对应反应的化学方程式为___________ 、___________ ;若不加入任何试剂,则改良实验可采取的措施为___________ 。
(2)由于上述方法制得的 存在的时间太短,无法长时间观察到
存在的时间太短,无法长时间观察到 的颜色,经小组讨论后,将实验装置改为如图2所示。已知:苯是一种密度小于钠的液体,空气不能溶解在苯中,且反应过程中苯不参加反应。
的颜色,经小组讨论后,将实验装置改为如图2所示。已知:苯是一种密度小于钠的液体,空气不能溶解在苯中,且反应过程中苯不参加反应。

①苯的作用为___________ 。
②将钠块加入试管中,可以观察到的现象为___________ ,钠块发生反应的离子方程式为___________ 。
 产生了浓厚的兴趣,其探究制备
产生了浓厚的兴趣,其探究制备 的过程如下(实验所用溶液均由去氧蒸馏水配制)。首先该小组的同学制备氢氧化亚铁的装置如图1。
的过程如下(实验所用溶液均由去氧蒸馏水配制)。首先该小组的同学制备氢氧化亚铁的装置如图1。
(1)图1中制备氢氧化亚铁时观察到的现象为
(2)由于上述方法制得的
 存在的时间太短,无法长时间观察到
存在的时间太短,无法长时间观察到 的颜色,经小组讨论后,将实验装置改为如图2所示。已知:苯是一种密度小于钠的液体,空气不能溶解在苯中,且反应过程中苯不参加反应。
的颜色,经小组讨论后,将实验装置改为如图2所示。已知:苯是一种密度小于钠的液体,空气不能溶解在苯中,且反应过程中苯不参加反应。
①苯的作用为
②将钠块加入试管中,可以观察到的现象为
您最近一年使用:0次
8 . 各物质的转化关系如图所示,其中M、X均为单质,A、B、C、D、E、F、G均为化合物,B为碱且其溶液的焰色反应呈黄绿色。向E溶液中滴加AgNO3溶液得到不溶于酸的白色沉淀。回答下列问题:

(1)M、B分别为___________ 、___________ 。(填化学式)
(2)C溶液和稀硫酸反应的离子方程式为___________ 。
(3)白色沉淀D转化成Fe(OH)3沉淀的化学方程式为___________ ,反应现象为___________ 。
(4)为探究Fe及Fe3+的氧化性或还原性:将M加入G溶液中观察到的现象为___________ ,由此可得出的结论是___________ 。

(1)M、B分别为
(2)C溶液和稀硫酸反应的离子方程式为
(3)白色沉淀D转化成Fe(OH)3沉淀的化学方程式为
(4)为探究Fe及Fe3+的氧化性或还原性:将M加入G溶液中观察到的现象为
您最近一年使用:0次
名校
解题方法
9 . A、B、C、D、E五种物质之间有如图所示的转化关系:

已知:A是红棕色粉末,由E转化成C的现象是白色沉淀迅速变为灰绿色,最后变为红褐色。回答问题:
(1)写出下列物质的化学式:A___________ ,B___________ ,D___________ ,甲____________ 。
(2)写出B→C的离子反应方程式__________________________________________ ;
(3)写出E→C的化学反应方程式__________________________________________ 。

已知:A是红棕色粉末,由E转化成C的现象是白色沉淀迅速变为灰绿色,最后变为红褐色。回答问题:
(1)写出下列物质的化学式:A
(2)写出B→C的离子反应方程式
(3)写出E→C的化学反应方程式
您最近一年使用:0次
2021-01-08更新
|
546次组卷
|
3卷引用:甘肃省兰州市第一中学2020-2021学年高一上学期期末考试化学(文)试题
10 . 物质A、B、C、D、E、F、G、H、I、J、K存在下图转化关系,其中气体D、E为单质,试回答:

(1)写出下列物质的化学式:A是_______ ,F是_______ ,I是_______ 。
(2)写出反应“C→F”的离子方程式:_______ 。
(3)写出反应“F→G”的化学方程式:_______ 。
(4)在溶液I中滴入NaOH溶液,可观察到的现象是_______ 。

(1)写出下列物质的化学式:A是
(2)写出反应“C→F”的离子方程式:
(3)写出反应“F→G”的化学方程式:
(4)在溶液I中滴入NaOH溶液,可观察到的现象是
您最近一年使用:0次



