1 . 铁及其化合物在生产、生活中有着广泛的应用。
(1)刻制铜印刷电路板时,要用FeCl3溶液作为“腐蚀液”,发生反应的离子方程式为_______ ,为了将反应后溶液中的Cu2+回收利用,并得到含有一种溶质的溶液,进行的具体操作是_______ 。
(2)高温时16.8g铁与足量水蒸气反应,生成气体的体积是_______ L(标准状况下)。
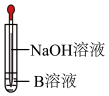
(3)如图,在胶头滴管挤出NaOH溶液的瞬间可观察到生成白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色,请写出上述现象中白色沉淀转化成红褐色沉淀的化学方程式_______ 。_______ 。
②酸浸时,Fe3O4与硫酸反应的化学方程式为_______ ;通入O2的目的是_______ 。
③滤渣的成分是_______ (填化学式)。
④“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+,再用酸性K2Cr2O7标准溶液测定Fe2+的量( 被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是
被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是_______ 。
(1)刻制铜印刷电路板时,要用FeCl3溶液作为“腐蚀液”,发生反应的离子方程式为
(2)高温时16.8g铁与足量水蒸气反应,生成气体的体积是
(3)如图,在胶头滴管挤出NaOH溶液的瞬间可观察到生成白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色,请写出上述现象中白色沉淀转化成红褐色沉淀的化学方程式
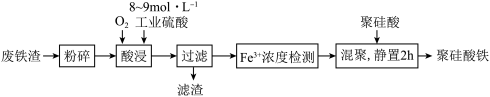
②酸浸时,Fe3O4与硫酸反应的化学方程式为
③滤渣的成分是
④“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+,再用酸性K2Cr2O7标准溶液测定Fe2+的量(
 被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是
被还原为Cr3+),则SnCl2、Fe2+和Cr3+中还原性最强的是
您最近一年使用:0次
名校
解题方法
2 . 采用氧化沉淀法可以利用绿矾制取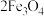 ,其制取流程如图所示:
,其制取流程如图所示:___________ (填写化学式),由溶液 获得该副产品的操作是:蒸发浓缩→
获得该副产品的操作是:蒸发浓缩→___________ →过滤洗涤 晶体加热至完全失去结晶水。
晶体加热至完全失去结晶水。
(2)某兴趣小组模仿如图流程制取 ,在实验前要测定绿矾的含量:称取
,在实验前要测定绿矾的含量:称取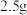 工业绿矾,配制成
工业绿矾,配制成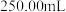 溶液。量取
溶液。量取 溶液于锥形瓶中,用
溶液于锥形瓶中,用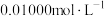 酸性
酸性 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的平均体积为
溶液的平均体积为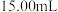 。(滴定时发生反应的离子方程式为
。(滴定时发生反应的离子方程式为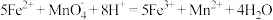 )则绿矾的质量分数为
)则绿矾的质量分数为___________ (计算结果保留三位小数)。
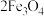 ,其制取流程如图所示:
,其制取流程如图所示:
 获得该副产品的操作是:蒸发浓缩→
获得该副产品的操作是:蒸发浓缩→ 晶体加热至完全失去结晶水。
晶体加热至完全失去结晶水。(2)某兴趣小组模仿如图流程制取
 ,在实验前要测定绿矾的含量:称取
,在实验前要测定绿矾的含量:称取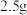 工业绿矾,配制成
工业绿矾,配制成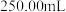 溶液。量取
溶液。量取 溶液于锥形瓶中,用
溶液于锥形瓶中,用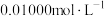 酸性
酸性 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的平均体积为
溶液的平均体积为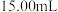 。(滴定时发生反应的离子方程式为
。(滴定时发生反应的离子方程式为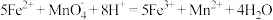 )则绿矾的质量分数为
)则绿矾的质量分数为
您最近一年使用:0次
3 . 健康人体内含铁元素大约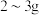 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:_____ ;试剂2的化学式为_____ 。
(2)加入新制氯水,溶液中发生反应的离子方程式是_____ 。
(3)加入试剂2时溶液为淡红色说明“速力非”中的 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_____ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:______ 。
(5) 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入______ ,防止 被氧化。
被氧化。
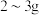 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:
(2)加入新制氯水,溶液中发生反应的离子方程式是
(3)加入试剂2时溶液为淡红色说明“速力非”中的
 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:(5)
 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入 被氧化。
被氧化。
您最近一年使用:0次
名校
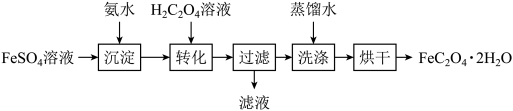
4 . 草酸亚铁晶体(FeC2O4·2H2O)可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如图:_______ 。
(2)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是_______ 。
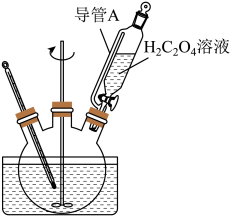
(3)“转化”在图所示的装置中进行。导管A的作用是_______ 。_______ 。
(5)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓H2SO4、磷酸,用0.04500mol·L-1KMnO4标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO2),消耗KMnO4标准溶液18.00mL。计算样品中FeC2O4·2H2O的纯度_______ (写出计算过程)。
(2)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是
(3)“转化”在图所示的装置中进行。导管A的作用是
(5)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓H2SO4、磷酸,用0.04500mol·L-1KMnO4标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO2),消耗KMnO4标准溶液18.00mL。计算样品中FeC2O4·2H2O的纯度
您最近一年使用:0次
5 . 高铁酸钾(K2FeO4)是一种高效、无毒的强氧化剂。在工业上,一种通过FeSO4溶液制备K2FeO4的工艺流程如图所示。回答下列问题:
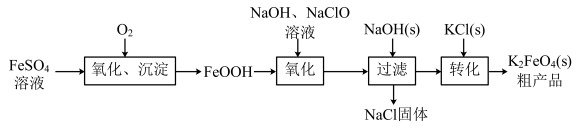
(1)K2FeO4中Fe元素的化合价为_______ 价
(2)“氧化、沉淀”时,氧化剂和还原剂的物质的量之比为_______ 。Fe2+在溶液中放置不稳定,易被氧化成Fe3+,用KSCN溶液检验溶液中的Fe3+是较好的方法,此法的离子方程式为_______ 。
(3)通过“氧化”时FeOOH与NaClO反应生成的Na2FeO4可知,在该条件下物质氧化性:Na2FeO4_______ NaClO(填“>”或“<”)。
(4)写出氢氧化亚铁溶液被空气中氧化为氢氧化铁的化学方程式_______ 。
(5)过滤操作所需要的玻璃仪器有烧杯和_______ 。

(1)K2FeO4中Fe元素的化合价为
(2)“氧化、沉淀”时,氧化剂和还原剂的物质的量之比为
(3)通过“氧化”时FeOOH与NaClO反应生成的Na2FeO4可知,在该条件下物质氧化性:Na2FeO4
(4)写出氢氧化亚铁溶液被空气中氧化为氢氧化铁的化学方程式
(5)过滤操作所需要的玻璃仪器有烧杯和
您最近一年使用:0次
名校
解题方法
6 . 某工厂的工业废水中含有大量的Fe2(SO4)3和较多的CuSO4。为了减少污染并变废为宝,工厂计划从该废水中回收绿矾和金属铜。请根据以下流程图,回答下列问题:
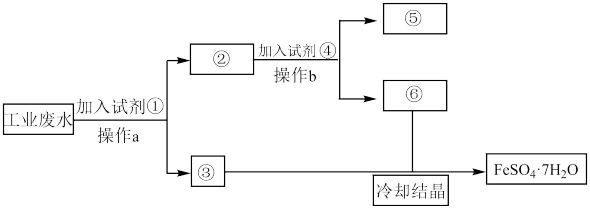
(1)操作a的名称为___________ 。
(2)②中物质为___________ ,试剂④为___________ 。鉴别溶液⑥中的金属阳离子时,应滴加的试剂依次是___________ 。请写出该鉴别过程中属于氧化还原反应的离子方程式___________ 。
(3)若取2mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是___________ 。

(1)操作a的名称为
(2)②中物质为
(3)若取2mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是
您最近一年使用:0次
名校
解题方法
7 . 用 溶液刻蚀铜电路板,对刻蚀后的液体(含
溶液刻蚀铜电路板,对刻蚀后的液体(含 、
、 和
和 )进行处理以提取
)进行处理以提取 和
和 ,流程如图所示:
,流程如图所示:
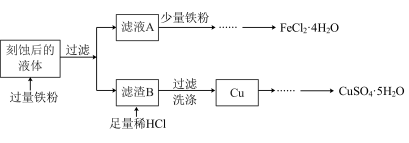
回答下列问题:
(1)氯化铁溶液刻蚀铜电路板的离子方程式为_______ ,过氧化氢和盐酸的混合溶液也可以刻蚀铜电路板,反应的化学方程式为_______ 。
(2)取少量滤液 ,滴入
,滴入 溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成
溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成_______ 沉淀。白色沉淀转化过程对应的化学方程式为_______ 。
(3)检验刻蚀后液体中 通常选用的试剂为
通常选用的试剂为_______ ,滤渣 的主要成分为
的主要成分为_______ 。
(4)检验滤渣 中提取出的
中提取出的 已经洗净的操作为
已经洗净的操作为_______ 。
 溶液刻蚀铜电路板,对刻蚀后的液体(含
溶液刻蚀铜电路板,对刻蚀后的液体(含 、
、 和
和 )进行处理以提取
)进行处理以提取 和
和 ,流程如图所示:
,流程如图所示:
回答下列问题:
(1)氯化铁溶液刻蚀铜电路板的离子方程式为
(2)取少量滤液
 ,滴入
,滴入 溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成
溶液,其现象:生成的白色絮状沉淀迅速变成灰绿色,最终生成(3)检验刻蚀后液体中
 通常选用的试剂为
通常选用的试剂为 的主要成分为
的主要成分为(4)检验滤渣
 中提取出的
中提取出的 已经洗净的操作为
已经洗净的操作为
您最近一年使用:0次
8 . 某铜冶炼厂排放的废水中含有较多的 、
、 、
、 、
、 和少量的
和少量的 ,为了减少污染并变废为宝,以该废水为原料制备硫酸钠、硫酸亚铁晶体(
,为了减少污染并变废为宝,以该废水为原料制备硫酸钠、硫酸亚铁晶体( )并回收金属铜,设计了如下流程(流程中加入的试剂均过量)。
)并回收金属铜,设计了如下流程(流程中加入的试剂均过量)。
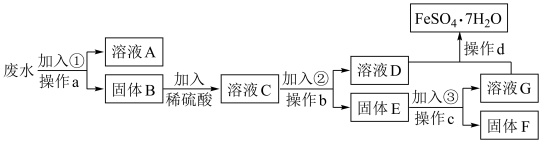
已知:加入试剂①为 溶液。回答下列问题:
溶液。回答下列问题:
(1)在实验室进行操作a的名称是___________ ;溶液A中所含的溶质主要为___________ (填化学式)。
(2)加入试剂②为___________ (填化学式);溶液C中的一种离子可与固体F反应,该反应的离子方程式为___________ 。
(3)若取2mL溶液G加入试管中,然后滴加氢氧化钠溶液,可观察到的现象为___________ ,此现象中涉及的氧化还原反应的化学方程式为___________ 。
(4)操作d为蒸发浓缩、___________ 、过滤、洗涤、干燥得到硫酸亚铁晶体,该过程中需要用到的玻璃仪器除烧杯、漏斗、酒精灯外,还有___________ 。该仪器在操作d过程中的作用是___________ 。(答出一点即可)
 、
、 、
、 、
、 和少量的
和少量的 ,为了减少污染并变废为宝,以该废水为原料制备硫酸钠、硫酸亚铁晶体(
,为了减少污染并变废为宝,以该废水为原料制备硫酸钠、硫酸亚铁晶体( )并回收金属铜,设计了如下流程(流程中加入的试剂均过量)。
)并回收金属铜,设计了如下流程(流程中加入的试剂均过量)。
已知:加入试剂①为
 溶液。回答下列问题:
溶液。回答下列问题:(1)在实验室进行操作a的名称是
(2)加入试剂②为
(3)若取2mL溶液G加入试管中,然后滴加氢氧化钠溶液,可观察到的现象为
(4)操作d为蒸发浓缩、
您最近一年使用:0次
解题方法
9 . 资源的回收利用,对可持续发展有着重要意义。某工业废料中主要含 、
、 等,现欲利用如图工业流程回收某些金属资源。
等,现欲利用如图工业流程回收某些金属资源。
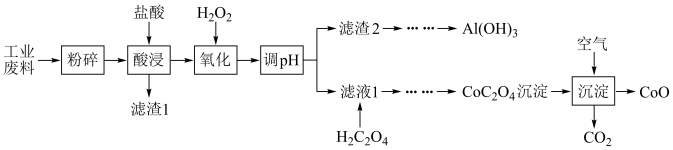
已知:①空气中氧气的体积分数约为20%。回答下列问题:
(1)“粉碎”的目的为___________ ,调节pH后的实验操作是___________ ;
(2)“氧化”的目的是将 氧化为
氧化为 ,其反应的离子方程式为
,其反应的离子方程式为___________ ;“氧化”过程中温度控制在 ,避免温度过高的原因为
,避免温度过高的原因为___________ ;
(3) 的化合物一般都容易被氧化,比如氢氧化亚铁在潮湿的空气中被氧化而发生变色,最终变为
的化合物一般都容易被氧化,比如氢氧化亚铁在潮湿的空气中被氧化而发生变色,最终变为___________ 色,写出其化学方程式___________ ;
(4)新型富钴电池常用到 的化合物
的化合物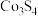 ,其化学性质与
,其化学性质与 相似,则
相似,则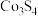 中Co的化合价为
中Co的化合价为___________ ;
(5)“煅烧”反应的化学方程式为___________ ,每制备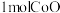 ,至少需要标准状况下的空气体积为
,至少需要标准状况下的空气体积为___________ L。
 、
、 等,现欲利用如图工业流程回收某些金属资源。
等,现欲利用如图工业流程回收某些金属资源。
已知:①空气中氧气的体积分数约为20%。回答下列问题:
(1)“粉碎”的目的为
(2)“氧化”的目的是将
 氧化为
氧化为 ,其反应的离子方程式为
,其反应的离子方程式为 ,避免温度过高的原因为
,避免温度过高的原因为(3)
 的化合物一般都容易被氧化,比如氢氧化亚铁在潮湿的空气中被氧化而发生变色,最终变为
的化合物一般都容易被氧化,比如氢氧化亚铁在潮湿的空气中被氧化而发生变色,最终变为(4)新型富钴电池常用到
 的化合物
的化合物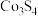 ,其化学性质与
,其化学性质与 相似,则
相似,则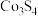 中Co的化合价为
中Co的化合价为(5)“煅烧”反应的化学方程式为
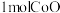 ,至少需要标准状况下的空气体积为
,至少需要标准状况下的空气体积为
您最近一年使用:0次
名校
解题方法
10 . 某磁铁矿石A主要成分是磁性氧化铁(Fe3O4),还含少量Al2O3、Cu2O。某工厂利用此矿石进行有关物质的回收利用,其中F为常见的补铁剂,工艺流程如图(已知Cu2O不溶于水和碱,但溶于强酸: )。根据流程回答下列问题:
)。根据流程回答下列问题:

(1)溶液C的溶质主要是___________ 。
(2)溶液D与过量试剂X反应的离子方程式是___________ 、___________ 、Fe + 2H+ = Fe2+ + H2↑。
(3)在溶液F中滴加NaOH溶液的现象是___________ 。
(4)已知该工艺中使用的H2SO4溶液浓度均为2.0 mol•L-1,若操作4可得到1.0 mol固体E,则操作2中Cu2O消耗的H2SO4溶液体积为______ mL。
 )。根据流程回答下列问题:
)。根据流程回答下列问题:
(1)溶液C的溶质主要是
(2)溶液D与过量试剂X反应的离子方程式是
(3)在溶液F中滴加NaOH溶液的现象是
(4)已知该工艺中使用的H2SO4溶液浓度均为2.0 mol•L-1,若操作4可得到1.0 mol固体E,则操作2中Cu2O消耗的H2SO4溶液体积为
您最近一年使用:0次



