1 . A~J是中学化学中常见的化学物质,它们之间的相互转化关系如下列框图所示(部分反应的产物未列出)。

已知:A、F为无色气体单质,B为无色具有刺激性气味的碱性气体,C为黑色氧化物,E为红色金属单质。请回答下列问题:
(1)D的化学式为_____________ ;F的电子式为______________ 。
(2)B和C反应的化学方程式为_______________ 。该反应中生成1molF时,转移的电子数为_________ mol
(3)E与G的稀溶液反应的离子方程式为:____________________ 。
(4)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式___________________ 。

已知:A、F为无色气体单质,B为无色具有刺激性气味的碱性气体,C为黑色氧化物,E为红色金属单质。请回答下列问题:
(1)D的化学式为
(2)B和C反应的化学方程式为
(3)E与G的稀溶液反应的离子方程式为:
(4)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式
您最近一年使用:0次
2 . 某研究小组通过实验探究Cu及其化合物的性质,操作正确且能达到实验目的的是
| A.将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色 |
| B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成 |
| C.将CuCl2溶液在蒸发皿中加热蒸干,得到Cu(OH)2固体 |
| D.将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿 |
您最近一年使用:0次
解题方法
3 . 辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下:
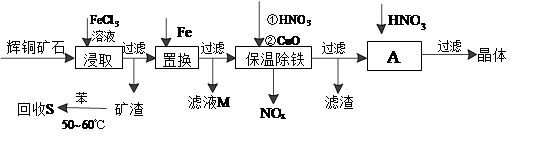
(1)写出浸取过程中Cu2S溶解的离子方程式____________ 。
(2)回收S过程中温度控制在50℃~60℃之间,不宜过高或过低的原因是_________ 、__________ 。
(3)保温除铁过程中加入CuO的目的是____________ 。
(4)A步操作为____________ 要用硝酸调节溶液的pH,其理由是____________ 。

(1)写出浸取过程中Cu2S溶解的离子方程式
(2)回收S过程中温度控制在50℃~60℃之间,不宜过高或过低的原因是
(3)保温除铁过程中加入CuO的目的是
(4)A步操作为
您最近一年使用:0次
名校
解题方法
4 . 在如图所示的有关物质转化关系中,各物质均是我们中学化学所学的物质。C为一种黑色粉末,D为一种气体。
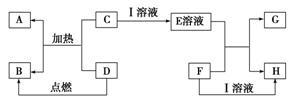
请根据框图中物质的转化关系及相关信息,用化学式填写下列空白:
(1)若F为可溶性碱,G为蓝色沉淀,则A为_________________ ;D可能为__________________ 。
(2)若G为蓝色沉淀,H为难溶性盐,则I为_________________ 。
(3)若G、H都属于盐,且G为蓝色溶液,则I可能为______________ ;F可能为_____________ 。

请根据框图中物质的转化关系及相关信息,用化学式填写下列空白:
(1)若F为可溶性碱,G为蓝色沉淀,则A为
(2)若G为蓝色沉淀,H为难溶性盐,则I为
(3)若G、H都属于盐,且G为蓝色溶液,则I可能为
您最近一年使用:0次
2016-12-09更新
|
387次组卷
|
2卷引用:江苏省扬州中学2020-2021学年高一上学期开学考暨奥赛选拔化学试题
名校
5 . 下物质间的转化通过一步化学反应不能实现的是
| A.Fe → Fe3O4 | B.CuO → Cu(OH)2 |
| C.HCl → Cl2 | D.Na → Na2O |
您最近一年使用:0次
2016-12-09更新
|
236次组卷
|
3卷引用:2014-2015江苏省南通中学高二上学期期末化学试卷
14-15高三上·江苏宿迁·阶段练习
名校
6 . 向一定量的Cu、Fe2O3的混合物中加入100 mL 2 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
| A.3.2 g | B.2.4 g | C.1.6 g | D.0.8 g |
您最近一年使用:0次
2016-12-09更新
|
349次组卷
|
8卷引用:2015届江苏省沭阳县银河学校高三上学期第一次阶段性检测化学试卷
7 . 我国古代“药金”的冶炼方法是:将炉甘石(ZnCO3)和赤铜矿(Cu2O)与木炭按一定的比例混合后加热至800℃,即可炼出闪烁似金子般光泽的“药金”。下列叙述正确的是
| A.“药金”实质上是铜锌合金 |
| B.冶炼炉中炉甘石直接被木炭还原为锌 |
| C.用王水可区别黄金和“药金” |
| D.用火焰灼烧不能区别黄金和药金 |
您最近一年使用:0次
2016-12-09更新
|
1193次组卷
|
11卷引用:2014年高一化学人教版必修二 4-1-1金属矿物的开发利用练习卷
(已下线)2014年高一化学人教版必修二 4-1-1金属矿物的开发利用练习卷山西省应县第一中学校2018-2019学年高一下学期期末考试化学试题2020届高三化学无机化学二轮专题复习——铜的氧化物的性质【选择精编26题】课时1 金属矿物的开发利用——A学习区 夯实基础(人教版必修2)课时1 金属矿物的开发利用——A学习区 夯实基础(人教版(2019)第二册)陕西省宝鸡中学2019-2020学年高一下学期期中考试化学试题必修第二册RJ第八章 第一节 课时1 金属矿物的开发利用(已下线)3.3 用途广泛的金属材料(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)江苏省盐城市东台创新高级中学2021-2022学年高一4月份月检测化学试题(苏教版2019)必修第二册专题9 金属与人类文明 第一单元 金属的冶炼方法(已下线)第25讲 金属矿物的开发利用(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
12-13高三上·陕西咸阳·期末
8 . 有一铁粉和氧化铜的混合物6.96g,进行如下实验:
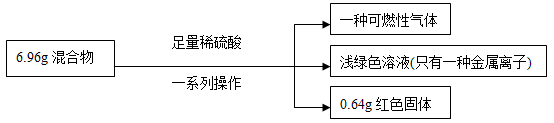
根据实验所得数据,关于混合物相关说法正确的是

根据实验所得数据,关于混合物相关说法正确的是
| A.生成气体质量为0.2g |
| B.原混合物中铁的质量分数无法计算 |
| C.实验中反应的H2SO4质量为10.78g |
| D.原混合物中铜元素的质量不一定为0.64g |
您最近一年使用:0次
10-11高三上·江苏南京·阶段练习
9 . 硫酸铜是一种重要的化工原料,工业上常用硫酸为原料来制备硫酸铜。
(1)工业上生产硫酸过程中,焙烧硫铁矿时产生的废渣是一种二次资源。
①为了从废渣中磁选获得品位合格的铁精矿,高温下利用CO使弱磁性Fe2O3转化为强磁性Fe3O4。写出该反应的化学方程式_________ ;实验发现:CO太多或太少都会导致磁铁矿产率降低,原因是___________ 。
②氯化焙烧工艺是将废渣用氯化钙水溶液调和、成球、高温焙烧,废渣中SiO2与CaCl2等在高温下反应放出HCl,HCl与金属氧化物等反应生成氯化物。反应生成的各金属氯化物以气态形式逸出,进而回收有色金属和回返氯化钙溶液。写出氯化焙烧工艺中生成HCl的化学方程式______________________ 。
(2)测定硫酸铜晶体中结晶水含量的实验步骤为:
步骤1:准确称量一个洁净、干燥的坩埚;
步骤2:将一定量的硫酸铜晶体试样研细后,放入坩埚中称重
步骤3:将盛有试样的坩埚加热,待晶体变成白色粉末时,停止加热;
步骤4:将步骤3中的坩埚放入干燥器,冷却至室温后,称重:
步骤5:_________________ ;
步骤6:根据实验数据计算硫酸铜晶体试样中结晶水的质量分数。
请完成实验步骤5。
(3)已知硫酸铜晶体受热可以逐步失去结晶水,温度升高还可以分解生成铜的氧化物。现取25.0g CuSO4·5H2O晶体均匀受热,缓慢升温至1200℃并恒温1小时,实验测得固体残留率(剩余固体的质量/原始固体质量)与温度的关系如下图所示:

在110℃时所得固体的成分为________________ ;在1200℃并恒温1小时,反应所得气态产物除去水后,物质的量为_______________ 。(填字母)
(1)工业上生产硫酸过程中,焙烧硫铁矿时产生的废渣是一种二次资源。
①为了从废渣中磁选获得品位合格的铁精矿,高温下利用CO使弱磁性Fe2O3转化为强磁性Fe3O4。写出该反应的化学方程式
②氯化焙烧工艺是将废渣用氯化钙水溶液调和、成球、高温焙烧,废渣中SiO2与CaCl2等在高温下反应放出HCl,HCl与金属氧化物等反应生成氯化物。反应生成的各金属氯化物以气态形式逸出,进而回收有色金属和回返氯化钙溶液。写出氯化焙烧工艺中生成HCl的化学方程式
(2)测定硫酸铜晶体中结晶水含量的实验步骤为:
步骤1:准确称量一个洁净、干燥的坩埚;
步骤2:将一定量的硫酸铜晶体试样研细后,放入坩埚中称重
步骤3:将盛有试样的坩埚加热,待晶体变成白色粉末时,停止加热;
步骤4:将步骤3中的坩埚放入干燥器,冷却至室温后,称重:
步骤5:
步骤6:根据实验数据计算硫酸铜晶体试样中结晶水的质量分数。
请完成实验步骤5。
(3)已知硫酸铜晶体受热可以逐步失去结晶水,温度升高还可以分解生成铜的氧化物。现取25.0g CuSO4·5H2O晶体均匀受热,缓慢升温至1200℃并恒温1小时,实验测得固体残留率(剩余固体的质量/原始固体质量)与温度的关系如下图所示:

在110℃时所得固体的成分为
| A.0 mol | B.0.1mol | C.0.125mol | D.大于0.125mol |
您最近一年使用:0次
10 . 把质量为mg的铜丝灼烧变成黑色,立即放入下列物质中,使铜丝变成红色,而且质量仍为mg的是
| A.稀H2SO4 | B.C2H5OH | C.CH3COOH溶液 | D.CO |
您最近一年使用:0次
2016-12-09更新
|
1018次组卷
|
4卷引用:江苏省南京市燕子矶中学2016-2017学年高一5月月考化学试题
江苏省南京市燕子矶中学2016-2017学年高一5月月考化学试题(已下线)2010年山东省聊城四中高二第二学期期末考试化学试题(已下线)2010年内蒙古通辽一中高一下学期期末考试化学试题河北省唐山市开滦第一中学2016-2017学年高一6月月考化学试题



