1 . 某无色透明溶液中可能大量含有 、
、 、
、 、
、 、
、 、
、 中的若干种,现对其进行如下实验:
中的若干种,现对其进行如下实验:
i:取少量该溶液,加入过量 溶液,产生白色沉淀,过滤;
溶液,产生白色沉淀,过滤;
ii:向i中所得沉淀中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
iii:向i中所得滤液中加入足量硝酸酸化后,再加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
回答下列问题:
(1)无需实验即可推断溶液中一定不会大量存在的离子为___________ 。
(2)通过实验i可知溶液中一定不会大量存在的离子为___________ 。
(3)由实验ii可知溶液中一定不会大量存在的离子为___________ 。
(4)由上述实验得到结论:该溶液一定大量存在的离子为___________ ,可能大量存在的离子为___________ 。
(5)写出实验ii中沉淀溶解的离子方程式___________ 。
 、
、 、
、 、
、 、
、 、
、 中的若干种,现对其进行如下实验:
中的若干种,现对其进行如下实验:i:取少量该溶液,加入过量
 溶液,产生白色沉淀,过滤;
溶液,产生白色沉淀,过滤;ii:向i中所得沉淀中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
iii:向i中所得滤液中加入足量硝酸酸化后,再加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。回答下列问题:
(1)无需实验即可推断溶液中一定不会大量存在的离子为
(2)通过实验i可知溶液中一定不会大量存在的离子为
(3)由实验ii可知溶液中一定不会大量存在的离子为
(4)由上述实验得到结论:该溶液一定大量存在的离子为
(5)写出实验ii中沉淀溶解的离子方程式
您最近一年使用:0次
名校
2 . 下列除杂方法正确的是
| 选项 | 物质(杂质) | 除杂方法 |
| A | 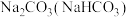 | 加热至恒重 |
| B |  | 加入足量稀盐酸,过滤 |
| C | 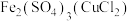 | 加入足量铁粉,过滤 |
| D | 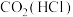 | 用饱和 溶液洗气 溶液洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-01更新
|
476次组卷
|
3卷引用:河北省邢台市质检联盟2023-2024学年高一上学期11月月考化学试题
2023高三·全国·专题练习
3 . 某小组同学取含有少量CuO杂质的Cu2O样品进行如下实验,以测定氧化亚铜的纯度。
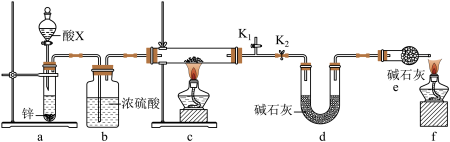
(1)装置a中所加的酸X是___________ (填化学式)。
(2)通过测定下列物理量,能达到实验目的的是___________(填字母)。
(3)熄灭酒精灯之后,仍需通一段时间H2至硬质玻璃管冷却,原因是___________ 。

(1)装置a中所加的酸X是
(2)通过测定下列物理量,能达到实验目的的是___________(填字母)。
| A.反应前后装置a的质量 |
| B.充分反应后装置c所得固体的质量 |
| C.反应前后装置d的质量 |
| D.反应前后装置e的质量 |
(3)熄灭酒精灯之后,仍需通一段时间H2至硬质玻璃管冷却,原因是
您最近一年使用:0次
解题方法
4 . CuCl常用作催化剂、杀菌剂、媒染剂、脱色剂和冶金工业等。实验室用如下装置(夹持仪器略去)将二氧化硫通入新制 悬浊液中制备CuCl(已知CuCl为白色固体,难溶于水和乙醇)。
悬浊液中制备CuCl(已知CuCl为白色固体,难溶于水和乙醇)。
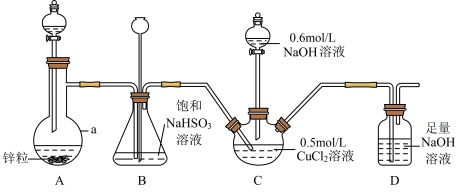
请回答下列问题:
(1)仪器a的名称是_______ ,装置A中分液漏斗中盛装的试剂为_______ 。
(2)装置B的作用是_______ 。
(3)装置D的作用是_______ ,其中发生反应的离子方程式为_______ 。
(4) 与装置C中生成的
与装置C中生成的 悬浊液反应制备CuCl的离子方程式为
悬浊液反应制备CuCl的离子方程式为_______ 。
(5)装置C中 溶液的体积为20mL,滴入足量NaOH溶液后再通入
溶液的体积为20mL,滴入足量NaOH溶液后再通入 ,反应结束后,将装置C中混合物过滤,依次用水和乙醇洗涤、烘干,得到固体的质量为0.693g。
,反应结束后,将装置C中混合物过滤,依次用水和乙醇洗涤、烘干,得到固体的质量为0.693g。
①先用水洗再用乙醇洗涤的目的是_______ 。
②该实验所得CuCl的产率为_______ %。
 悬浊液中制备CuCl(已知CuCl为白色固体,难溶于水和乙醇)。
悬浊液中制备CuCl(已知CuCl为白色固体,难溶于水和乙醇)。
请回答下列问题:
(1)仪器a的名称是
(2)装置B的作用是
(3)装置D的作用是
(4)
 与装置C中生成的
与装置C中生成的 悬浊液反应制备CuCl的离子方程式为
悬浊液反应制备CuCl的离子方程式为(5)装置C中
 溶液的体积为20mL,滴入足量NaOH溶液后再通入
溶液的体积为20mL,滴入足量NaOH溶液后再通入 ,反应结束后,将装置C中混合物过滤,依次用水和乙醇洗涤、烘干,得到固体的质量为0.693g。
,反应结束后,将装置C中混合物过滤,依次用水和乙醇洗涤、烘干,得到固体的质量为0.693g。①先用水洗再用乙醇洗涤的目的是
②该实验所得CuCl的产率为
您最近一年使用:0次
解题方法
5 . 下列各组离子在同一溶液中一定能大量共存的是
A.含大量Ba2+的溶液中:Cl-、K+、 、 、 |
B.含大量H+的溶液中:Mg2+、Na+、 、 、 |
C.含大量OH-的溶液中:K+、 、 、 、Cu2+ 、Cu2+ |
D.含大量Na+的溶液中:H+、K+、 、 、 |
您最近一年使用:0次
2023-11-26更新
|
74次组卷
|
2卷引用:江西省南昌市南钢学校2023-2024学年高一上学期期中考试化学试卷
6 . 下图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程。
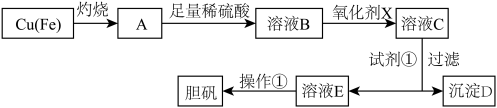
部分正离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)铜原子的价电子排布式为___________ 。
(2)若恰好完全沉淀时, 的浓度为
的浓度为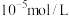 ,则常温下氢氧化铜的
,则常温下氢氧化铜的
___________ (用科学计数法表示)。
(3)溶液B中含有的金属离子有___________ (填离子符号)。
(4)下列物质中可以做氧化剂X的是___________(不定项)。
(5)试剂①可通过调节pH除去 。沉淀D的化学式为
。沉淀D的化学式为___________ ,试剂①可以选择___________ (填化学式),操作时需控制pH值的范围为___________ 。
(6)写出实验室配制 溶液的方法:
溶液的方法:___________ 。
(7)溶液E经过操作①可得到胆矾,操作①为___________ 、___________ 、过滤、洗涤、干燥。

部分正离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |  |  |  |
| 开始沉淀 | 2.7 | 7.5 | 4.4 |
| 完全沉淀 | 3.7 | 9.7 | 6.7 |
(1)铜原子的价电子排布式为
(2)若恰好完全沉淀时,
 的浓度为
的浓度为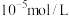 ,则常温下氢氧化铜的
,则常温下氢氧化铜的
(3)溶液B中含有的金属离子有
(4)下列物质中可以做氧化剂X的是___________(不定项)。
A. | B. | C. | D.氧气 |
(5)试剂①可通过调节pH除去
 。沉淀D的化学式为
。沉淀D的化学式为(6)写出实验室配制
 溶液的方法:
溶液的方法:(7)溶液E经过操作①可得到胆矾,操作①为
您最近一年使用:0次
7 . 2022年央视春晚的节目《只此青绿》,提到了颜料石绿{铜绿,又名孔雀石,主要成分是碱式碳酸铜[Cu2(OH)2CO3]}。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:
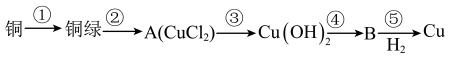
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:___________ 。
(2)将绿豆大小的金属钠投入盛有A溶液的烧杯中,溶液中出现蓝色絮状沉淀,振荡摇匀即为悬浊液,悬浊液与溶液的本质区别是___________ 。若投入的钠块比较大,可能会出现黑色固体,其成分是___________ 。
(3)A、B在无色火焰上灼烧时,其焰色为________ 色,该原理是_______ (填“物理”或“化学”)变化。
(4)完成步骤②和③可选用的试剂分别为___________ 、___________ 。(填标号)
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
写出CuCl2在水溶液中的电离方程式:___________ 。

(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:
(2)将绿豆大小的金属钠投入盛有A溶液的烧杯中,溶液中出现蓝色絮状沉淀,振荡摇匀即为悬浊液,悬浊液与溶液的本质区别是
(3)A、B在无色火焰上灼烧时,其焰色为
(4)完成步骤②和③可选用的试剂分别为
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
写出CuCl2在水溶液中的电离方程式:
您最近一年使用:0次
8 . 钠及其化合物的生产、应用,是化工生产与研究的重要组成部分。
(1) 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:

①生成 的化学方程式是
的化学方程式是_______ 。
② 样品加水溶解的化学方程式为
样品加水溶解的化学方程式为_______ ,样液中加入 后产生
后产生 ,说明
,说明 与水反应的过程中生成了
与水反应的过程中生成了_______ (填化学式)。
③滤液中加入 溶液产生白色沉淀,说明
溶液产生白色沉淀,说明 样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为
样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为_______ 。
(2)工业上以侯氏制碱法为基础生产焦亚硫酸钠( ,能溶于水)的工艺流程如图:
,能溶于水)的工艺流程如图:
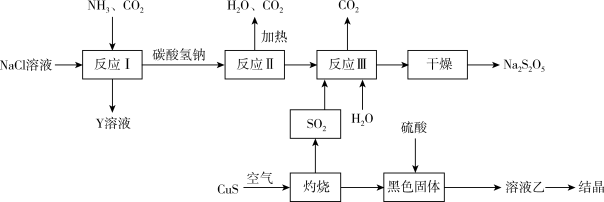
①反应Ⅱ的化学方程式为_______ 。
②关于该流程,下列说法正确的是_______ (填字母)
A.反应Ⅰ属于氧化还原反应 B.该流程中, 可以循环使用
可以循环使用
C.反应Ⅰ中应先通入 ,再通入
,再通入 D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体
D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体
(3) 在空气中灼烧的化学方程式为
在空气中灼烧的化学方程式为_______ 。
(1)
 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:
①生成
 的化学方程式是
的化学方程式是②
 样品加水溶解的化学方程式为
样品加水溶解的化学方程式为 后产生
后产生 ,说明
,说明 与水反应的过程中生成了
与水反应的过程中生成了③滤液中加入
 溶液产生白色沉淀,说明
溶液产生白色沉淀,说明 样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为
样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为(2)工业上以侯氏制碱法为基础生产焦亚硫酸钠(
 ,能溶于水)的工艺流程如图:
,能溶于水)的工艺流程如图:
①反应Ⅱ的化学方程式为
②关于该流程,下列说法正确的是
A.反应Ⅰ属于氧化还原反应 B.该流程中,
 可以循环使用
可以循环使用C.反应Ⅰ中应先通入
 ,再通入
,再通入 D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体
D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体(3)
 在空气中灼烧的化学方程式为
在空气中灼烧的化学方程式为
您最近一年使用:0次
2023-11-14更新
|
261次组卷
|
2卷引用:重庆市第十一中学校2023-2024学年高一上学期期中考试化学试题
名校
解题方法
9 . 已知:①铜矿石中含有Cu2(OH)2CO3及含铁元素的杂质;
②黄铵铁矾化学式为(NH4)xFey(SO4)m(OH)n,其中铁为+3价;黄铵铁矾可完全溶于盐酸中;
③Fe(OH)3受热易分解为Fe2O3。
某兴趣小组利用该铜矿石制黄铵铁矾的流程如图_______ mol。
(2)黄铵铁矾化学式中x、y、m、n之间的等量关系式是_______ 。
(3)该小组为测定黄铵铁矾的组成,进行了如下实验:
a.称取Wg样品,加盐酸完全溶解后,向其中加入足量NaOH溶液并加热,收集到标准状况下560.0mL的气体(假设气体全部逸出)。将所得沉淀过滤、洗涤、灼烧至恒重,得到红棕色粉末6.000g。
b.再称取Wg样品,加盐酸完全溶解后,向其中加入足量BaCl2溶液充分反应后,过滤、洗涤、干燥得沉淀11.65g。
①由实验a可计算Wg样品中n(Fe3+)=_______ mol,如何检验实验a中沉淀是否洗涤干净?_______ 。由实验b可计算Wg样品中n( )=
)=_______ mol。
②黄铵铁矾的化学式为_______ 。
②黄铵铁矾化学式为(NH4)xFey(SO4)m(OH)n,其中铁为+3价;黄铵铁矾可完全溶于盐酸中;
③Fe(OH)3受热易分解为Fe2O3。
某兴趣小组利用该铜矿石制黄铵铁矾的流程如图

(2)黄铵铁矾化学式中x、y、m、n之间的等量关系式是
(3)该小组为测定黄铵铁矾的组成,进行了如下实验:
a.称取Wg样品,加盐酸完全溶解后,向其中加入足量NaOH溶液并加热,收集到标准状况下560.0mL的气体(假设气体全部逸出)。将所得沉淀过滤、洗涤、灼烧至恒重,得到红棕色粉末6.000g。
b.再称取Wg样品,加盐酸完全溶解后,向其中加入足量BaCl2溶液充分反应后,过滤、洗涤、干燥得沉淀11.65g。
①由实验a可计算Wg样品中n(Fe3+)=
 )=
)=②黄铵铁矾的化学式为
您最近一年使用:0次
名校
解题方法
10 . 某无色透明溶液中可能大量存在Ag+、Mg2+、Fe3+、Cu2+中的一种或几种。请回答下列问题:
(1)不用做任何实验就可以肯定溶液中不存在的离子是___________
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是___________ ,有关反应的离子方程式为___________
(3)取(2)的滤液加入过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是___________ ,生成沉淀的离子方程式为___________
(4)原溶液中可能大量存在的阴离子是___________ (填序号)。
A.Cl- B. C.OH-
C.OH-
(1)不用做任何实验就可以肯定溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
(3)取(2)的滤液加入过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是
(4)原溶液中可能大量存在的阴离子是
A.Cl- B.
 C.OH-
C.OH-
您最近一年使用:0次



