解题方法
1 . 下列装置不能达到相应实验目的的是
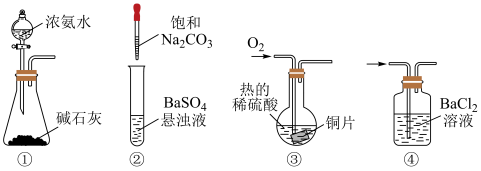

| A.装置①用于制备氨气 |
B.装置②用于验证 可转化为 可转化为 |
C.装置③可用铜制 溶液 溶液 |
D.装置④用于检验 中是否含有 中是否含有 |
您最近一年使用:0次
2 . 由实验操作和现象,可得出相应正确结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将浓硫酸与乙醇混合加热产生的气体通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色 | 产生的气体为乙烯 |
| B | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的Cu(OH)2悬浊液 | 无砖红色沉淀 | 蔗糖未发生水解 |
| C | 将苯与液溴在铁催化下生成的气体通入硝酸银溶液中 | 硝酸银溶液产生淡黄色沉淀 | 苯和液溴发生取代反应 |
| D | 检验乙醇中是否含有水 | 将少量的乙醇样品滴在无水硫酸铜上,固体变蓝 | 乙醇中含有水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 部分含铜物质的价类关系如图所示。下列说法正确的是
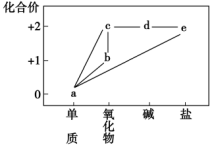

A.a能与FeCl3溶液反应: |
| B.b在酸性环境中可以转化为a和e |
| C.c经一步反应可转化为d |
D.若e为Cu(NO3)2,则其水溶液中可能大量存在H+、 、Fe2+ 、Fe2+ |
您最近一年使用:0次
2023-01-12更新
|
235次组卷
|
2卷引用:山东省滕州市2022-2023学年高三上学期期末质量检测化学试题
4 . 下列各选项中,不能满足如图转化关系的是
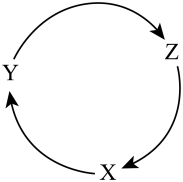

| X | Y | Z | |
| A | CuSO4 | Cu(OH)2 | Cu2O |
| B | CO2 | Na2CO3 | NaHCO3 |
| C | CH3CH2OH | CH3CHO | CH3COOH |
| D | Fe | FeCl3 | Fe(OH)3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-11更新
|
150次组卷
|
2卷引用:山东省日照市2022-2023学年高三上学期期末校际考试化学试题
名校
解题方法
5 . 硫酸四氨合铜晶体([Cu(NH3)4]SO4·H2O)常用作杀虫剂,媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。常温下该物质溶于水,不溶于乙醇、乙醚,在空气中不稳定,受热时易发生分解。某化学兴趣小组以Cu粉、3mol·L-1的硫酸、浓氨水、10%NaOH溶液、95%的乙醇溶液、0.500mol·L-1稀盐酸、0.500mol·L-1的NaOH溶液来合成硫酸四氨合铜晶体并测定其纯度。
I.CuSO4溶液的制备
①称取4g铜粉,在坩埚中灼烧10分钟并不断搅拌,放置冷却。
②在蒸发皿中加入30mL 3mol·L-1的硫酸,将坩埚中固体慢慢放入其中,加热并不断搅拌。
③趁热过滤得蓝色溶液。
(1)某同学在实验中有1.5g的铜粉剩余,该同学将制得的CuSO4溶液倒入另一蒸发皿中加热浓缩至有晶膜出现,冷却析出的晶体中含有白色粉末,试解释其原因___________ 。
Ⅱ.晶体的制备
将上述制备的CuSO4溶液按如图所示进行操作:
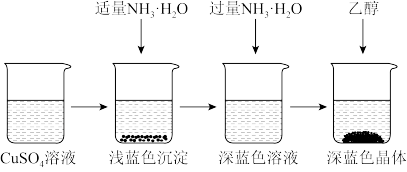
(2)已知浅蓝色沉淀的成分为Cu2(OH)2SO4,试写出生成此沉淀的离子反应方程式___________ 。
(3)析出晶体时采用加入乙醇的方法,而不是浓缩结晶的原因是___________ 。
Ⅲ.氨含量的测定
精确称取mg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入VmL 10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用V1mL C1mol·L-1的盐酸标准溶液完全吸收。取下接收瓶,用C2mol·L-1NaOH标准溶液滴定过剩的HCl(选用甲基橙作指示剂),到终点时消耗V2mL NaOH溶液。
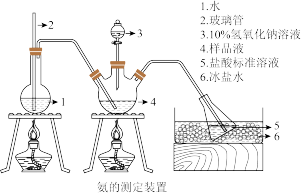
(4)玻璃管2的作用是___________ ,样品中氨的质量分数的表达式___________ 。
(5)下列实验操作可能使氨含量测定结果偏低的原因是___________ (填序号)。
A.滴定时未用NaOH标准溶液润洗滴定管
B.读数时,滴定前平视,滴定后俯视
C.滴定过程中选用酚酞作指示剂
D.取下接收瓶前,未用蒸馏水冲洗插入接收瓶中的导管外壁。
I.CuSO4溶液的制备
①称取4g铜粉,在坩埚中灼烧10分钟并不断搅拌,放置冷却。
②在蒸发皿中加入30mL 3mol·L-1的硫酸,将坩埚中固体慢慢放入其中,加热并不断搅拌。
③趁热过滤得蓝色溶液。
(1)某同学在实验中有1.5g的铜粉剩余,该同学将制得的CuSO4溶液倒入另一蒸发皿中加热浓缩至有晶膜出现,冷却析出的晶体中含有白色粉末,试解释其原因
Ⅱ.晶体的制备
将上述制备的CuSO4溶液按如图所示进行操作:

(2)已知浅蓝色沉淀的成分为Cu2(OH)2SO4,试写出生成此沉淀的离子反应方程式
(3)析出晶体时采用加入乙醇的方法,而不是浓缩结晶的原因是
Ⅲ.氨含量的测定
精确称取mg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入VmL 10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用V1mL C1mol·L-1的盐酸标准溶液完全吸收。取下接收瓶,用C2mol·L-1NaOH标准溶液滴定过剩的HCl(选用甲基橙作指示剂),到终点时消耗V2mL NaOH溶液。

(4)玻璃管2的作用是
(5)下列实验操作可能使氨含量测定结果偏低的原因是
A.滴定时未用NaOH标准溶液润洗滴定管
B.读数时,滴定前平视,滴定后俯视
C.滴定过程中选用酚酞作指示剂
D.取下接收瓶前,未用蒸馏水冲洗插入接收瓶中的导管外壁。
您最近一年使用:0次
解题方法
6 . 某企业以辉铜矿为原料生产碱式碳酸铜,工艺流程如图所示:
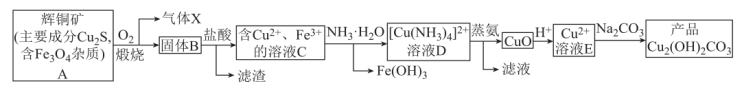
已知:Cu(OH)2溶于氨水形成[Cu(NH3)4]2+,根据以上流程,下列说法错误的是

已知:Cu(OH)2溶于氨水形成[Cu(NH3)4]2+,根据以上流程,下列说法错误的是
A.煅烧生成的气体X为 |
| B.为实现溶液C到溶液D的转化,加入过量的NH3•H2O后过滤即可 |
C.蒸氨过程总反应方程式为[Cu(NH3)4]Cl2+H2O CuO+2HCl↑+4NH3↑ CuO+2HCl↑+4NH3↑ |
| D.溶液E与碳酸钠的混合比例及方式(加入顺序)不影响产品成分 |
您最近一年使用:0次
名校
7 . 某同学通过如下流程制备氧化亚铜:
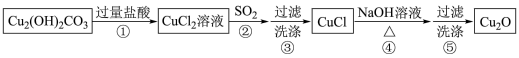
已知:CuCl难溶于水和稀硫酸;Cu2O+2H+=Cu2++Cu+H2O。下列说法错误的是
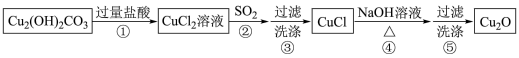
已知:CuCl难溶于水和稀硫酸;Cu2O+2H+=Cu2++Cu+H2O。下列说法错误的是
| A.步骤②中,SO2为还原剂,将CuCl2还原为CuCl |
| B.步骤③中为防止CuCl被氧化,可用H2SO3水溶液洗涤 |
| C.步骤④发生反应的离子方程式为2CuCl+2OH-=Cu2O+2Cl-+H2O |
| D.得到的Cu2O试样中可能会混有CuCl杂质,可通过加足量稀硫酸充分溶解过滤后分离除去 |
您最近一年使用:0次
2020-09-28更新
|
508次组卷
|
5卷引用:山东泰安市2021届高三上学期期末考试化学试题
山东泰安市2021届高三上学期期末考试化学试题山东省济南市商河县第一中学2021届高三上学期阶段性考试化学试题河南省洛阳市2021届高三上学期期中考试化学试题河南通许县第一高级中学2021届高三上学期第一次月考化学试题(已下线)易错21 化学工艺流程类选择题-备战2021年高考化学一轮复习易错题
名校
解题方法
8 . 废旧印刷电路板是一种电子废弃物,某科研小组设计如下工艺流程回收铜并制取胆矾(流程中RH为萃取剂),下列说法正确的是
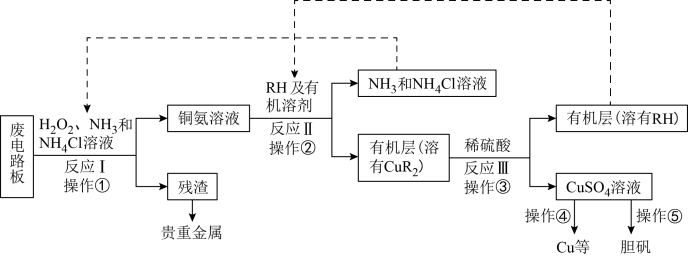

A.反应I的离子方程式为:Cu+H2O2+2NH3+2 ==Cu(NH3) ==Cu(NH3)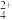 +2H2O +2H2O |
| B.操作②用到的主要仪器为蒸馏烧瓶 |
| C.操作④以石墨为电极电解硫酸铜溶液:阳极产物为O2和H2SO4 |
| D.操作⑤为:蒸发浓缩、冷却结晶、过滤、热水洗涤、干燥 |
您最近一年使用:0次
2020-02-14更新
|
322次组卷
|
5卷引用:山东省青岛市2020届高三上学期期末考试化学试题
名校
9 . CuCl是应用广泛的有机合成催化剂,可从黄铜矿(主要成分为CuFeS2)中制取。
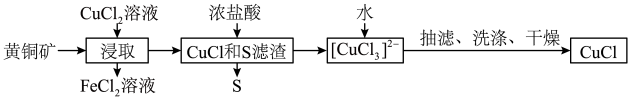
已知:CuCl是一种白色粉末,微溶于水,难溶于乙醇,在空气中易被氧化,在水溶液中存在平衡:CuCl(s)+2Cl-(aq) [CuCl3]2-(aq)(无色溶液)
[CuCl3]2-(aq)(无色溶液)
下列叙述错误的是( )

已知:CuCl是一种白色粉末,微溶于水,难溶于乙醇,在空气中易被氧化,在水溶液中存在平衡:CuCl(s)+2Cl-(aq)
 [CuCl3]2-(aq)(无色溶液)
[CuCl3]2-(aq)(无色溶液)下列叙述错误的是( )
| A.浸取中的主要反应为CuFeS2+3CuCl2=4CuCl+FeCl2+2S |
| B.浸取所得到的FeCl2溶液,可用来腐蚀覆在绝缘板上的铜箔制造印刷电路板 |
C.加水有利于CuCl(s)+2Cl(aq)- [CuCl3]2-(aq)平衡逆向移动,析出CuCl [CuCl3]2-(aq)平衡逆向移动,析出CuCl |
| D.为提高产率和纯度,可采用乙醇洗涤、真空干燥 |
您最近一年使用:0次
2019-11-13更新
|
282次组卷
|
2卷引用:山东省潍坊昌乐县第二中学2020届高三上学期期末化学模拟试题二
10 . 氧化亚铜是大型水面舰艇防护涂层的重要原料.某小组通过查阅资料,进行如图研究.

I.Cu2O的制取
(1)葡萄糖还原法制Cu2O的化学方程式为____________
(2)实验室用此方法制取并获得少量Cu2O固体,需要的玻璃仪器除试管、酒精灯、烧杯外,还需要____________
Ⅱ.检验样品中是否含有CuO
方案1:将制得的Cu2O样品溶于足量稀硫酸.
(3)甲同学认为若溶液变为蓝色,则说明样品中含有CuO杂质.乙同学认为此推论不合理,用化学用语解释原因_____________
(4)甲同学通过反思,认为将定性检验改为定量测定便能确定样品中是否含有CuO杂质,应测量的数据是________________
方案2:丙同学认为采用如下装置(所加药品均足量)进行实验,通过测定c装置反应后固体的质量以及d装置反应前后增重的质量,可计算,从而确定样品中是否含有氧化铜.
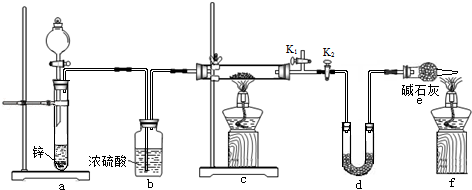
(5)装置a中所加的酸是__________
(填化学式),装置e中碱石灰的作用是_______________
(6)点燃装置c中酒精灯之前需进行的操作是_________________
(7)熄灭酒精灯之后,仍需通一段时间H2至试管冷却,原因是_______________ .

I.Cu2O的制取
(1)葡萄糖还原法制Cu2O的化学方程式为
(2)实验室用此方法制取并获得少量Cu2O固体,需要的玻璃仪器除试管、酒精灯、烧杯外,还需要
Ⅱ.检验样品中是否含有CuO
方案1:将制得的Cu2O样品溶于足量稀硫酸.
(3)甲同学认为若溶液变为蓝色,则说明样品中含有CuO杂质.乙同学认为此推论不合理,用化学用语解释原因
(4)甲同学通过反思,认为将定性检验改为定量测定便能确定样品中是否含有CuO杂质,应测量的数据是
方案2:丙同学认为采用如下装置(所加药品均足量)进行实验,通过测定c装置反应后固体的质量以及d装置反应前后增重的质量,可计算,从而确定样品中是否含有氧化铜.

(5)装置a中所加的酸是
(填化学式),装置e中碱石灰的作用是
(6)点燃装置c中酒精灯之前需进行的操作是
(7)熄灭酒精灯之后,仍需通一段时间H2至试管冷却,原因是
您最近一年使用:0次
2016-12-09更新
|
382次组卷
|
2卷引用:2016届山东省枣庄市滕州五中高三上学期期末化学试卷



