1 . 下图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程。
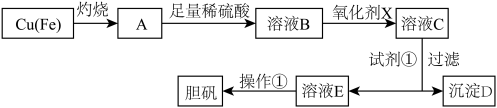
部分正离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)铜原子的价电子排布式为___________ 。
(2)若恰好完全沉淀时, 的浓度为
的浓度为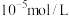 ,则常温下氢氧化铜的
,则常温下氢氧化铜的
___________ (用科学计数法表示)。
(3)溶液B中含有的金属离子有___________ (填离子符号)。
(4)下列物质中可以做氧化剂X的是___________(不定项)。
(5)试剂①可通过调节pH除去 。沉淀D的化学式为
。沉淀D的化学式为___________ ,试剂①可以选择___________ (填化学式),操作时需控制pH值的范围为___________ 。
(6)写出实验室配制 溶液的方法:
溶液的方法:___________ 。
(7)溶液E经过操作①可得到胆矾,操作①为___________ 、___________ 、过滤、洗涤、干燥。

部分正离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |  |  |  |
| 开始沉淀 | 2.7 | 7.5 | 4.4 |
| 完全沉淀 | 3.7 | 9.7 | 6.7 |
(1)铜原子的价电子排布式为
(2)若恰好完全沉淀时,
 的浓度为
的浓度为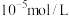 ,则常温下氢氧化铜的
,则常温下氢氧化铜的
(3)溶液B中含有的金属离子有
(4)下列物质中可以做氧化剂X的是___________(不定项)。
A. | B. | C. | D.氧气 |
(5)试剂①可通过调节pH除去
 。沉淀D的化学式为
。沉淀D的化学式为(6)写出实验室配制
 溶液的方法:
溶液的方法:(7)溶液E经过操作①可得到胆矾,操作①为
您最近一年使用:0次
名校
解题方法
2 . 足量C(s)与H2O(g)反应生成1mol H2(g)和1mol CO(g)时,吸收131.3kJ的热量,该反应可用于制取水煤气;下列化学反应表示正确的是
A.制取水煤气的热化学方程式: 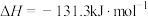 |
B.高温下甲烷还原氧化铜: |
C.乙酸除水垢: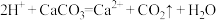 |
D.CaC2与水反应: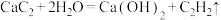 |
您最近一年使用:0次
2023-10-17更新
|
225次组卷
|
3卷引用:江西省广丰中学2023-2024学年高二上学期10月月考化学试题
3 . 随着现代工业的发展,人类生活水平的提高,生活中产生的废铜合金垃圾越来越多,为了变废为宝,工业上一种利用废铜合金(主要成分:Cu、Fe、Al的单质及少量氧化物)制备胆矾( )的流程如下:
)的流程如下:
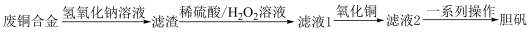
回答下列问题:
(1)废铜合金在反应前需要粉碎,目的是___________ ,将其先溶于氢氧化钠溶液,目的是___________ ,实验室中上述四步操作都需要的玻璃仪器名称是___________ 。
(2)写出第二步中铜与稀硫酸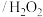 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(3)加入氧化铜的目的是除铁,检验铁离子是否除尽的试剂是___________ (填化学式)。一系列操作包括___________ 、过滤、洗涤、干燥。
(4)上述流程同时能够得到的副产品有___________ (填化学式)。若用100g废铜合金经上述转化,最后得到胆矾300g,___________ (填“能”或“不能”)据此求出废铜合金中铜元素的百分含量。
 )的流程如下:
)的流程如下: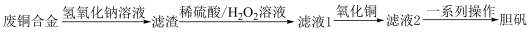
回答下列问题:
(1)废铜合金在反应前需要粉碎,目的是
(2)写出第二步中铜与稀硫酸
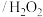 溶液反应的离子方程式:
溶液反应的离子方程式:(3)加入氧化铜的目的是除铁,检验铁离子是否除尽的试剂是
(4)上述流程同时能够得到的副产品有
您最近一年使用:0次
名校
解题方法
4 . 中华优秀传统文化涉及了很多化学知识,下列有关说法错误的是
| A.《本草纲目拾遗》中对强水的记载:“性最猛烈,能蚀五金。”强水为强电解质 |
| B.《神农本草经》中“石胆……能化铁为铜、成金银”描述的是湿法炼铜 |
| C.刘长卿诗云“水声冰下咽,砂路雪中平”,固态冰转化为液态水为熵增的过程 |
| D.“火树银花合,星桥铁锁开”中涉及化学能转化为热能和光能 |
您最近一年使用:0次
2023-10-12更新
|
741次组卷
|
5卷引用:四川省成都外国语学校2023-2024学年高二上学期10月月考化学试题
名校
5 . 成都理工大学刘兴诗教授提出了三星堆青铜器源自四川彭州龙门山的猜想并展开科考活动,经过调查初步判断,三星堆的铜来自龙门山区。经调查,上世纪80~90年代,该地利用资源优势,大规模进行冶铜及生产大量附属产品。以黄铜矿为原料生产硫酸、铁红、胆矾的流程如下:

已知:黄铜矿中 含量不高,工业上一般通过浮选除去矿石中的其他成分,得到仅含
含量不高,工业上一般通过浮选除去矿石中的其他成分,得到仅含 的
的 (Fe化合价为+2价)矿粉。
(Fe化合价为+2价)矿粉。
回答下列问题:
(1)已知信息中涉及的“浮选”过程是为了使矿石中的 含量大大增加,该过程在工业上称为矿石(元素)的
含量大大增加,该过程在工业上称为矿石(元素)的_________ 。
(2)黄铜矿粉在空气中焙烧时的化学方程式为 ,该反应中还原产物为
,该反应中还原产物为___________ ,若有标准状况下的空气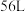 (假设空气中氧气的体积分数为
(假设空气中氧气的体积分数为 )参与反应,则反应过程中转移电子的物质的量为
)参与反应,则反应过程中转移电子的物质的量为___________ 。
(3)若在实验室环境下由固体C制得铁红,需要在___________ (填仪器名称)中进行。
(4)由气体B制硫酸的过程中,为了避免___________ ,用 的浓硫酸代替水进行气体的吸收。
的浓硫酸代替水进行气体的吸收。
(5)由固体B通过一系列操作制备 溶液的过程中,有以下四种方案:
溶液的过程中,有以下四种方案:
①固体B先在空气中充分灼烧,再用稀硫酸溶解,过滤;
②直接用浓硫酸溶解,过滤;
③边通空气边加热,在稀硫酸中溶解,过滤;
④在混酸(按一定比例混合的稀硝酸和稀硫酸)溶液中溶解,过滤;
ⅰ.方案②相对方案①,不足之处有___________ ;
ⅰ.方案③中发生反应的离子方程式为___________ ;
ⅲ.方案④中当金属和酸同时消耗完,所得溶液不含硝酸铜,则硝酸和硫酸的物质的量浓度比为___________ 时恰好满足。

已知:黄铜矿中
 含量不高,工业上一般通过浮选除去矿石中的其他成分,得到仅含
含量不高,工业上一般通过浮选除去矿石中的其他成分,得到仅含 的
的 (Fe化合价为+2价)矿粉。
(Fe化合价为+2价)矿粉。回答下列问题:
(1)已知信息中涉及的“浮选”过程是为了使矿石中的
 含量大大增加,该过程在工业上称为矿石(元素)的
含量大大增加,该过程在工业上称为矿石(元素)的(2)黄铜矿粉在空气中焙烧时的化学方程式为
 ,该反应中还原产物为
,该反应中还原产物为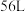 (假设空气中氧气的体积分数为
(假设空气中氧气的体积分数为 )参与反应,则反应过程中转移电子的物质的量为
)参与反应,则反应过程中转移电子的物质的量为(3)若在实验室环境下由固体C制得铁红,需要在
(4)由气体B制硫酸的过程中,为了避免
 的浓硫酸代替水进行气体的吸收。
的浓硫酸代替水进行气体的吸收。(5)由固体B通过一系列操作制备
 溶液的过程中,有以下四种方案:
溶液的过程中,有以下四种方案:①固体B先在空气中充分灼烧,再用稀硫酸溶解,过滤;
②直接用浓硫酸溶解,过滤;
③边通空气边加热,在稀硫酸中溶解,过滤;
④在混酸(按一定比例混合的稀硝酸和稀硫酸)溶液中溶解,过滤;
ⅰ.方案②相对方案①,不足之处有
ⅰ.方案③中发生反应的离子方程式为
ⅲ.方案④中当金属和酸同时消耗完,所得溶液不含硝酸铜,则硝酸和硫酸的物质的量浓度比为
您最近一年使用:0次
6 . 现对一批已生锈的弹壳进行回收利用,主要流程如下:
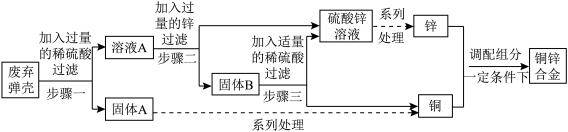
(资料)①该弹壳由铜锌合金制成,其锈的主要成分是Cu2(OH)2CO3。
②Cu2(OH)2CO3能与稀硫酸反应生成硫酸铜,其他杂质不溶于水,也不参与反应。
(1)为加快步骤一的反应速率,可采用的方法是___________ (填一种即可);
(2)溶液A中的溶质是(写化学式)___________ ;固体B含有的物质为(写化学式)___________ ;
(3)步骤三中发生反应的化学方程式为___________ ;
(4)回收锌的质量___________ 废弃弹壳中锌元素的质量(选填“大于”、“小于”或“等于”);
(5)改变铜锌合金中锌的含量可以得到不同机械性能的黄铜。现欲制备120吨(t)含锌量小于35%的黄铜,该类黄铜具有良好的塑性,能承受冷热加工,但在200℃~700℃之间热加工时易断裂。下列符合原料配比及热加工条件的是___________ (填字母序号)。
a.锌44t 铜76t 750℃ b.锌38t 铜82t 500℃
c.锌55t 铜65t 190℃ d.锌25t 铜95t 750℃

(资料)①该弹壳由铜锌合金制成,其锈的主要成分是Cu2(OH)2CO3。
②Cu2(OH)2CO3能与稀硫酸反应生成硫酸铜,其他杂质不溶于水,也不参与反应。
(1)为加快步骤一的反应速率,可采用的方法是
(2)溶液A中的溶质是(写化学式)
(3)步骤三中发生反应的化学方程式为
(4)回收锌的质量
(5)改变铜锌合金中锌的含量可以得到不同机械性能的黄铜。现欲制备120吨(t)含锌量小于35%的黄铜,该类黄铜具有良好的塑性,能承受冷热加工,但在200℃~700℃之间热加工时易断裂。下列符合原料配比及热加工条件的是
a.锌44t 铜76t 750℃ b.锌38t 铜82t 500℃
c.锌55t 铜65t 190℃ d.锌25t 铜95t 750℃
您最近一年使用:0次
7 . Ⅰ.铜与浓硝酸反应的装置如下图。

(1)仪器A的名称为_______ ,装置B的作用为_______ 。
(2)装置C中发生反应的离子方程式为_______ 。
Ⅱ.胆矾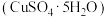 是一种重要化工原料,某研究小组以生锈的铜屑为原料[主要成分是
是一种重要化工原料,某研究小组以生锈的铜屑为原料[主要成分是 ,含有少量的油污、
,含有少量的油污、 、
、 、
、 ]制备胆矾。流程如下。
]制备胆矾。流程如下。
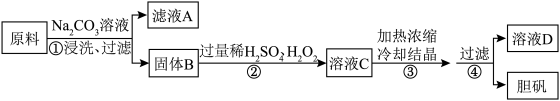
回答下列问题:
(3)“步骤①”中使用 溶液的目的是
溶液的目的是_______ 。
(4)“步骤②”中,在 存在下
存在下 溶于稀
溶于稀 ,该过程发生反应的化学方程式为
,该过程发生反应的化学方程式为_______ 。
(5)“步骤②”中,该研究小组认为仅用浓 溶解固体
溶解固体 ,也可以得到溶液
,也可以得到溶液 ,该方案的不足之处为
,该方案的不足之处为_______ 。
(6)该研究小组甲乙两名同学继续实验探究,发现溶液D能将 氧化为
氧化为 。
。
a.甲同学认为不可能是“步骤②”中过量 将
将 氧化为
氧化为 ,理由是
,理由是_______ 。
b.乙同学通过实验证实,只能是 将
将 氧化为
氧化为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。

(1)仪器A的名称为
(2)装置C中发生反应的离子方程式为
Ⅱ.胆矾
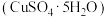 是一种重要化工原料,某研究小组以生锈的铜屑为原料[主要成分是
是一种重要化工原料,某研究小组以生锈的铜屑为原料[主要成分是 ,含有少量的油污、
,含有少量的油污、 、
、 、
、 ]制备胆矾。流程如下。
]制备胆矾。流程如下。
回答下列问题:
(3)“步骤①”中使用
 溶液的目的是
溶液的目的是(4)“步骤②”中,在
 存在下
存在下 溶于稀
溶于稀 ,该过程发生反应的化学方程式为
,该过程发生反应的化学方程式为(5)“步骤②”中,该研究小组认为仅用浓
 溶解固体
溶解固体 ,也可以得到溶液
,也可以得到溶液 ,该方案的不足之处为
,该方案的不足之处为(6)该研究小组甲乙两名同学继续实验探究,发现溶液D能将
 氧化为
氧化为 。
。a.甲同学认为不可能是“步骤②”中过量
 将
将 氧化为
氧化为 ,理由是
,理由是b.乙同学通过实验证实,只能是
 将
将 氧化为
氧化为 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
解题方法
8 . 铜的氯化物是重要的化工原料,常用作有机合成催化剂。实验室用粗铜(含杂质Fe)制备氯化亚铜、氯化铜晶体的流程如下:
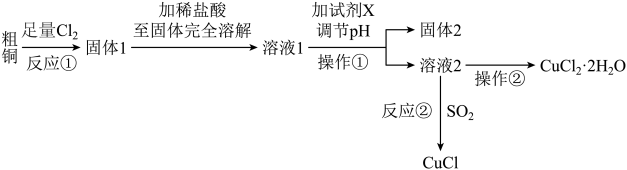
下列说法错误的是

下列说法错误的是
A.反应②的离子方程式为2Cu2++SO2+2H2O+2Cl-=2CuCl↓+SO +4H+ +4H+ |
| B.检验溶液2中的杂质离子是否除尽可以选用KSCN溶液 |
| C.试剂X可能是CuO,操作②中结晶时需要通入HCl气体 |
| D.固体1和固体2中Fe元素的价态不相同 |
您最近一年使用:0次
9 . 某研究小组探究白色难溶盐X(含五种元素,M<200 g•mol-1)的组成,进行如图实验:
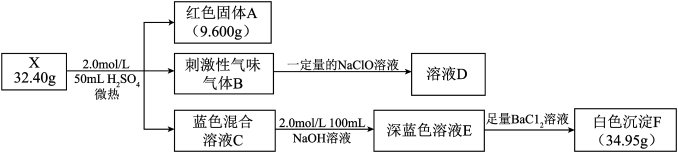
已知:固体A为常见单质:气体B能使品红褪色,实验测得气体体积为3.36L(标准状况),为防止污染环境,实验过程中用NaClO溶液吸收;溶液E中含有两种溶质,且阴离子相同。
请回答下列问题:
(1)X除含有H、O元素,还含有_________ 元素。
(2)混合溶液C中的溶质主要有_________ (填化学式)。
(3)可用气体B通入深蓝色溶液E制备X,写出相应的离子方程式________ 。
(4)设计实验方案证明吸收气体B的NaClO溶液已过量:_________ 。

已知:固体A为常见单质:气体B能使品红褪色,实验测得气体体积为3.36L(标准状况),为防止污染环境,实验过程中用NaClO溶液吸收;溶液E中含有两种溶质,且阴离子相同。
请回答下列问题:
(1)X除含有H、O元素,还含有
(2)混合溶液C中的溶质主要有
(3)可用气体B通入深蓝色溶液E制备X,写出相应的离子方程式
(4)设计实验方案证明吸收气体B的NaClO溶液已过量:
您最近一年使用:0次
名校
解题方法
10 . 金属M能与Cu(NO3)2溶液反应:M+Cu(NO3)2=Cu+M(NO3)2,下列叙述不正确的是
| A.金属M不可能是铝 |
| B.一定能发生反应:M+2AgNO3=2Ag+M(NO3)2 |
| C.若M为镁,恰好完全反应后,固体质量增大 |
| D.恰好完全反应后, M表面有红色固体析出,溶液一定由蓝色变为无色 |
您最近一年使用:0次



