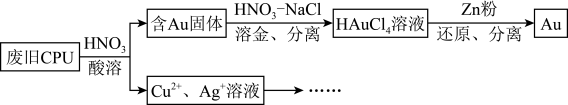
1 . 用如图方法回收废旧CPU中的单质Au(金),Ag和Cu。
(1)酸溶后经_______ 操作,将混合物分离。
(2)浓、稀 均可作酸溶试剂。溶解等量的Cu消耗
均可作酸溶试剂。溶解等量的Cu消耗 的物质的量不同,写出消耗
的物质的量不同,写出消耗 物质的量少的反应的化学方程式:
物质的量少的反应的化学方程式:_______ 。
(3)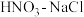 与王水[V(浓硝酸)∶V(浓盐酸)=1∶3]溶金原理相同。
与王水[V(浓硝酸)∶V(浓盐酸)=1∶3]溶金原理相同。
①将溶金反应的化学方程式补充完整:_________________ 。

②关于溶金的下列说法正确的是_______ 。
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)若用Zn粉将溶液中的1 mol HAuCl4完全还原,则参加反应的Zn的物质的量是____ mol。

(1)酸溶后经
(2)浓、稀
 均可作酸溶试剂。溶解等量的Cu消耗
均可作酸溶试剂。溶解等量的Cu消耗 的物质的量不同,写出消耗
的物质的量不同,写出消耗 物质的量少的反应的化学方程式:
物质的量少的反应的化学方程式:(3)
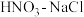 与王水[V(浓硝酸)∶V(浓盐酸)=1∶3]溶金原理相同。
与王水[V(浓硝酸)∶V(浓盐酸)=1∶3]溶金原理相同。①将溶金反应的化学方程式补充完整:

②关于溶金的下列说法正确的是
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)若用Zn粉将溶液中的1 mol HAuCl4完全还原,则参加反应的Zn的物质的量是
您最近一年使用:0次
2022-05-27更新
|
342次组卷
|
3卷引用:北京市第一六一中学2021-2022学年高一下学期期中阶段(选考班)化学试题
名校
解题方法
2 . 为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验I 反应产物的定性探究
实验装置如图所示。(固定装置已略去)
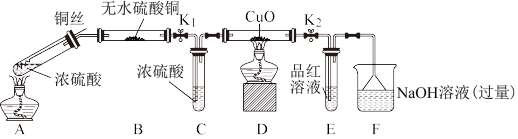
(1)A中反应的化学方程式为_______ 。
(2)无水硫酸铜的作用是:_______ 。
(3)F烧杯中的溶液通常是过量的氢氧化钠溶液,写出其发生反应的离子方程式_______ 。
(4)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是_______ 。
(5)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是_______ 。
实验II 反应产物的定量探究
(6)为测出硫酸铜的产率,将该反应所得溶液中和后配制成250.00mL溶液,取该溶液25.00mL加入足量KI溶液振荡,以淀粉溶液为指示剂,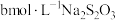 溶液滴定生成的
溶液滴定生成的 ,3次实验平均消耗该
,3次实验平均消耗该 溶液V mL。若反应消耗铜的质量为a g,则硫酸铜的产率为
溶液V mL。若反应消耗铜的质量为a g,则硫酸铜的产率为_______ 。
(已知: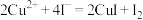 ,
, )
)
实验I 反应产物的定性探究
实验装置如图所示。(固定装置已略去)

(1)A中反应的化学方程式为
(2)无水硫酸铜的作用是:
(3)F烧杯中的溶液通常是过量的氢氧化钠溶液,写出其发生反应的离子方程式
(4)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是
(5)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是
实验II 反应产物的定量探究
(6)为测出硫酸铜的产率,将该反应所得溶液中和后配制成250.00mL溶液,取该溶液25.00mL加入足量KI溶液振荡,以淀粉溶液为指示剂,
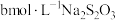 溶液滴定生成的
溶液滴定生成的 ,3次实验平均消耗该
,3次实验平均消耗该 溶液V mL。若反应消耗铜的质量为a g,则硫酸铜的产率为
溶液V mL。若反应消耗铜的质量为a g,则硫酸铜的产率为(已知:
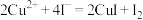 ,
, )
)
您最近一年使用:0次
名校
解题方法
3 . 某实验小组在研究硝酸与铜的反应时,发现稀硝酸和铜反应后的混合液为蓝色,而浓硝酸和铜反应后的混合液为绿色,为此对产生绿色的原因开展探究。按要求完成下列问题:
[猜想假设]
(1)假设1:___________
假设2:硝酸铜溶液中溶解了
[实验操作及现象分析]
实验一:向蒸馏水中不断加入硝酸铜晶体,最终配成饱和溶液。配制过程中溶液颜色始终是蓝色,未见绿色出现。
甲同学根据实验一的现象证明了假设1不成立,请补全假设。
实验二:
(2)甲同学在实验一的基础上继续开展了实验二,并初步验证了假设2成立,他的实验操作及现象是___________ 。
乙同学认为假设2不严谨,用以下实验对假设2进行了深入探究:
实验三:
(3)结合实验三,乙同学认为假设2不严谨的证据是___________
(4)乙同学查阅资料发现:
①铜与浓硝酸反应后溶液呈现绿色是由于 (或
(或 )与铜离子作用的结果。
)与铜离子作用的结果。
②金属和浓 的反应一旦发生后速率不断加快。原因是过程中有
的反应一旦发生后速率不断加快。原因是过程中有 生成。如
生成。如 和浓
和浓 反应,开始生成的
反应,开始生成的 溶于水形成
溶于水形成 ,它再和
,它再和 反应,速率就大大加快。
反应,速率就大大加快。
请依据资料完成以下离子反应方程式。
i.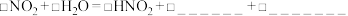 ;
;___________
ii. ;
;___________
iii.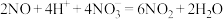
实验四:乙同学通过以下实验证实了反应过程中 的生成。
的生成。
(5)结合化学用语,解释实验3产生该现象的原因是___________ 。
[猜想假设]
(1)假设1:
假设2:硝酸铜溶液中溶解了

[实验操作及现象分析]
实验一:向蒸馏水中不断加入硝酸铜晶体,最终配成饱和溶液。配制过程中溶液颜色始终是蓝色,未见绿色出现。
甲同学根据实验一的现象证明了假设1不成立,请补全假设。
实验二:
(2)甲同学在实验一的基础上继续开展了实验二,并初步验证了假设2成立,他的实验操作及现象是
乙同学认为假设2不严谨,用以下实验对假设2进行了深入探究:
实验三:
| 操作及试剂 | 现象 |
向浓硝酸和铜反应后的混合液中通入 | 大量红棕色气体放出,短时间内溶液仍保持绿色。长时间后变成蓝色 |
(4)乙同学查阅资料发现:
①铜与浓硝酸反应后溶液呈现绿色是由于
 (或
(或 )与铜离子作用的结果。
)与铜离子作用的结果。②金属和浓
 的反应一旦发生后速率不断加快。原因是过程中有
的反应一旦发生后速率不断加快。原因是过程中有 生成。如
生成。如 和浓
和浓 反应,开始生成的
反应,开始生成的 溶于水形成
溶于水形成 ,它再和
,它再和 反应,速率就大大加快。
反应,速率就大大加快。请依据资料完成以下离子反应方程式。
i.
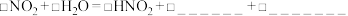 ;
;ii.
 ;
;iii.
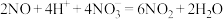
实验四:乙同学通过以下实验证实了反应过程中
 的生成。
的生成。| 实验 | 操作 | 现象 |
| 1 | 向试管a中加入lmL浓硝酸,再插入铜丝 | 快速产生红棕色气体,溶液变为绿色 |
| 2 | 向试管b中加入1mL浓硝酸,3滴蒸馏水,再插入铜丝 | 快速产生红棕色气体溶液变为绿色 |
| 3 | 向试管c中加入1mL浓硝酸,3滴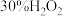 ,再插入铜丝 ,再插入铜丝 | 反应较慢,溶液变为蓝色 |
您最近一年使用:0次
2022-03-31更新
|
713次组卷
|
3卷引用:北京市房山区2022届高三一模化学试题
名校
4 . 硝酸是一种重要的化工原料。
(1)在浓硝酸中加入铜片,开始反应时有红棕色气体产生,写出发生反应的离子方程式_______ ;反应停止后,仍有铜剩余,加入20%的稀硫酸,铜片上又有气泡产生,稀硫酸的作用是_______ (填字母)。
A.还原剂 B.氧化剂 C.酸化 D.提供热能
(2)实验小组用稀硝酸和铜分别设计了甲、乙两组实验(装置如图所示,夹持仪器已略去)。
①甲组实验中,同学们观察到集气瓶中收集到无色气体。部分同学认为该实验不能确定是铜与稀硝酸反应生成了 ,因为集气瓶中无色气体的来源可能是
,因为集气瓶中无色气体的来源可能是_______ 。
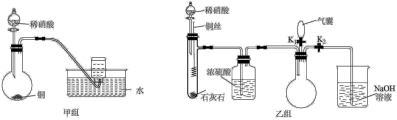
②乙组实验的操作步骤是:
a.关闭活塞 ,打开活塞
,打开活塞 ,将过量稀硝酸加入石灰石中。该操作的目的是
,将过量稀硝酸加入石灰石中。该操作的目的是_______ 。
b.待石灰石反应完全后,将铜丝插入过量稀硝酸中。
c.一段时间后,欲证明圆底烧瓶中收集列的无色气体是 ,应进行的操作是
,应进行的操作是_______ ,观察到的现象是_______ 。
(3)某些资料认为 不能与
不能与 反应。某同学提出质疑,他认为
反应。某同学提出质疑,他认为 易与
易与 发生反应,应该更容易被
发生反应,应该更容易被 氧化。
氧化。
查阅资料:a.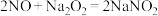 ;
;
b.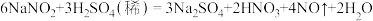
c.酸性条件下, 能被
能被 氧化生成
氧化生成 。
。
该同学在乙组实验的基础上,用如图所示装置探究 与
与 的反成。
的反成。
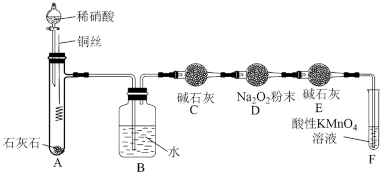
①C装置中碱石灰的作用是_______ ;F装置中反应的离子方程式为_______ 。
②充分反应后,检验D装置中是否发生反应a的实验操作及现象是_______ 。
(1)在浓硝酸中加入铜片,开始反应时有红棕色气体产生,写出发生反应的离子方程式
A.还原剂 B.氧化剂 C.酸化 D.提供热能
(2)实验小组用稀硝酸和铜分别设计了甲、乙两组实验(装置如图所示,夹持仪器已略去)。
①甲组实验中,同学们观察到集气瓶中收集到无色气体。部分同学认为该实验不能确定是铜与稀硝酸反应生成了
 ,因为集气瓶中无色气体的来源可能是
,因为集气瓶中无色气体的来源可能是
②乙组实验的操作步骤是:
a.关闭活塞
 ,打开活塞
,打开活塞 ,将过量稀硝酸加入石灰石中。该操作的目的是
,将过量稀硝酸加入石灰石中。该操作的目的是b.待石灰石反应完全后,将铜丝插入过量稀硝酸中。
c.一段时间后,欲证明圆底烧瓶中收集列的无色气体是
 ,应进行的操作是
,应进行的操作是(3)某些资料认为
 不能与
不能与 反应。某同学提出质疑,他认为
反应。某同学提出质疑,他认为 易与
易与 发生反应,应该更容易被
发生反应,应该更容易被 氧化。
氧化。查阅资料:a.
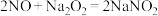 ;
;b.
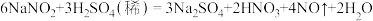
c.酸性条件下,
 能被
能被 氧化生成
氧化生成 。
。该同学在乙组实验的基础上,用如图所示装置探究
 与
与 的反成。
的反成。
①C装置中碱石灰的作用是
②充分反应后,检验D装置中是否发生反应a的实验操作及现象是
您最近一年使用:0次
2022-02-21更新
|
880次组卷
|
2卷引用:北京市第一六一中学2022-2023学年高一下学期期中考试化学试题
解题方法
5 . 某小组同学利用下面的实验装置(气密性已检验)验证稀硝酸的性质。
(1)步骤I中,红棕色气体是 ___________ 。
(2)得出结论:铜与稀硝酸反应生成NO,所依据的实验现象是____________ 。
(3)步骤II中,生成蓝色沉淀的离子方程式是___________ 。
(4)上述实验说明稀硝酸具有的性质是酸性、___________ 。
| 实验装置 | 实验步骤 | 实验现象 |
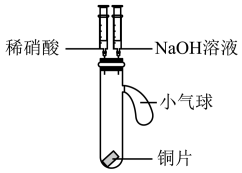 | I.向试管中加入2 mL稀硝酸 | 铜片表面产生无色气泡; 溶液逐渐变为蓝色; 试管上部气体逐渐变为红棕色 |
| II.试管上部气体变为红棕色后, 立即将NaOH溶液加入到试管中 | 溶液中产生蓝色沉淀; 试管上部气体逐渐变为无色 |
(2)得出结论:铜与稀硝酸反应生成NO,所依据的实验现象是
(3)步骤II中,生成蓝色沉淀的离子方程式是
(4)上述实验说明稀硝酸具有的性质是酸性、
您最近一年使用:0次
2021-12-25更新
|
530次组卷
|
2卷引用:2021年北京第二次普通高中学业水平合格性考试化学试题
解题方法
6 . 某同学在实验室中进行如图所示实验。

(1)铜丝与浓硝酸发生反应的离子方程式是________ 。
(2)烧杯中NaOH溶液的作用是________ 。
(3)铜丝下端弯成螺旋状的原因是________ 。
(4)根据反应产生的现象,从不同角度推断该反应所属反应类型:
①根据________ 现象,可推断该反应为氧化还原反应。
②根据反应后试管壁发热的现象,可推断该反应属于________ 反应。

(1)铜丝与浓硝酸发生反应的离子方程式是
(2)烧杯中NaOH溶液的作用是
(3)铜丝下端弯成螺旋状的原因是
(4)根据反应产生的现象,从不同角度推断该反应所属反应类型:
①根据
②根据反应后试管壁发热的现象,可推断该反应属于
您最近一年使用:0次
名校
解题方法
7 . 某校化学小组同学研究 Cu与H2SO4 溶液反应,小伟同学实验记录如下:
(1)实验一:探究白雾的成分
①波波同学收集实验Ⅰ中白雾,加入品红溶液,溶液褪色,得出结论:白雾成分包含 SO2。可能是因为局部温度过高产生,写出有关化学方程式________ 。
②艳艳同学认为不妥,补充实验Ⅲ:
根据实验Ⅲ,可推断白雾成分是______ ,而并非SO2。
(2)实验二:探究红色固体的成分。经过分析,实验Ⅰ和实验Ⅱ中的红色浑浊成分相同。
【资料】Cu2O能溶在浓氨水中形成无色Cu(NH3)2+,很容易被氧气氧化为蓝色Cu(NH3)22+;Cu2O能与一定浓度的酸溶液发生反应:Cu2O+2H+=Cu2++Cu+H2O。
①写出Cu2O溶在浓氨水中的离子方程式_______ 。
②对于红色浑浊的成分,谷哥设计实验并实施,证实了红色固体中只有Cu2O。他的实验是:将实验Ⅰ试管中固体过滤洗涤,得红色固体,__________ 。
③结合实验Ⅰ和Ⅱ,吉吉同学确定铜丝烧至红热时生成了______ 。
(3)实验三:探究红色固体不溶的原因。经过检验,实验Ⅰ和实验Ⅱ反应后的溶液均显酸性,对于体系中有Cu2O固体的原因:
龙校假设:在实验条件下,随着溶液酸性降低,Cu2O与酸无法反应。
乔博假设:在实验条件下,随着溶液酸性降低,Cu2O与酸反应速率变小。
邹邹同学继续实验:
①实验Ⅴ的目的是 ______ 。
②通过以上实验,臧臧同学得出的结论是______ 。
| 实验编号 | 实验操作 | 实验现象 |
| Ⅰ | 取螺旋状铜丝在酒精灯上烧至红热,迅速伸入装有 10 mL 3 mol/L H2SO4溶液的试管中 | 产生大量白雾;溶液颜色变为浅蓝色;试管中出现红色浑浊 |
| Ⅱ | 步骤一:取螺旋状铜丝在酒精灯上烧至红热, 迅速伸入装有10 mL蒸馏水的试管中; 步骤二:冷却后加入5 mL 3 mol/L H2SO4 | 步骤一:产生少量白雾;试管中出现黑色浑浊,略带红色 步骤二:浑浊全部为红色;溶液略显蓝色 |
①波波同学收集实验Ⅰ中白雾,加入品红溶液,溶液褪色,得出结论:白雾成分包含 SO2。可能是因为局部温度过高产生,写出有关化学方程式
②艳艳同学认为不妥,补充实验Ⅲ:
| 实验编号 | 实验操作 | 实验现象 |
| Ⅲ | 步骤一:取品红溶液,加 3 mol/L H2SO4溶液,加热; 步骤二:收集实验Ⅰ中白雾,加入品红溶液,加热 | 步骤一:溶液褪色,加热无颜色变化; 步骤二:溶液褪色,加热无颜色变化 |
(2)实验二:探究红色固体的成分。经过分析,实验Ⅰ和实验Ⅱ中的红色浑浊成分相同。
【资料】Cu2O能溶在浓氨水中形成无色Cu(NH3)2+,很容易被氧气氧化为蓝色Cu(NH3)22+;Cu2O能与一定浓度的酸溶液发生反应:Cu2O+2H+=Cu2++Cu+H2O。
①写出Cu2O溶在浓氨水中的离子方程式
②对于红色浑浊的成分,谷哥设计实验并实施,证实了红色固体中只有Cu2O。他的实验是:将实验Ⅰ试管中固体过滤洗涤,得红色固体,
③结合实验Ⅰ和Ⅱ,吉吉同学确定铜丝烧至红热时生成了
(3)实验三:探究红色固体不溶的原因。经过检验,实验Ⅰ和实验Ⅱ反应后的溶液均显酸性,对于体系中有Cu2O固体的原因:
龙校假设:在实验条件下,随着溶液酸性降低,Cu2O与酸无法反应。
乔博假设:在实验条件下,随着溶液酸性降低,Cu2O与酸反应速率变小。
邹邹同学继续实验:
| 实验编号 | 实验操作 | 实验现象 |
| Ⅳ | 取Cu2O固体少量,加入到装有 10 mL3 mol/L H2SO4 溶液的试管中 | 溶液迅速变为蓝色;试管中出现少量亮红色固体 |
| Ⅴ | 取Cu2O固体少量,加入到装有 10 mL 3 mol/L H2SO4 和少量CuSO4 (浅蓝色)的试管中 | 现象同Ⅳ |
| Ⅵ | 重复实验Ⅰ,振荡试管,分为两等份。第一份立刻加入浓硫酸至 c(H2SO4)=3 mol/L;第二份静置 4 h之后,过滤,向固体中加入浓硫酸至 c(H2SO4)=3 mol/L | 第一份加酸后红色固体明显减少,溶液蓝色加深;第二份静置时,固体减少,溶液缓慢变为蓝色,固体加酸后无明显现象。 |
②通过以上实验,臧臧同学得出的结论是
您最近一年使用:0次
8 . 实验小组为验证NO2与水反应的产物,用如图所示装置进行实验(夹持装置已略去,气密性已检验)。
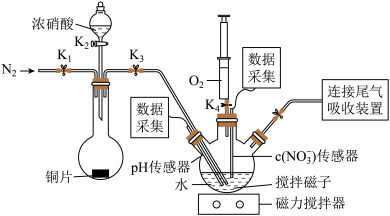
【实验过程】
步骤II中,传感器记录数据如图所示:

【解释及结论】
(1)NO2与水反应的离子方程式为___ 。
(2)步骤I中,通入N2的目的是___ 。
(3)将步骤II中圆底烧瓶内的实验现象补充完整:___ 。
(4)该实验验证NO2与水反应产物的实验证据包括___ (填序号)。
A.圆底烧瓶中溶液变为蓝绿色
B.三颈瓶内的气体从无色变为浅红棕色
C.pH传感器记录所得数据
D.NO3-传感器记录所得数据
(5)有同学认为该实验不严谨,因为也可能导致传感器所记录的数据结果___ 。

【实验过程】
| 实验步骤 | 实验现象 |
| Ⅰ.打开K1、K3、K5,关闭K2、K4,通入一段时间N2,关闭K1 | —— |
| Ⅱ.打开K2,放入足量浓HNO3,同时打开pH传感器和NO3-传感器,记录数据 | 圆底烧瓶中反应剧烈,铜片逐渐溶解,溶液变为蓝绿色, ;片刻后,三颈瓶内的导管口有气泡冒出 |
| III.5min后,打开K4,用注射器将少量空气注入三颈瓶,关闭K4 | 三颈瓶内的气体从无色变为浅红棕色 |
步骤II中,传感器记录数据如图所示:

【解释及结论】
(1)NO2与水反应的离子方程式为
(2)步骤I中,通入N2的目的是
(3)将步骤II中圆底烧瓶内的实验现象补充完整:
(4)该实验验证NO2与水反应产物的实验证据包括
A.圆底烧瓶中溶液变为蓝绿色
B.三颈瓶内的气体从无色变为浅红棕色
C.pH传感器记录所得数据
D.NO3-传感器记录所得数据
(5)有同学认为该实验不严谨,因为也可能导致传感器所记录的数据结果
您最近一年使用:0次
2020-06-02更新
|
232次组卷
|
2卷引用:北京市海淀区2018-2019学年高一学业水平合格性考试适应练习化学试题
名校
解题方法
9 . 如图为铜丝与浓硫酸反应并验证其产物性质的实验装置。
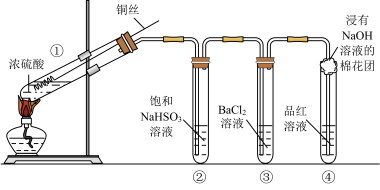
(1)①中反应的化学方程式是______ 。
(2)②中饱和NaHSO3溶液的作用是除去①中挥发出的硫酸。加热一段时间后,③中溶液依然澄清,④中溶液褪色。想要立即终止铜与硫酸的反应,最恰当的方法是______ 。
a.上移铜丝,使其脱离硫酸 b.撤去酒精灯 c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
完成上述反应的离子方程式。
(4)④中棉花团的作用是______ 。
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是______ 。

(1)①中反应的化学方程式是
(2)②中饱和NaHSO3溶液的作用是除去①中挥发出的硫酸。加热一段时间后,③中溶液依然澄清,④中溶液褪色。想要立即终止铜与硫酸的反应,最恰当的方法是
a.上移铜丝,使其脱离硫酸 b.撤去酒精灯 c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
| 加入试剂 | 现象 | 反应的离子方程式 | |
| 第一份 | 加入氨水 | 有白色沉淀生成 | |
| 第二份 | 加入氯水 | 有白色沉淀生成 |
完成上述反应的离子方程式。
(4)④中棉花团的作用是
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是
您最近一年使用:0次
10 . 铜与浓硫酸在如图所示装置中发生反应,实验中观察到的现象为 试管中溶液变为绿色,试管底部出现黑色和灰白色沉淀;
试管中溶液变为绿色,试管底部出现黑色和灰白色沉淀; 试管中先出现气泡,短时间内品红溶液无变化,之后溶液的红色逐渐变浅直至褪去。试回答下列问题:
试管中先出现气泡,短时间内品红溶液无变化,之后溶液的红色逐渐变浅直至褪去。试回答下列问题:
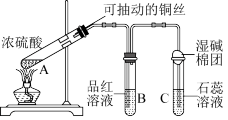
(1) 试管中发生反应的化学方程式为
试管中发生反应的化学方程式为______ 。
(2) 试管中先出现的气泡为
试管中先出现的气泡为______ (填名称)。
(3)实验完毕后取下 试管,
试管,______ ,若溶液______ ,可证明使品红溶液褪色的物质为 。
。
(4) 试管中的现象是
试管中的现象是______ 。
(5)湿碱棉团的作用是______ 。
(6)实验完毕后,待溶液冷却后,取 试管中上层清液加入水中,发现溶液温度升高。试解释溶液温度升高的原因:
试管中上层清液加入水中,发现溶液温度升高。试解释溶液温度升高的原因:____________ 。
(7)将反应后的沉淀加入水中,黑色沉淀不溶解,灰白色沉淀大部分溶解,溶液变为蓝色,则灰白色沉淀的主要成分为____________ 。
(8)黑色沉淀可能为 、
、 或
或 ,根据所学知识,设计实验验证黑色沉淀中是否含有
,根据所学知识,设计实验验证黑色沉淀中是否含有 (已知
(已知 、
、 均为黑色固体,不溶于水和稀硫酸):
均为黑色固体,不溶于水和稀硫酸):____________ 。
 试管中溶液变为绿色,试管底部出现黑色和灰白色沉淀;
试管中溶液变为绿色,试管底部出现黑色和灰白色沉淀; 试管中先出现气泡,短时间内品红溶液无变化,之后溶液的红色逐渐变浅直至褪去。试回答下列问题:
试管中先出现气泡,短时间内品红溶液无变化,之后溶液的红色逐渐变浅直至褪去。试回答下列问题:
(1)
 试管中发生反应的化学方程式为
试管中发生反应的化学方程式为(2)
 试管中先出现的气泡为
试管中先出现的气泡为(3)实验完毕后取下
 试管,
试管, 。
。(4)
 试管中的现象是
试管中的现象是(5)湿碱棉团的作用是
(6)实验完毕后,待溶液冷却后,取
 试管中上层清液加入水中,发现溶液温度升高。试解释溶液温度升高的原因:
试管中上层清液加入水中,发现溶液温度升高。试解释溶液温度升高的原因:(7)将反应后的沉淀加入水中,黑色沉淀不溶解,灰白色沉淀大部分溶解,溶液变为蓝色,则灰白色沉淀的主要成分为
(8)黑色沉淀可能为
 、
、 或
或 ,根据所学知识,设计实验验证黑色沉淀中是否含有
,根据所学知识,设计实验验证黑色沉淀中是否含有 (已知
(已知 、
、 均为黑色固体,不溶于水和稀硫酸):
均为黑色固体,不溶于水和稀硫酸):
您最近一年使用:0次
2020-03-04更新
|
493次组卷
|
3卷引用:2015-2016学年北京市怀柔区高一上学期期末化学试卷



