1 . 某学习小组利用下图装置探究铜与浓H2SO4的反应(夹持装置和A中加热装置已略,气密性已检验)。
资料:微量Cu2+与过量NaOH溶液发生反应:Cu2++4OH− =[Cu(OH)4]2−,[Cu(OH)4]2−溶于甘油形成特征的绛蓝色溶液。
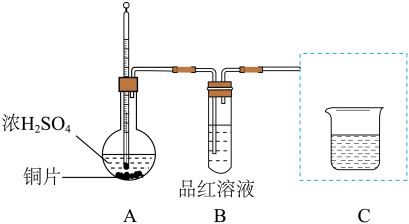
(1)A中反应的化学方程式是________ 。
(2)将装置C补充完整并标明所用试剂________ 。
(3)实验I中,铜片表面的黑色沉淀可能含CuO、Cu2S或CuS。为探究黑色沉淀的成分,取出反应后的铜片,用水小心冲洗后,进行下列操作:
甲认为通过上述两个实验证明黑色沉淀不含CuO,理由是________ 。
②乙同学认为仅通过颜色判断不能得出上述结论,理由是______ 。需要增加实验iii,说明黑色沉淀不含CuO,实验iii的操作和现象是_______ 。
(4)甲同学对黑色沉淀成分继续探究,补全实验方案:
(5)用仪器分析黑色沉淀的成分,数据如下:
230℃时黑色沉淀的成分是__________ 。
(6)为探究黑色沉淀消失的原因,取230℃时的黑色沉淀,加入浓H2SO4,加热至250℃时,黑色沉淀溶解,有刺激性气味的气体生成,试管底部出现淡黄色固体,溶液变蓝。用化学方程式解释原因____ 。
(7)综合上述实验过程,说明Cu和浓H2SO4除发生主反应外,还发生着其他副反应,为了避免副反应的发生,Cu和浓H2SO4反应的实验方案是______ 。
资料:微量Cu2+与过量NaOH溶液发生反应:Cu2++4OH− =[Cu(OH)4]2−,[Cu(OH)4]2−溶于甘油形成特征的绛蓝色溶液。

| 编号 | 实验用品 | 实验现象 | |
| I | 10mL 15mol/L 浓H2SO4溶液 | 过量铜片 | 剧烈反应,品红溶液褪色,150℃时铜片表面产生大量黑色沉淀,继续加热,250℃时黑色沉淀消失。 |
| II | 10mL 15mol/L 浓H2SO4溶液 | 适量铜片 | 剧烈反应,品红溶液褪色,150℃时铜片表面产生少量黑色沉淀,继续加热,250℃时黑色沉淀消失。 |
(1)A中反应的化学方程式是
(2)将装置C补充完整并标明所用试剂
(3)实验I中,铜片表面的黑色沉淀可能含CuO、Cu2S或CuS。为探究黑色沉淀的成分,取出反应后的铜片,用水小心冲洗后,进行下列操作:
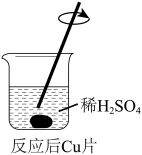 | 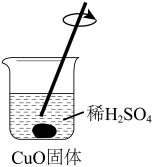 |
| i. 黑色沉淀脱落,一段时间后,上层溶液呈无色。 | ii. 开始时,上层溶液呈无色,一段时间后,上层溶液呈淡蓝色。 |
甲认为通过上述两个实验证明黑色沉淀不含CuO,理由是
②乙同学认为仅通过颜色判断不能得出上述结论,理由是
(4)甲同学对黑色沉淀成分继续探究,补全实验方案:
| 编号 | 实验操作 | 实验现象 |
| iv | 取洗净后的黑色沉淀,加入适量 | 黑色沉淀全部溶解,试管上部出现红棕色气体,底部有淡黄色固体生成。 |
(5)用仪器分析黑色沉淀的成分,数据如下:
| 150℃取样 | 230℃取样 |
| 铜元素3.2g,硫元0.96g。 | 铜元素1.28g,硫元0.64g。 |
230℃时黑色沉淀的成分是
(6)为探究黑色沉淀消失的原因,取230℃时的黑色沉淀,加入浓H2SO4,加热至250℃时,黑色沉淀溶解,有刺激性气味的气体生成,试管底部出现淡黄色固体,溶液变蓝。用化学方程式解释原因
(7)综合上述实验过程,说明Cu和浓H2SO4除发生主反应外,还发生着其他副反应,为了避免副反应的发生,Cu和浓H2SO4反应的实验方案是
您最近一年使用:0次
解题方法
2 . 某校课外活动小组为了探讨铜与硝酸的反应设计了如下实验。
(1)甲同学欲探究铜与稀硝酸反应产生的气体主要是NO,设计装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是含有一半空气的注射器。
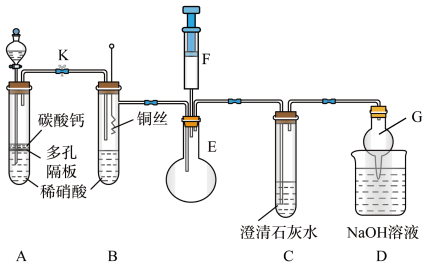
请回答有关问题:
①装置A中进行反应时打开止水夹K,当装置C中_________ 时,关闭止水夹K,试分析这样操作的目的是________ ,A中反应的离子方程式为______________ 。
②在完成①中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是__________________ ,B中反应的离子方程式为____________________ 。
③为进一步证明产物是NO,将注射器F中的空气推入E中,看到的现象是_________________ 。
④装置G的作用是_____________________ 。
(2)同学们发现铜与稀、浓硝酸反应所得溶液的颜色不同,并记录如下:
有同学认为是铜与浓硝酸反应的溶液中溶解了生成的气体,也有同学认为是溶液中剩余硝酸浓度较大所致,同学们分别设计了以下4个实验来判断该看法是否正确,以下方案中可行的是(选填序号字母)____________ 。
a. 向上述绿色溶液中通入氮气,观察颜色变化
b. 加水稀释上述绿色溶液,观察颜色变化
c. 向饱和的硝酸铜溶液中不断滴加14 mol·L-1HNO3溶液
d. 向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
(1)甲同学欲探究铜与稀硝酸反应产生的气体主要是NO,设计装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是含有一半空气的注射器。

请回答有关问题:
①装置A中进行反应时打开止水夹K,当装置C中
②在完成①中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是
③为进一步证明产物是NO,将注射器F中的空气推入E中,看到的现象是
④装置G的作用是
(2)同学们发现铜与稀、浓硝酸反应所得溶液的颜色不同,并记录如下:
| 将1 g细铜丝放入盛有10 mL的1 mol·L-1 HNO3溶液的试管中加热 | 铜丝表面有无色气体逸出,溶液变为天蓝色 |
| 将1 g细铜丝放入盛有10 mL的14 mol·L-1HNO3溶液的试管中 | 产生大量红棕色气体,溶液变为绿色,绿色由深到浅,未见到蓝色 |
a. 向上述绿色溶液中通入氮气,观察颜色变化
b. 加水稀释上述绿色溶液,观察颜色变化
c. 向饱和的硝酸铜溶液中不断滴加14 mol·L-1HNO3溶液
d. 向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
您最近一年使用:0次
名校
解题方法
3 . 课外小组的同学利用下图装置研究铜与稀硝酸的反应。
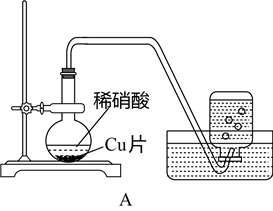
(1)铜与稀硝酸反应的离子方程式________________________________________ 。
(2)实验过程中水槽中的集气瓶收集到无色气体,甲同学由此认为铜与稀硝酸反应生成了NO。乙同学认为上述理由不完备,原因是________________________________________ (用化学方程式表示)。
(3)同学们经过讨论,决定改用装置B进行反应,实验步骤①~③如下图所示。

步骤③拔去注射器的橡胶帽,拉动活塞吸入少量的空气后,迅速盖上橡胶帽。如果观察到____________________ 的现象,就能证明铜与稀硝酸反应生成了NO。

(1)铜与稀硝酸反应的离子方程式
(2)实验过程中水槽中的集气瓶收集到无色气体,甲同学由此认为铜与稀硝酸反应生成了NO。乙同学认为上述理由不完备,原因是
(3)同学们经过讨论,决定改用装置B进行反应,实验步骤①~③如下图所示。

步骤③拔去注射器的橡胶帽,拉动活塞吸入少量的空气后,迅速盖上橡胶帽。如果观察到
您最近一年使用:0次
名校
解题方法
4 . 某同学在实验室做铜与浓硫酸反应的实验。
(1)写出反应的化学方程式________________________________________ 停止加热,将试管中的混合物冷却后倒入装有冷水的烧杯中,搅拌、静置,观察到烧杯底部有黑色物质。于是他对黑色物质进行了探究。
(2)该同学假设黑色物质是CuO。检验过程如下:
【查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6]溶液,若产生红褐红沉淀,证明有Cu2+】该同学的实验操作:
①将CuO放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,产生红褐色沉淀。
②将黑色物质放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,未见红褐色沉淀。实验①的目的是____________________ 由该检验过程所得结论是____________________ 。
(3)再次假设,黑色物质是铜的硫化物。实验如下:
①现象2说明黑色物质具有__________ 性。
②A试管上方产生浅红棕色气体的化学方程式是____________________ 。
③能确认黑色沉淀中含有S元素的现象是__________ 。
(4)以上实验说明,黑色物质中存在铜的硫化物。进一步实验后证明黑色物质是CuS与Cu2S的混合物。已知1molCu2S与稀硝酸反应转移8mole-,写出试管A中Cu2S溶解的化学方程式___________________ 。
(1)写出反应的化学方程式
(2)该同学假设黑色物质是CuO。检验过程如下:
【查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6]溶液,若产生红褐红沉淀,证明有Cu2+】该同学的实验操作:
①将CuO放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,产生红褐色沉淀。
②将黑色物质放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,未见红褐色沉淀。实验①的目的是
(3)再次假设,黑色物质是铜的硫化物。实验如下:
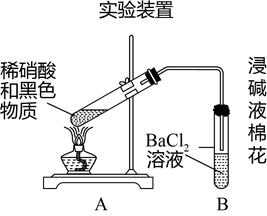 | 现象 1.A试管中黑色沉淀逐渐溶解 2.A试管内上方出现浅红棕色气体 3.B试管中出现白色沉淀 |
②A试管上方产生浅红棕色气体的化学方程式是
③能确认黑色沉淀中含有S元素的现象是
(4)以上实验说明,黑色物质中存在铜的硫化物。进一步实验后证明黑色物质是CuS与Cu2S的混合物。已知1molCu2S与稀硝酸反应转移8mole-,写出试管A中Cu2S溶解的化学方程式
您最近一年使用:0次
5 . 某学习小组为研究铜与浓、稀HNO3反应的差异,设计了如图所示的实验装置。
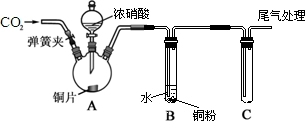
实验步骤如下:
Ⅰ.检查装置的气密性;
Ⅱ.向装置A中通入过量的CO2气体,关闭弹簧夹;
Ⅲ.滴加浓硝酸;
……
(1)步骤Ⅲ中滴加浓硝酸的具体操作是____________ 。
(2)A装置中反应的化学方程式是____________ 。
(3)B中溶液慢慢变成蓝色,能解释此现象的化学方程式是_____________ 。
(4)证明B中有NO生成的实验操作是_____________ 。
(5)步骤Ⅱ向装置A中通入过量CO2气体的目的是______________ 。
(6)上述实验结束后,观察到A装置中的溶液呈绿色,B装置中的溶液呈蓝色。在分析溶液为绿色的原因时,甲同学用加水稀释的方法,乙同学认为不合理,因在稀释时,也会引起Cu2+浓度变化。请设计实验证明绿色是由溶有NO2引起的___________ 。

实验步骤如下:
Ⅰ.检查装置的气密性;
Ⅱ.向装置A中通入过量的CO2气体,关闭弹簧夹;
Ⅲ.滴加浓硝酸;
……
(1)步骤Ⅲ中滴加浓硝酸的具体操作是
(2)A装置中反应的化学方程式是
(3)B中溶液慢慢变成蓝色,能解释此现象的化学方程式是
(4)证明B中有NO生成的实验操作是
(5)步骤Ⅱ向装置A中通入过量CO2气体的目的是
(6)上述实验结束后,观察到A装置中的溶液呈绿色,B装置中的溶液呈蓝色。在分析溶液为绿色的原因时,甲同学用加水稀释的方法,乙同学认为不合理,因在稀释时,也会引起Cu2+浓度变化。请设计实验证明绿色是由溶有NO2引起的
您最近一年使用:0次
2016-12-09更新
|
243次组卷
|
2卷引用:2015-2016学年北京市朝阳区高一上学期期末考试化学试卷
13-14高三·北京·阶段练习
6 . 下列关系图中,A是一种正盐,E是强酸,当甲无论是强酸或强碱都有如下反应关系:
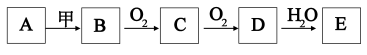
友情提示:当甲无论是强酸或强碱,A、B、C、D、E均为同种元素对应的不同的化合物。
回答下列问题:
(1)A是___________ (用化学式表示)
(2)当甲是稀盐酸溶液时,B为具有臭鸡蛋气味的气体
①写出B与C的反应方程式:________
②一定质量的Zn与100mL 12.0mol/L的E的浓溶液充分反应,反应后称量剩余锌发现质量减少了65.0g。将反应后的溶液稀释至1L,此时溶液中c(SO )=
)=____ mol/L,产生SO2体积(标准状况下)=_____________ L
(3)当甲是浓氢氧化钠溶液时,B为易液化的气体可作制冷剂
①C是______ ,在浓的E溶液中放入过量的铜片,则反应将要结束时的离子方程式为______________ 。
②将盛有D和O2的混合气体12mL的量筒倒立于水槽中,充分反应后,剩余2mL无色气体(均在同温同压下测定),则原混合气体中氧气的体积是___________ 。
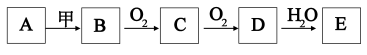
友情提示:当甲无论是强酸或强碱,A、B、C、D、E均为同种元素对应的不同的化合物。
回答下列问题:
(1)A是
(2)当甲是稀盐酸溶液时,B为具有臭鸡蛋气味的气体
①写出B与C的反应方程式:
②一定质量的Zn与100mL 12.0mol/L的E的浓溶液充分反应,反应后称量剩余锌发现质量减少了65.0g。将反应后的溶液稀释至1L,此时溶液中c(SO
 )=
)=(3)当甲是浓氢氧化钠溶液时,B为易液化的气体可作制冷剂
①C是
②将盛有D和O2的混合气体12mL的量筒倒立于水槽中,充分反应后,剩余2mL无色气体(均在同温同压下测定),则原混合气体中氧气的体积是
您最近一年使用:0次
11-12高三上·北京·阶段练习
7 . 兴趣小组通过实验探究溶解铜的方法和本质。
(1)在热水浴中进行3个实验,部分实验报告如下表所示
①实验Ⅰ、Ⅱ的目的是__________________ 。
②实验Ⅲ中反应的本质是(用离子方程式表示)____________________ 。
(2)利用电化学原理实现铜溶于稀硫酸并生成氢气。
①Cu作________ 极。②总反应的离子方程式是____________ 。
(1)在热水浴中进行3个实验,部分实验报告如下表所示
| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 稀硫酸中加入铜片 | 无明显变化 |
| Ⅱ | 硝酸钠溶液中加入铜片 | 无明显变化 |
| Ⅲ | 稀硫酸中加入硝酸钠溶液 | 无明显变化 |
| 再加入铜片 | 有无色气泡;溶液变蓝 |
①实验Ⅰ、Ⅱ的目的是
②实验Ⅲ中反应的本质是(用离子方程式表示)
(2)利用电化学原理实现铜溶于稀硫酸并生成氢气。
①Cu作
您最近一年使用:0次
11-12高三上·北京西城·期末
8 . 兴趣小组通过实验探究溶解铜的方法和本质。
(1)在热水浴中进行3个实验,部分实验报告如下表所示。
① 实验I、II的目的是______ 。
②实验III中反应的本质是(用离子方程式表示)______ 。
(2)利用电化学原理实现铜溶于稀硫酸并生成氢气。
① Cu作______ 极。
②总反应的离子方程式是______ 。
(1)在热水浴中进行3个实验,部分实验报告如下表所示。
| 序号 | 实验操作 | 实验现象 |
| I | 稀硫酸中加入铜片 | 无明显变化 |
| II | 硝酸钠溶液中加入铜片 | 无明显变化 |
| III | 稀硫酸中加入硝酸钠溶液 | 无明显变化 |
| 再加入铜片 | 有无色气泡;溶液变蓝 |
②实验III中反应的本质是(用离子方程式表示)
(2)利用电化学原理实现铜溶于稀硫酸并生成氢气。
① Cu作
②总反应的离子方程式是
您最近一年使用:0次
2010·北京·二模
解题方法
9 . 硫酸铜、硝酸铁都是重要的化工原料。
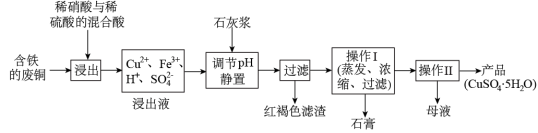
(1)以下是某工厂用含铁的废铜为原料生产胆巩(CuSO4·5H2O)的生产流程示意图:
胆矾和石膏在不同温度下的溶解度(∥100g水)见下表。
请回答下列问题:
①红褐色滤渣的主要成分是
②写出浸出过程中生成硫酸铜的化学方程式 ;
③操作I的温度应该控制在 左右;
④从溶液中分离出硫酸铜晶体的操作Ⅱ应为:将热溶液 、 、洗涤、干燥。
(2)某兴趣小组在实验室用铁粉和稀硝酸及右图装置制取Fe(NO3)3(固定所用
仪器和加热装置未画出)。
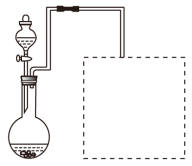
①为保证原料的充分利用,并加快反应速率,往往将加热温度控制在100℃以内。该实验中对圆底烧瓶加热的最佳方式是 加热;
②请在图中虚线框内画出尾气吸收装置(提示:碱液可快速、充分吸收产生的氮氧化物气体)。
(1)以下是某工厂用含铁的废铜为原料生产胆巩(CuSO4·5H2O)的生产流程示意图:

胆矾和石膏在不同温度下的溶解度(∥100g水)见下表。
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
①红褐色滤渣的主要成分是
②写出浸出过程中生成硫酸铜的化学方程式 ;
③操作I的温度应该控制在 左右;
④从溶液中分离出硫酸铜晶体的操作Ⅱ应为:将热溶液 、 、洗涤、干燥。
(2)某兴趣小组在实验室用铁粉和稀硝酸及右图装置制取Fe(NO3)3(固定所用
仪器和加热装置未画出)。

①为保证原料的充分利用,并加快反应速率,往往将加热温度控制在100℃以内。该实验中对圆底烧瓶加热的最佳方式是 加热;
②请在图中虚线框内画出尾气吸收装置(提示:碱液可快速、充分吸收产生的氮氧化物气体)。
您最近一年使用:0次



