2021·湖南·高考真题
1 . 铁的配合物离子(用 表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:
表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:
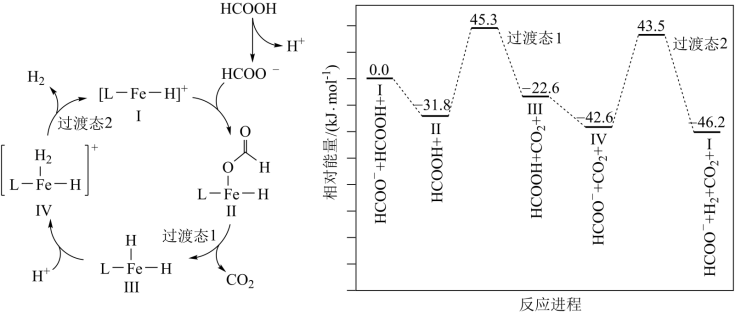
下列说法错误的是
 表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:
表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:
下列说法错误的是
A.该过程的总反应为 |
B. 浓度过大或者过小,均导致反应速率降低 浓度过大或者过小,均导致反应速率降低 |
C.该催化循环中 元素的化合价发生了变化 元素的化合价发生了变化 |
| D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定 |
您最近一年使用:0次
2021-06-09更新
|
9154次组卷
|
39卷引用:2020年山东卷化学高考真题变式题11-15
(已下线)2020年山东卷化学高考真题变式题11-15山东省泰安市部分学校2023-2024学年高二上学期期末调研化学试题山东省威海市乳山市银滩高级中学2023-2024学年高二上学期1月模块考试化学试题2021年新高考湖南化学高考真题(已下线)考点17 化学反应速率及其影响因素-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点17 化学反应速率及其影响因素-备战2022年高考化学一轮复习考点帮(浙江专用)江苏省如皋中学2021-2022学年高三上学期期初测试化学试题(已下线)课时35 化学反应速率及影响因素-2022年高考化学一轮复习小题多维练(全国通用)安徽省合肥工业大学附属中学2021-2022学年高三上学期第一次阶段考试化学试题辽宁省东北育才学校2021-2022学年高二上学期期中考试化学试题(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)2021年湖南省高考化学试卷变式题11-19北京市第八中学2021-2022学年高二上学期期中考试化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题10 化学反应与能量-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)卷10 化学反应机理选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)秘籍08 反应历程探究与催化原理图象分析-备战2022年高考化学抢分秘籍(全国通用)(已下线)押新高考卷11题 反应机理分析-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题09 化学反应速率、化学平衡-三年(2020-2022)高考真题分项汇编(已下线)考点21 化学反应速率-备战2023年高考化学一轮复习考点帮(全国通用)江苏省海安高级中学2021-2022学年高二上学期阶段测试(二)化学试题(已下线)第15讲 化学反应的热效应 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题36 高考“明星”考点—催化剂-备战2023年高考化学一轮复习考点微专题(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题湖南省衡阳师范学院祁东附属中学2021-2022学年高三上学期12月月考化学试题(已下线)专题12 化学反应机理(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)第七章 化学反应速率与化学平衡 热点强化12 化学反应历程、机理的分析应用(已下线)素养卷02 循环转化过渡态理论图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)考点21 化学反应速率(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题09 化学反应中的热效应与反应机理-2023年高考化学真题题源解密(全国通用)(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)热点题型训练 催化剂与反应历程(机理)(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)北京大学附属中学2021-2022学年高二下学期期末考试化学试卷(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题
名校
解题方法
2 . 氮及其化合物的转化过程如图所示。下列分析合理的是
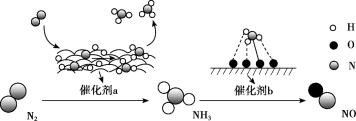

| A.催化剂a表面只发生极性共价键的断裂和形成 |
| B.N2与H2反应生成NH3的原子利用率为100% |
| C.在催化剂b表面形成氮氧键时,不涉及电子转移 |
| D.催化剂a、b能提高反应的平衡转化率 |
您最近一年使用:0次
2021-05-19更新
|
784次组卷
|
23卷引用:山东省2020届高三模拟考试化学试题
山东省2020届高三模拟考试化学试题山东省潍坊市昌乐县2020年高三上学期第一次高考模拟化学试题山东省2020届普通高中学业水平等级考试 · 模拟卷(三)化学试题【区级联考】北京市朝阳区2019届高三下学期二模考试化学试题云南省玉溪一中2020届高三上学期期中考试理综化学试题辽宁省沈阳市五校协作体2020届高三上学期期中考试化学试题北京市石景山区精华学校2019-2020学年高三上学期二次月考化学试题河北省枣强中学2019-2020学年高二下学期第三次月考化学试题北京市房山区2020届高三一模化学试题天津市南开区2020届高三上学期期末考试化学试题福建省福州市2019届高三5月高考模拟化学试题新疆吾尔自治区乌鲁木齐市第七十中学2021届高三上学期第一次月考(9月)化学试题安徽省涡阳县第一中学2021届高三上学期第二次月考化学试题湖南省张家界市2020-2021学年高二上学期期末考试化学试题福建省莆田第一中学2020-2021学年高二下学期期中考试化学试题天津市西青区张家窝中学2022届高三上学期第一次月考化学试题(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-测试(已下线)2022年江苏卷高考真题变式题1-13湖南省长沙市宁乡市2020-2021学年高二下学期期末调研考试化学试题(已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题6-10)北京市中国人民大学附属中学朝阳学校2021-2022学年高三上学期第一次月考化学试题陕西省榆林市2023-2024学年高二上学期10月月考化学试题(已下线)物质反应及转化
20-21高三上·广东·阶段练习
3 . 据报道,亚硝胺[(CH3)2N−N=O]是一种直接的致癌物质,亚硝酸与二甲胺[(CH3)2NH]相遇会迅速反应生成亚硝胺,其反应机理如下图所示:

下列说法正确的是

下列说法正确的是
| A.亚硝酸与二甲胺生成亚硝胺的反应是吸热反应 |
| B.过程i发生的是加成反应,过程ii发生的是取代反应 |
| C.过程i的反应速率比过程ii的反应速率慢 |
| D.降低温度在一定程度上会抑制亚硝胺的生成 |
您最近一年使用:0次
名校
解题方法
4 . 氧化亚氮(N2O)是一种强温室气体,且易转换成颗粒污染物。碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g)→2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k•c(N2O)•[c(I2)]0.5(k为速率常数)。下列表述正确的是
第一步I2(g)→2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k•c(N2O)•[c(I2)]0.5(k为速率常数)。下列表述正确的是
| A.N2O分解反应中,k(含碘)>k(无碘) | B.第一步对总反应速率起决定作用 |
| C.第二步活化能比第三步小 | D.I2浓度与N2O分解速率无关 |
您最近一年使用:0次
2021-03-12更新
|
361次组卷
|
3卷引用:湖南省攸县第三中学2020届高三第五次月考化学试题
5 . 氨氮废水中的氮元素多以NH 和NH3·H2O的形式存在,在一定条件下,NH
和NH3·H2O的形式存在,在一定条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO ,两步反应的能量变化示意图如下:
,两步反应的能量变化示意图如下:
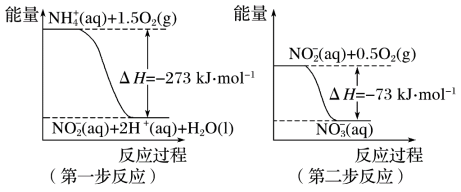
下列说法合理的是
 和NH3·H2O的形式存在,在一定条件下,NH
和NH3·H2O的形式存在,在一定条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO ,两步反应的能量变化示意图如下:
,两步反应的能量变化示意图如下: 
下列说法合理的是
A.该反应的催化剂是NO |
B.升高温度,两步反应速率均加快,有利于NH 转化成NO 转化成NO |
| C.在第一步反应中,当溶液中水的电离程度不变时,该反应即达平衡状态 |
D.1 mol NH 在第一步反应中与1 mol NO 在第一步反应中与1 mol NO 在第二步反应中失电子数之比为1:3 在第二步反应中失电子数之比为1:3 |
您最近一年使用:0次
2020-12-04更新
|
269次组卷
|
2卷引用:湖北省汉川市第二中学2020-2021学年高二上学期期中考试化学试题
名校
6 . 二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如图所示。

下列叙述正确的是

下列叙述正确的是
A.海水酸化能引起HCO 浓度减小、CO 浓度减小、CO 浓度增大 浓度增大 |
| B.海水酸化能促进CaCO3的溶解,导致珊瑚礁减少 |
C.CO2能引起海水酸化,其原理为HCO ⇌H++ CO ⇌H++ CO |
| D.珊瑚周围藻类植物的生长不利于珊瑚的形成 |
您最近一年使用:0次
2020-11-17更新
|
246次组卷
|
2卷引用:山东省日照市莒县2020-2021学年高二11月模块考试化学试题
名校
7 . 工业上生产环氧乙烷的反应为:2 CH2=CH2 (g) + O2 (g) = 2 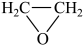 (g) ∆H = -106 kJ • mol−1,其反应机理如下:
(g) ∆H = -106 kJ • mol−1,其反应机理如下:
①Ag + O2=AgO2慢
②CH2=CH2+ AgO2 = + AgO 快
+ AgO 快
③CH2= CH2 + 6AgO =2CO2 + 2H2O + 6Ag 快
下列有关该反应的说法正确的是
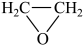 (g) ∆H = -106 kJ • mol−1,其反应机理如下:
(g) ∆H = -106 kJ • mol−1,其反应机理如下:①Ag + O2=AgO2慢
②CH2=CH2+ AgO2 =
 + AgO 快
+ AgO 快③CH2= CH2 + 6AgO =2CO2 + 2H2O + 6Ag 快
下列有关该反应的说法正确的是
| A.反应的活化能等于 106 kJ·mol−1 |
| B.工业上生产环氧乙烷的反应是一个焓减熵增的反应,所以能自发进行 |
| C.增大乙烯浓度能显著提高环氧乙烷的生成速率 |
| D.理论上 0.7 mol 乙烯参与反应最多可得到 0.6 mol 环氧乙烷 |
您最近一年使用:0次
2020-10-31更新
|
256次组卷
|
3卷引用:北京二中2020-2021学年高二上学期10月月考化学试题
名校
8 . 二氧化碳的捕捉与封存是实现温室气体减排的重要途径之一,也是未来实现低碳经济转型的重要环节。一些科学家利用太阳能加热反应器来“捕捉”空气中的CO2(如图所示)。下列说法中正确的是( )

生石灰捕捉和封存二氧化碳的示意图

生石灰捕捉和封存二氧化碳的示意图
| A.步骤一中将反应器加热到400 ℃,可提高CaCO3的生成速率 |
| B.步骤一中生成CaCO3的反应为吸热反应 |
| C.步骤一与步骤二中的反应互为可逆反应 |
| D.步骤二中反应的ΔS<0 |
您最近一年使用:0次
2020-09-21更新
|
401次组卷
|
4卷引用:山东省东营市胜利第二中学2020-2021学年高二10月月考化学试题
山东省东营市胜利第二中学2020-2021学年高二10月月考化学试题(已下线)第02章 化学反应速率与化学平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)山东省东营市广饶县第一中学三校区2022-2023学年高二9月月考化学试题山东省菏泽市郓城第一中学2022-2023学年高二上学期自我检测(10月)化学试题
名校
解题方法
9 . 以纳米二氧化钛膜为工作电极,常温常压电解CO2,可制得低密度聚乙烯(LDPE),该反应过程的机理如图所示下列说法正确的是( )
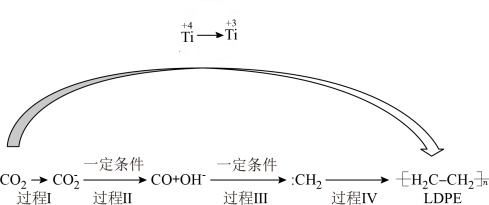

| A.过程Ⅰ~Ⅲ中碳元素均发生还原反应 |
| B.﹕CH2这个8电子微粒中既包含极性共价键又包含非极性共价键 |
| C.工业上生产7×103kg的LDPE,理论上需要CO2的体积是1.12×107L |
D.CO2最终转化为LDPE的电极反应式是2nCO2-12e-+12nH+=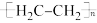 +4nH2O +4nH2O |
您最近一年使用:0次
名校
解题方法
10 . 某无色溶液中可能含有CrO 、NH
、NH 、SO
、SO 、Mg2+、Al3+、K+、SO
、Mg2+、Al3+、K+、SO 、Cl-、NO
、Cl-、NO 中的一种或几种,已知所含离子的物质的量浓度相等。取甲、乙两支试管分别加入1mL该溶液进行如下实验:①向甲中加入适量稀盐酸,无明显现象;②向乙中逐滴滴加NaOH溶液至过量并加热,现象为先有白色沉淀产生,进而产生刺激性气味气体,最后白色沉淀完全溶解。对于该溶液中的离子成分,下列说法正确的是( )
中的一种或几种,已知所含离子的物质的量浓度相等。取甲、乙两支试管分别加入1mL该溶液进行如下实验:①向甲中加入适量稀盐酸,无明显现象;②向乙中逐滴滴加NaOH溶液至过量并加热,现象为先有白色沉淀产生,进而产生刺激性气味气体,最后白色沉淀完全溶解。对于该溶液中的离子成分,下列说法正确的是( )
 、NH
、NH 、SO
、SO 、Mg2+、Al3+、K+、SO
、Mg2+、Al3+、K+、SO 、Cl-、NO
、Cl-、NO 中的一种或几种,已知所含离子的物质的量浓度相等。取甲、乙两支试管分别加入1mL该溶液进行如下实验:①向甲中加入适量稀盐酸,无明显现象;②向乙中逐滴滴加NaOH溶液至过量并加热,现象为先有白色沉淀产生,进而产生刺激性气味气体,最后白色沉淀完全溶解。对于该溶液中的离子成分,下列说法正确的是( )
中的一种或几种,已知所含离子的物质的量浓度相等。取甲、乙两支试管分别加入1mL该溶液进行如下实验:①向甲中加入适量稀盐酸,无明显现象;②向乙中逐滴滴加NaOH溶液至过量并加热,现象为先有白色沉淀产生,进而产生刺激性气味气体,最后白色沉淀完全溶解。对于该溶液中的离子成分,下列说法正确的是( )A.一定含有NH 、Al3+、SO 、Al3+、SO 、Cl-、NO 、Cl-、NO |
B.一定不含CrO 、SO 、SO 、Mg2+、NO 、Mg2+、NO |
C.可能含有Mg2+、K+、Cl-、NO |
D.一定不含CrO 、SO 、SO 、Mg2+、SO 、Mg2+、SO |
您最近一年使用:0次
2020-08-15更新
|
1287次组卷
|
6卷引用:山东省济南市历城区第一中学2020届高三12月检测化学试题
山东省济南市历城区第一中学2020届高三12月检测化学试题(已下线)第07讲 离子共存 离子的检验和推断(精讲)——2021年高考化学一轮复习讲练测(已下线)专题04 离子反应(缺项配平、离子检验、离子推断、共存)-2021年高考化学必做热点专题河南省南阳市第一中学校2021-2022学年高三上学期第三次月考化学试题(已下线)第3讲 离子反应的应用(离子共存、离子检验和推断)黑龙江哈尔滨第三中学2024届高三上学期期中考试化学试题



