1 . 氢能是一种清洁能源,按照生产过程中的碳排放情况分为灰氢、蓝氢和绿氢。
(1)煤的气化制得灰氢 : 。该反应的平衡常数表达式K=
。该反应的平衡常数表达式K=_______ 。该方法生产过程有CO2排放。
(2)甲烷水蒸气催化重整制得蓝氢 ,步骤如下。
ⅰ.H2的制取:
 。为提高CH4的平衡转化率,可采取的措施有
。为提高CH4的平衡转化率,可采取的措施有_______ (写出两条即可)。
ⅱ.H2的富集:
 。已知830℃时,该反应的平衡常数K=1,向体积为1 L的恒容密闭容器中充入3 mol CO和3 mol H2O(g),某时刻测得H2为1 mol,此时反应
。已知830℃时,该反应的平衡常数K=1,向体积为1 L的恒容密闭容器中充入3 mol CO和3 mol H2O(g),某时刻测得H2为1 mol,此时反应_______ (填“已达到”或“未达到”)化学平衡状态,理由是_______ ,反应达平衡时CO的转化率为_______ 。
(3)热化学硫碘循环分解水制得绿氢 ,全程零碳排放。反应如下:
反应ⅰ: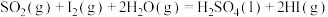
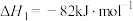
反应ⅱ: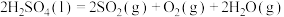
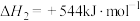
反应ⅲ:……
反应ⅰ~ⅲ循环可实现分解水:
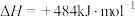
①已知破坏1 mol H2和破坏1 mol O2中化学键所消耗能量分别是436 kJ和498 kJ,则H2O中H-O键比H2中H-H键_______ (填“强”或“弱”)。
②写出反应ⅲ的热化学方程式_______ 。
(1)煤的气化制得
 。该反应的平衡常数表达式K=
。该反应的平衡常数表达式K=(2)甲烷水蒸气催化重整制得
ⅰ.H2的制取:

 。为提高CH4的平衡转化率,可采取的措施有
。为提高CH4的平衡转化率,可采取的措施有ⅱ.H2的富集:

 。已知830℃时,该反应的平衡常数K=1,向体积为1 L的恒容密闭容器中充入3 mol CO和3 mol H2O(g),某时刻测得H2为1 mol,此时反应
。已知830℃时,该反应的平衡常数K=1,向体积为1 L的恒容密闭容器中充入3 mol CO和3 mol H2O(g),某时刻测得H2为1 mol,此时反应(3)热化学硫碘循环分解水制得
反应ⅰ:
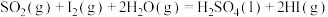
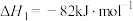
反应ⅱ:
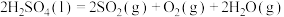
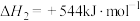
反应ⅲ:……
反应ⅰ~ⅲ循环可实现分解水:

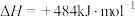
①已知破坏1 mol H2和破坏1 mol O2中化学键所消耗能量分别是436 kJ和498 kJ,则H2O中H-O键比H2中H-H键
②写出反应ⅲ的热化学方程式
您最近一年使用:0次
2023-01-14更新
|
141次组卷
|
2卷引用: 北京市大兴区第一中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
2 . 中国科学家在淀粉人工光合成方面取得重大突破性进展,该实验方法首先将 催化还原为
催化还原为 。已知
。已知 催化加氢的主要反应有:
催化加氢的主要反应有:
①

②
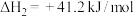
其他条件不变时,在相同时间内温度对 催化加氢的影响如图。
催化加氢的影响如图。
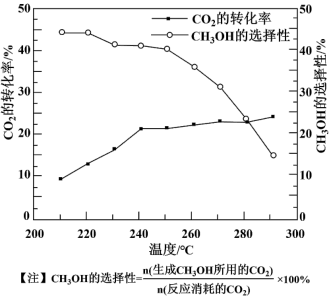
下列说法不正确的是
 催化还原为
催化还原为 。已知
。已知 催化加氢的主要反应有:
催化加氢的主要反应有:①


②

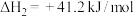
其他条件不变时,在相同时间内温度对
 催化加氢的影响如图。
催化加氢的影响如图。
下列说法不正确的是
A.  |
| B.使用催化剂,能降低反应的活化能,增大活化分子百分数 |
| C.220~240℃,升高温度,对反应②速率的影响比对反应①的小 |
D.其他条件不变,增大压强,不利于反应向生成 的方向进行 的方向进行 |
您最近一年使用:0次
2022-12-09更新
|
412次组卷
|
4卷引用:北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题
北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题山东省临沂市沂水县2022-2023学年高二上学期学科素养(期中)检测化学试题(已下线)2023年高考山东卷化学真题变式题(不定项选择题)北京市对外经济贸易大学附属中学2022-2023学年高二上学期期中考试化学试题
解题方法
3 .  相关转化的研究对解决环境、能源问题意义重大。
相关转化的研究对解决环境、能源问题意义重大。
I.(1) 与
与 经催化重整可制得合成气:
经催化重整可制得合成气: 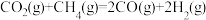
按一定体积比加入 和
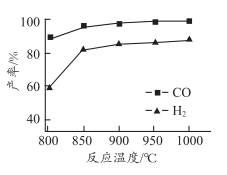
和 ,在恒压下发生反应温度对
,在恒压下发生反应温度对 和
和 产率影响如图所示。生产中优选的温度范围是
产率影响如图所示。生产中优选的温度范围是___________ (填字母序号)。
a.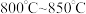 b.
b.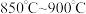 c.
c.
Ⅱ. 与
与 反应制取甲醇
反应制取甲醇
(1) 与
与 反应的热化学方程式表示如下:
反应的热化学方程式表示如下:
反应i:
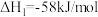
反应ⅱ:
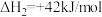
写出 与
与 生成
生成 的热化学方程式
的热化学方程式___________ 。
(2)关于反应i和反应ⅱ的说法正确的是___________ 。
a.升高温度能使反应i的反应速率增大,平衡常数减小
b.增大压强能提高反应ⅱ中 的转化率
的转化率
c.低温、高压有利于 催化加氢制取
催化加氢制取
(3)某同学研究温度、压强对反应平衡的影响,得到上述反应i和反应ⅱ中 平衡转化率、甲醇选择性与温度、压强的关系如下图。
平衡转化率、甲醇选择性与温度、压强的关系如下图。
已知:
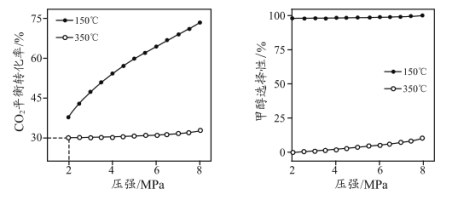
结合上图,350℃、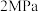 时,发生的主要反应是
时,发生的主要反应是___________ (填“反应i”或“反应ii”)。此条件下,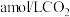 和
和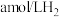 在恒容、密闭容器中充分反应达到平衡,写出所发生反应的化学平衡常数K的计算过程及结果
在恒容、密闭容器中充分反应达到平衡,写出所发生反应的化学平衡常数K的计算过程及结果___________ (结果用分数表示)。
Ⅲ.利用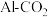 电池(工作原理如下图所示)能有效地将
电池(工作原理如下图所示)能有效地将 转化成化工原料草酸铝
转化成化工原料草酸铝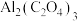 。
。
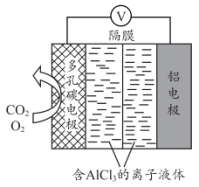
(1)电池的负极反应式为___________ 。
(2)电池的正极反应式: (草酸根)正极反应过程中,
(草酸根)正极反应过程中, 起催化作用,催化过程可表示为:
起催化作用,催化过程可表示为:
①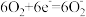
②……
写出反应②的离子方程式___________ 。
 相关转化的研究对解决环境、能源问题意义重大。
相关转化的研究对解决环境、能源问题意义重大。I.(1)
 与
与 经催化重整可制得合成气:
经催化重整可制得合成气: 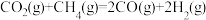
按一定体积比加入
 和
和 ,在恒压下发生反应温度对
,在恒压下发生反应温度对 和
和 产率影响如图所示。生产中优选的温度范围是
产率影响如图所示。生产中优选的温度范围是
a.
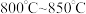 b.
b.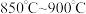 c.
c.
Ⅱ.
 与
与 反应制取甲醇
反应制取甲醇
(1)
 与
与 反应的热化学方程式表示如下:
反应的热化学方程式表示如下:反应i:

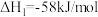
反应ⅱ:

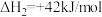
写出
 与
与 生成
生成 的热化学方程式
的热化学方程式(2)关于反应i和反应ⅱ的说法正确的是
a.升高温度能使反应i的反应速率增大,平衡常数减小
b.增大压强能提高反应ⅱ中
 的转化率
的转化率c.低温、高压有利于
 催化加氢制取
催化加氢制取
(3)某同学研究温度、压强对反应平衡的影响,得到上述反应i和反应ⅱ中
 平衡转化率、甲醇选择性与温度、压强的关系如下图。
平衡转化率、甲醇选择性与温度、压强的关系如下图。已知:


结合上图,350℃、
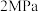 时,发生的主要反应是
时,发生的主要反应是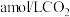 和
和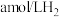 在恒容、密闭容器中充分反应达到平衡,写出所发生反应的化学平衡常数K的计算过程及结果
在恒容、密闭容器中充分反应达到平衡,写出所发生反应的化学平衡常数K的计算过程及结果Ⅲ.利用
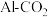 电池(工作原理如下图所示)能有效地将
电池(工作原理如下图所示)能有效地将 转化成化工原料草酸铝
转化成化工原料草酸铝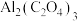 。
。
(1)电池的负极反应式为
(2)电池的正极反应式:
 (草酸根)正极反应过程中,
(草酸根)正极反应过程中, 起催化作用,催化过程可表示为:
起催化作用,催化过程可表示为:①
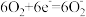
②……
写出反应②的离子方程式
您最近一年使用:0次
4 . 氨是现代社会中必不可少的原料。催化合成氨是氮循环的重要一环。
(1)目前工业上用氢气和氮气合成氨。
①写出工业合成氨的化学方程式_____________________________ 。
② NH3和PH3的分解温度分别是600℃和500℃,热稳定性差异的原因是
____________________________________________________ ,
元素的非金属性逐渐减弱,氢化物稳定性逐渐减弱。
(2)工业合成氨主要经过原料气(N2、H2)的制取、净化、压缩合成三大过程。
①天然气蒸汽转化法是目前获取原料气中H2的主流方法。CH4经过两步反应完全转化为H2和CO2,其能量变化示意图如下:
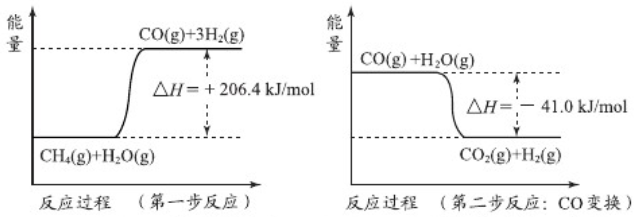
1mol CH4(g)通过蒸汽转化为CO2(g)和H2(g)的热化学方程式是
______________________________________________________ 。
②CO变换过程可由Fe2O3催化完成。将下述催化过程补充完整:
i.3Fe2O3 + CO = 2Fe3O4 + CO2
ii._____________________________________________
③醋酸铜氨液可以吸收原料气中CO等少量杂质。吸收CO反应为:
[Cu(NH3)2]Ac(aq)+NH3(aq)+CO(g)==[Cu(NH3)3CO]Ac(aq) △H <0。
下图表示压强和温度对醋酸铜氨液吸收CO能力的影响。L(L1、L2),X可分别代表压强或温度。
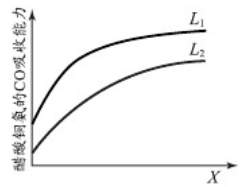
i.X代表的物理量是_________ 。
ii.判断L1、L2的大小关系并简述理由_________________________________________ 。
(3)电化学法也可合成氨。下图是用低温固体质子导体作为电解质,用Pt-C3N4作阴极催化剂电解H2(g)和N2(g)合成NH3的原理示意图:
①Pt-C3N4电极反应产生的气体是NH3和______ 。
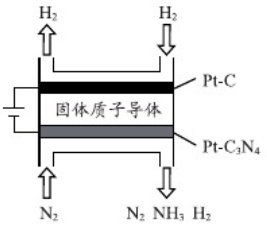
②实验表明,其它条件不变,逐渐增加电解电压,氨气生成速率会逐渐增大,但当电解电压高于1.2V后,氨气生成速率反而会随电压升高而下降,分析其可能原因_________________________ 。
(1)目前工业上用氢气和氮气合成氨。
①写出工业合成氨的化学方程式
② NH3和PH3的分解温度分别是600℃和500℃,热稳定性差异的原因是
元素的非金属性逐渐减弱,氢化物稳定性逐渐减弱。
(2)工业合成氨主要经过原料气(N2、H2)的制取、净化、压缩合成三大过程。
①天然气蒸汽转化法是目前获取原料气中H2的主流方法。CH4经过两步反应完全转化为H2和CO2,其能量变化示意图如下:

1mol CH4(g)通过蒸汽转化为CO2(g)和H2(g)的热化学方程式是
②CO变换过程可由Fe2O3催化完成。将下述催化过程补充完整:
i.3Fe2O3 + CO = 2Fe3O4 + CO2
ii.
③醋酸铜氨液可以吸收原料气中CO等少量杂质。吸收CO反应为:
[Cu(NH3)2]Ac(aq)+NH3(aq)+CO(g)==[Cu(NH3)3CO]Ac(aq) △H <0。
下图表示压强和温度对醋酸铜氨液吸收CO能力的影响。L(L1、L2),X可分别代表压强或温度。

i.X代表的物理量是
ii.判断L1、L2的大小关系并简述理由
(3)电化学法也可合成氨。下图是用低温固体质子导体作为电解质,用Pt-C3N4作阴极催化剂电解H2(g)和N2(g)合成NH3的原理示意图:
①Pt-C3N4电极反应产生的气体是NH3和

②实验表明,其它条件不变,逐渐增加电解电压,氨气生成速率会逐渐增大,但当电解电压高于1.2V后,氨气生成速率反而会随电压升高而下降,分析其可能原因
您最近一年使用:0次



