名校
解题方法
1 . 反应速率与化学平衡均是化工生产中关注的重要问题。
(1)平衡常数K能为化学工作者提供许多信息。
实验测得下列3个反应的平衡常数K与温度T的函数关系如下:
则在该实验条件下,反应Ⅰ的活化能Ea(正) ___________ Ea(逆)(填“>”或“<”), 的数值范围是
的数值范围是___________ 。
A.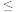 2 B.-2~0 C.0~2 D.>2
2 B.-2~0 C.0~2 D.>2
(2)工业上利用CO2氧化乙苯制苯乙烯的反应为:

①催化剂MxOy作用下,该反应可能存在如下图所示反应机理:

写出该机理表示的两个基元反应:
ⅰ:___________ 。
ⅱ:___________ 。
②常压下,乙苯和CO2在催化剂MxOy作用下反应。控制投料比[n(CO2):n(乙苯)]分别为1:1、5:1和10:1,乙苯平衡转化率与反应温度的关系如下图所示:

乙苯平衡转化率相同时,投料比越高,对应的反应温度越___________ (填“高”或“低”)。相同温度下,投料比远大于10:1时,乙苯的消耗速率明显下降,可能的原因是___________ 。
③700K时,向恒容密闭容器中加入过量CaCO3和一定量乙苯,初始和平衡时容器内压强分别为p1kPa和p2kPa,则平衡时苯乙烯的分压为___________ kPa(以含有p1、p2、p3的代数式表示)。[已知:CaCO3(s) CaO(s)+CO2(g) Kp=p3kPa]
CaO(s)+CO2(g) Kp=p3kPa]
(1)平衡常数K能为化学工作者提供许多信息。
实验测得下列3个反应的平衡常数K与温度T的函数关系如下:
| 序号 | 化学反应 | K与T的关系(c1、c2、c3为常数) |
| Ⅰ | 2O3(g) 3O2(g) △H1 3O2(g) △H1 | 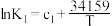 |
| Ⅱ | 4NO2(g)+O2(g) 2N2O5(g) △H2 2N2O5(g) △H2 | 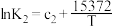 |
| Ⅲ | 2NO2(g)+O3(g) N2O5(g)+O2(g) △H3 N2O5(g)+O2(g) △H3 | 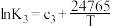 |
 的数值范围是
的数值范围是A.
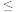 2 B.-2~0 C.0~2 D.>2
2 B.-2~0 C.0~2 D.>2(2)工业上利用CO2氧化乙苯制苯乙烯的反应为:

①催化剂MxOy作用下,该反应可能存在如下图所示反应机理:

写出该机理表示的两个基元反应:
ⅰ:
ⅱ:
②常压下,乙苯和CO2在催化剂MxOy作用下反应。控制投料比[n(CO2):n(乙苯)]分别为1:1、5:1和10:1,乙苯平衡转化率与反应温度的关系如下图所示:

乙苯平衡转化率相同时,投料比越高,对应的反应温度越
③700K时,向恒容密闭容器中加入过量CaCO3和一定量乙苯,初始和平衡时容器内压强分别为p1kPa和p2kPa,则平衡时苯乙烯的分压为
 CaO(s)+CO2(g) Kp=p3kPa]
CaO(s)+CO2(g) Kp=p3kPa]
您最近一年使用:0次
2 . 硫和氮是生物必须的营养元素,含硫和氮的化合物在自然界中广泛存在。
(1)火山喷发产生H2S在大气中发生如下反应:
①2H2S(g)+O2(g)=2S(g)+2H2O(l) △H=akJ•mol-1
②S(g)+O2(g)=SO2(g) △H=bkJ•mol-1
写出H2S(g)燃烧的热化学方程式_____ 。
(2)工业上可用NaClO碱性溶液吸收SO2。为了提高吸收效率,常用Ni2O3作为催化剂。反应过程中产生的四价镍和原子氧具有极强的氧化能力,可加快对SO2的吸收。该催化过程的示意图如图所示。Ca(ClO)2也可用于脱硫,且脱硫效果比NaClO更好,原因是______ 。

(3)氮的氧化物脱除可以利用电化学原理处理,利用如图所示装置可同时吸收SO2和NO。
已知:H2S2O4是一种弱酸。

①阴极的电极反应式为_____ 。
②若无能量损失,相同条件下,SO2和NO的体积比为_____ 时,两种气体都能被完全处理。
(4)已知2NO(g)+O2(g) 2NO2(g)的反应历程分两步。
2NO2(g)的反应历程分两步。
第一步:2NO(g)+ N2O2(g)(快反应)
N2O2(g)(快反应)
第二步:N2O2(g)+O2(g) 2NO2(g)(慢反应)
2NO2(g)(慢反应)
用O2表示的速率方程为v(O2)=k1c2(NO)•c(O2);用NO2表示的速率方程为v(NO2)=k2c2(NO)•c(O2),k1与k2分别表示速率常数,则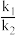 =
=_____ 。(填数值)
(5)太阳能光电催化—化学耦合分解H2S的装置如图所示。

①该太阳能光电催化—化学耦合分解H2S的过程可描述为______ 。
②从能源利用和资源综合利用角度分析该方法优点是______ 。
(1)火山喷发产生H2S在大气中发生如下反应:
①2H2S(g)+O2(g)=2S(g)+2H2O(l) △H=akJ•mol-1
②S(g)+O2(g)=SO2(g) △H=bkJ•mol-1
写出H2S(g)燃烧的热化学方程式
(2)工业上可用NaClO碱性溶液吸收SO2。为了提高吸收效率,常用Ni2O3作为催化剂。反应过程中产生的四价镍和原子氧具有极强的氧化能力,可加快对SO2的吸收。该催化过程的示意图如图所示。Ca(ClO)2也可用于脱硫,且脱硫效果比NaClO更好,原因是

(3)氮的氧化物脱除可以利用电化学原理处理,利用如图所示装置可同时吸收SO2和NO。
已知:H2S2O4是一种弱酸。

①阴极的电极反应式为
②若无能量损失,相同条件下,SO2和NO的体积比为
(4)已知2NO(g)+O2(g)
 2NO2(g)的反应历程分两步。
2NO2(g)的反应历程分两步。第一步:2NO(g)+
 N2O2(g)(快反应)
N2O2(g)(快反应)第二步:N2O2(g)+O2(g)
 2NO2(g)(慢反应)
2NO2(g)(慢反应)用O2表示的速率方程为v(O2)=k1c2(NO)•c(O2);用NO2表示的速率方程为v(NO2)=k2c2(NO)•c(O2),k1与k2分别表示速率常数,则
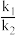 =
=(5)太阳能光电催化—化学耦合分解H2S的装置如图所示。

①该太阳能光电催化—化学耦合分解H2S的过程可描述为
②从能源利用和资源综合利用角度分析该方法优点是
您最近一年使用:0次
名校
3 . "碳达峰”“碳中和”是我国社会发展重大战略之一
I.中国首次实现了利用二氧化碳人工合成淀粉,其中最关键的一步是以CO2为原料制CH3OH.在某CO2催化加氢制CH3OH的反应体系中,发生的主要反应有:
①CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41.1kJmol-1
CO(g)+H2O(g) △H1=+41.1kJmol-1
②CO(g)+2H2(g) CH3OH(g) △H2=-90.0kJmol-1
CH3OH(g) △H2=-90.0kJmol-1
③CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3=-48.9kJmol-1
CH3OH(g)+H2O(g) △H3=-48.9kJmol-1
(1)5Mpa时,往某密闭容器中按投料比n(H2):n(CO2)=3:1充入H2和CO2反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
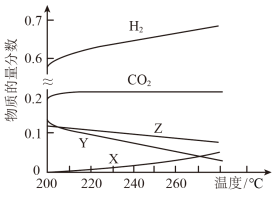
①图中Y代表___________ (填化学式)。
②体系中CO2的物质的量分数受温度影响不大,原因是___________ 。
II.CH4还原CO2是实现“双碳”经济的有效途径之一,相关的主要反应有:
①CH4(g)+CO2(g) 2CO(g)+2H2(g) K1
2CO(g)+2H2(g) K1
②CO2(g)+H2(g) CO(g)+H2O(g) K2
CO(g)+H2O(g) K2
请回答:
(2)反应CH4(g)+3CO2(g) 4CO(g)+2H2O(g)的K=
4CO(g)+2H2O(g)的K=___________ (用K1,K2表示)。
(3)恒压,750°C时,CH4和CO2按物质的量之比1:3投料,经如下流程可实现CO2高效转化。
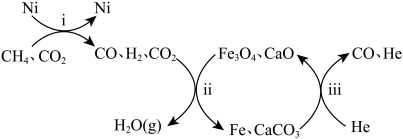
①写出过程ii产生H2O(g)的化学方程式___________ 。
②过程ii的催化剂是___________ ,若CH4和CO2按物质的量之比1:1投料,则会导致过程ii___________ 。
③过程ii平衡后通入稀有气体He,测得一段时间内CO物质的量上升,根据过程iii,结合平衡移动原理,解释CO物质的量上升的原因___________ 。
I.中国首次实现了利用二氧化碳人工合成淀粉,其中最关键的一步是以CO2为原料制CH3OH.在某CO2催化加氢制CH3OH的反应体系中,发生的主要反应有:
①CO2(g)+H2(g)
 CO(g)+H2O(g) △H1=+41.1kJmol-1
CO(g)+H2O(g) △H1=+41.1kJmol-1②CO(g)+2H2(g)
 CH3OH(g) △H2=-90.0kJmol-1
CH3OH(g) △H2=-90.0kJmol-1③CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3=-48.9kJmol-1
CH3OH(g)+H2O(g) △H3=-48.9kJmol-1(1)5Mpa时,往某密闭容器中按投料比n(H2):n(CO2)=3:1充入H2和CO2反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。

①图中Y代表
②体系中CO2的物质的量分数受温度影响不大,原因是
II.CH4还原CO2是实现“双碳”经济的有效途径之一,相关的主要反应有:
①CH4(g)+CO2(g)
 2CO(g)+2H2(g) K1
2CO(g)+2H2(g) K1②CO2(g)+H2(g)
 CO(g)+H2O(g) K2
CO(g)+H2O(g) K2请回答:
(2)反应CH4(g)+3CO2(g)
 4CO(g)+2H2O(g)的K=
4CO(g)+2H2O(g)的K=(3)恒压,750°C时,CH4和CO2按物质的量之比1:3投料,经如下流程可实现CO2高效转化。

①写出过程ii产生H2O(g)的化学方程式
②过程ii的催化剂是
③过程ii平衡后通入稀有气体He,测得一段时间内CO物质的量上升,根据过程iii,结合平衡移动原理,解释CO物质的量上升的原因
您最近一年使用:0次
20-21高三上·江苏扬州·开学考试
4 . H2O2在Fe2+、Cu2+的存在下生成具有强氧化性的·OH(羟基自由基),·OH可将有机物氧化降解。
(1)Cu2+-H2O2体系中存在下列反应:
Cu2+(aq)+H2O2(aq)= CuOOH+(aq)+H+(aq) ΔH1=a kJ·mol-1
CuOOH+(aq)=Cu+(aq)+·OH(aq)+ O2(g) ΔH2=b kJ·mol-1
O2(g) ΔH2=b kJ·mol-1
2CuOOH+(aq)=2Cu+(aq)+H2O2(aq)+O2(g) ΔH3=c kJ·mol-1
则H2O2(aq)=2·OH(aq) ΔH=________ kJ·mol-1。
(2)为探究Fe2+-Cu2+-H2O2能够协同催化氧化降解甲基橙,某研究小组的实验结果如图1所示。得出“Fe2+-Cu2+-H2O2催化氧化降解甲基橙效果优于单独加入Fe2+或Cu2+”结论的证据为_______ 。
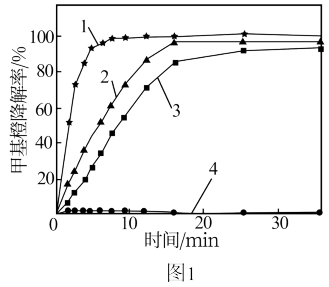
实验条件:200 mL甲基橙模拟废水(1.5 g·L-1,pH=3.0),温度60 ℃、V(H2O2)=2.0 mL
1—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0.4
2—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0
3—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0.4
4—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0
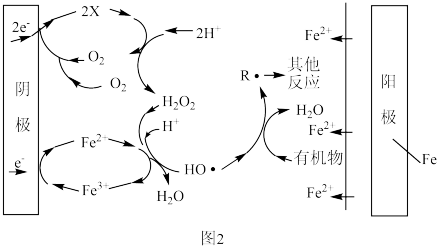
(3)EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如图2所示。阳极的电极反应式为______ ,X微粒的化学式为________ ,阴极附近Fe2+参与反应的离子方程式为_______ 。
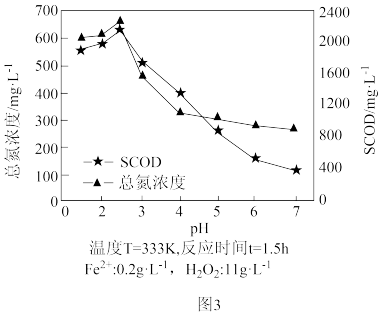
(4)SCOD是指溶解性化学需氧量,是衡量水中有机物质含量多少的指标。水体SCOD越大,说明其有机物含量越高。用Fe2+-H2O2法氧化破解啤酒工业污泥中的微生物,释放出有机物和氮等。测得不同初始pH下污泥经氧化破解后上层清液中的SCOD及总氮浓度如图3所示。当pH>2.5时,总氮浓度、SCOD均降低,其原因可能是__________ 。
(1)Cu2+-H2O2体系中存在下列反应:
Cu2+(aq)+H2O2(aq)= CuOOH+(aq)+H+(aq) ΔH1=a kJ·mol-1
CuOOH+(aq)=Cu+(aq)+·OH(aq)+
 O2(g) ΔH2=b kJ·mol-1
O2(g) ΔH2=b kJ·mol-12CuOOH+(aq)=2Cu+(aq)+H2O2(aq)+O2(g) ΔH3=c kJ·mol-1
则H2O2(aq)=2·OH(aq) ΔH=
(2)为探究Fe2+-Cu2+-H2O2能够协同催化氧化降解甲基橙,某研究小组的实验结果如图1所示。得出“Fe2+-Cu2+-H2O2催化氧化降解甲基橙效果优于单独加入Fe2+或Cu2+”结论的证据为

实验条件:200 mL甲基橙模拟废水(1.5 g·L-1,pH=3.0),温度60 ℃、V(H2O2)=2.0 mL
1—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0.4
2—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0
3—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0.4
4—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0
(3)EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如图2所示。阳极的电极反应式为

(4)SCOD是指溶解性化学需氧量,是衡量水中有机物质含量多少的指标。水体SCOD越大,说明其有机物含量越高。用Fe2+-H2O2法氧化破解啤酒工业污泥中的微生物,释放出有机物和氮等。测得不同初始pH下污泥经氧化破解后上层清液中的SCOD及总氮浓度如图3所示。当pH>2.5时,总氮浓度、SCOD均降低,其原因可能是

您最近一年使用:0次
21-22高三下·江苏·开学考试
5 . 燃煤烟气中SO2和NOx是大气污染物的主要来源,脱硫脱硝技术是烟气治理技术的研究热点。
(1)尿素/H2O2溶液脱硫脱硝。尿素[CO(NH2)2]是一种强还原剂。60℃时在一定浓度的尿素/H2O2溶液中通入含有SO2和NO的烟气,烟气中有毒气体被一定程度吸收。尿素/H2O2溶液对SO2具有很高的去除效率,写出尿素和H2O2溶液吸收SO2,生成硫酸铵和CO2的化学方程式为____ 。
(2)除去烟气中的NOx,利用氢气选择性催化还原(H2—SCR)是目前消除NO的理想方法。H2—SCR法的主反应:2NO(g)+2H2(g)=N2(g)+2H2O(g) △H1
副反应:2NO(g)+H2(g)=N2O(g)+H2O(g) △H2<0
①已知H2(g)+ O2(g)=H2O(g) △H3=-241.5kJ·mol-1
O2(g)=H2O(g) △H3=-241.5kJ·mol-1
N2(g)+O2(g)=2NO(g) △H4=+180.5kJ·mol-1
则△H1=____ kJ·mol-1。
②H2—SCR在Pt—HY催化剂表面的反应机理如图所示:
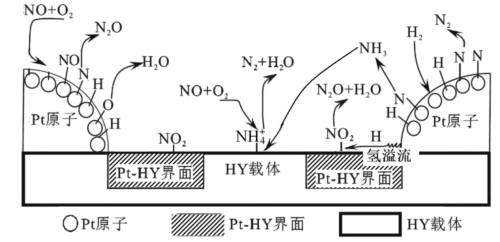
已知在HY载体表面发生反应的NO、O2物质的量之比为4∶1,反应中每生成1molN2,转移的电子的物质的量为___ mol。
(3)V2O5/炭基材料(活性炭、活性焦、活炭纤维)也可以脱硫脱硝。V2O5/炭基材料脱硫原理是:SO2在炭表面被吸附,吸附态SO2在炭表面被催化氧化为SO3,SO3再转化为硫酸盐等。
①V2O5/炭基材料脱硫时,通过红外光谱发现,脱硫开始后催化剂表面出现了VOSO4的吸收峰,再通入O2后VOSO4吸收峰消失,该脱硫反应过程可描述为____ 。
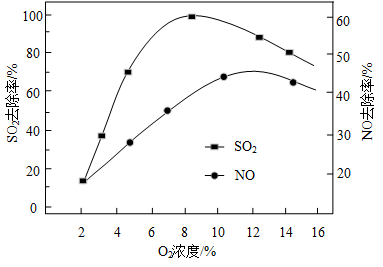
②V2O5/炭基材料脱硫时,控制一定气体流速和温度,考察了烟气中O2的存在对V2O5/炭基材料催化剂脱硫脱硝活性的影响,结果如图所示,当O2浓度过高时,去除率下降,其可能原因是_____ 。
(1)尿素/H2O2溶液脱硫脱硝。尿素[CO(NH2)2]是一种强还原剂。60℃时在一定浓度的尿素/H2O2溶液中通入含有SO2和NO的烟气,烟气中有毒气体被一定程度吸收。尿素/H2O2溶液对SO2具有很高的去除效率,写出尿素和H2O2溶液吸收SO2,生成硫酸铵和CO2的化学方程式为
(2)除去烟气中的NOx,利用氢气选择性催化还原(H2—SCR)是目前消除NO的理想方法。H2—SCR法的主反应:2NO(g)+2H2(g)=N2(g)+2H2O(g) △H1
副反应:2NO(g)+H2(g)=N2O(g)+H2O(g) △H2<0
①已知H2(g)+
 O2(g)=H2O(g) △H3=-241.5kJ·mol-1
O2(g)=H2O(g) △H3=-241.5kJ·mol-1N2(g)+O2(g)=2NO(g) △H4=+180.5kJ·mol-1
则△H1=
②H2—SCR在Pt—HY催化剂表面的反应机理如图所示:

已知在HY载体表面发生反应的NO、O2物质的量之比为4∶1,反应中每生成1molN2,转移的电子的物质的量为
(3)V2O5/炭基材料(活性炭、活性焦、活炭纤维)也可以脱硫脱硝。V2O5/炭基材料脱硫原理是:SO2在炭表面被吸附,吸附态SO2在炭表面被催化氧化为SO3,SO3再转化为硫酸盐等。
①V2O5/炭基材料脱硫时,通过红外光谱发现,脱硫开始后催化剂表面出现了VOSO4的吸收峰,再通入O2后VOSO4吸收峰消失,该脱硫反应过程可描述为
②V2O5/炭基材料脱硫时,控制一定气体流速和温度,考察了烟气中O2的存在对V2O5/炭基材料催化剂脱硫脱硝活性的影响,结果如图所示,当O2浓度过高时,去除率下降,其可能原因是

您最近一年使用:0次
2022-03-05更新
|
1516次组卷
|
7卷引用:黄金卷7-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)
(已下线)黄金卷7-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)(已下线)必刷卷02-2022年高考化学考前信息必刷卷(江苏专用)江苏南京师范大学附属中学2022-2023学年高三一模适应性考试化学试题(已下线)化学-2023年高考押题预测卷03(江苏卷)(含考试版、全解全析、参考答案、答题卡)江苏省六校2021-2022学年高三下学期期初联合调研考试化学试题(已下线)秘籍15 反应热、盖斯定律应用及图象分析-备战2022年高考化学抢分秘籍(全国通用)(已下线)专题17 原理综合题
名校
6 . 有机物催化脱氢制备氢气和化工原料是当前石化工业研究的重要课题之一、
(1)以甲烷、水蒸气为原料进行催化重整是制氢的常见方法之一,过程可能涉及反应:
CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2 kJ∙mol−1
CO(g)+H2O(g)=CO2(g)+H2(g) △H2=−41.1 kJ∙mol−1
CH4(g)=C(g)+2H2(g) △H3=+74.8 kJ∙mol−1
①反应C(g)+2H2O(g)=CO2(g)+2H2(g) △H4=___________ kJ·mol-1
②向原料中添加正硅酸锂Li4SiO4作为CO2的吸附剂,除产生氢气外还生成两种盐,写出该反应的方程式___________ 。
(2)甲基环己烷催化脱氢(

 +3H2)是石油工业制氢常见方法,以Ni−Cu为催化剂,固定反应温度为650K,以氮气为载气,在不同载气流速情况下,甲基环己烷脱氢转化率如图1所示,b点转化率能与a点保持相当的原因是
+3H2)是石油工业制氢常见方法,以Ni−Cu为催化剂,固定反应温度为650K,以氮气为载气,在不同载气流速情况下,甲基环己烷脱氢转化率如图1所示,b点转化率能与a点保持相当的原因是___________ 。

(3)以H2O、CaBr2、Fe3O4为原料进行气固相反应可以实现水的分解制得氢气,其反应原理如图2所示。反应“①”中生成3molHBr,生成氢气的物质的量为_______ ,从原料到O2的生成过程可描述为_______ 。
(1)以甲烷、水蒸气为原料进行催化重整是制氢的常见方法之一,过程可能涉及反应:
CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2 kJ∙mol−1
CO(g)+H2O(g)=CO2(g)+H2(g) △H2=−41.1 kJ∙mol−1
CH4(g)=C(g)+2H2(g) △H3=+74.8 kJ∙mol−1
①反应C(g)+2H2O(g)=CO2(g)+2H2(g) △H4=
②向原料中添加正硅酸锂Li4SiO4作为CO2的吸附剂,除产生氢气外还生成两种盐,写出该反应的方程式
(2)甲基环己烷催化脱氢(


 +3H2)是石油工业制氢常见方法,以Ni−Cu为催化剂,固定反应温度为650K,以氮气为载气,在不同载气流速情况下,甲基环己烷脱氢转化率如图1所示,b点转化率能与a点保持相当的原因是
+3H2)是石油工业制氢常见方法,以Ni−Cu为催化剂,固定反应温度为650K,以氮气为载气,在不同载气流速情况下,甲基环己烷脱氢转化率如图1所示,b点转化率能与a点保持相当的原因是
(3)以H2O、CaBr2、Fe3O4为原料进行气固相反应可以实现水的分解制得氢气,其反应原理如图2所示。反应“①”中生成3molHBr,生成氢气的物质的量为
您最近一年使用:0次
2021-12-14更新
|
970次组卷
|
4卷引用:江苏省南通市海门区2021-2022学年高三第二次诊断测试化学试题
江苏省南通市海门区2021-2022学年高三第二次诊断测试化学试题(已下线)黄金卷6-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)江苏省南京市第九中学2023-2024学年高二上学期期末化学试卷(已下线)秘籍15 反应热、盖斯定律应用及图象分析-备战2022年高考化学抢分秘籍(全国通用)
7 . H2O2在Fe2+、Cu2+的存在下生成具有强氧化性的•OH(羟基自由基),•OH可将有机物氧化降解。
(1)Cu2+H2O2体系中存在下列反应:
Cu2+(aq)+H2O2(aq)═CuOOH+(aq)+H+(aq)△H1=a kJ•mol﹣1
CuOOH+(aq)═Cu+(aq)+•OH(aq)+1/2O2(g)△H2=b kJ•mol﹣1
2CuOOH+(aq)═2Cu+(aq)+H2O2(aq)+O2(g)△H3=c kJ•mol﹣1
则H2O2(aq)═2•OH(aq)△H=_____ kJ•mol﹣1。
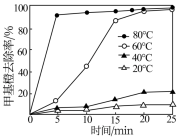
(2)为探究温度对Cu2+H2O2甲基橙去除率的影响,某研究小组在不同温度下进行实验(其他条件相同),实验结果如图所示。相同条件下,温度升高,甲基橙去除速率增大,其原因是_____ 。
(3)为探究Fe2+Cu2+H2O2能够协同催化氧化降解甲基橙,某研究小组的实验结果如图所示。得出“Fe2+Cu2+H2O2催化氧化降解甲基橙效果优于单独加入Fe2+或Cu2+”结论的证据为_____ 。
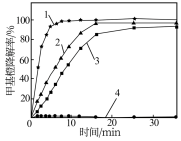
实验条件:200 mL甲基橙模拟废水(1.5 g•L﹣1,pH=3.0),温度60℃、V(H2O2)=2.0 mL
1﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0.02:0.4
2﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0.02:0
3﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0:0.4
4﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0:0
(4)EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如下图所示。阳极的电极反应式为_____ ,X微粒的化学式为_____ ,阴极附近Fe2+参与反应的离子方程式为_____ 。
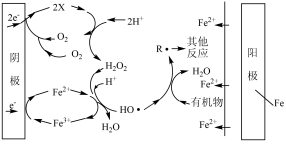
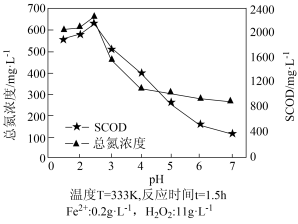
(5)SCOD是指溶解性化学需氧量,是衡量水中有机物质含量多少的指标。水体SCOD越大,说明其有机物含量越高。用Fe2+H2O2法氧化破解啤酒工业污泥中的微生物,释放出有机物和氮等。测得不同初始pH下污泥经氧化破解后上层清液中的SCOD及总氮浓度如上图所示。当pH>2.5时,总氮浓度、SCOD均降低,其原因可能是_____ 。
(1)Cu2+H2O2体系中存在下列反应:
Cu2+(aq)+H2O2(aq)═CuOOH+(aq)+H+(aq)△H1=a kJ•mol﹣1
CuOOH+(aq)═Cu+(aq)+•OH(aq)+1/2O2(g)△H2=b kJ•mol﹣1
2CuOOH+(aq)═2Cu+(aq)+H2O2(aq)+O2(g)△H3=c kJ•mol﹣1
则H2O2(aq)═2•OH(aq)△H=

(2)为探究温度对Cu2+H2O2甲基橙去除率的影响,某研究小组在不同温度下进行实验(其他条件相同),实验结果如图所示。相同条件下,温度升高,甲基橙去除速率增大,其原因是
(3)为探究Fe2+Cu2+H2O2能够协同催化氧化降解甲基橙,某研究小组的实验结果如图所示。得出“Fe2+Cu2+H2O2催化氧化降解甲基橙效果优于单独加入Fe2+或Cu2+”结论的证据为

实验条件:200 mL甲基橙模拟废水(1.5 g•L﹣1,pH=3.0),温度60℃、V(H2O2)=2.0 mL
1﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0.02:0.4
2﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0.02:0
3﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0:0.4
4﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0:0
(4)EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如下图所示。阳极的电极反应式为


(5)SCOD是指溶解性化学需氧量,是衡量水中有机物质含量多少的指标。水体SCOD越大,说明其有机物含量越高。用Fe2+H2O2法氧化破解啤酒工业污泥中的微生物,释放出有机物和氮等。测得不同初始pH下污泥经氧化破解后上层清液中的SCOD及总氮浓度如上图所示。当pH>2.5时,总氮浓度、SCOD均降低,其原因可能是
您最近一年使用:0次
2011·江苏南京·模拟预测
解题方法
8 . 现代炼锌的方法可分为火法(蒸馏法)和湿法(电解法)两大类。
(1)以上三个反应中,一定是放热反应的是______________ (填序号)。
(2)反应:ZnS(s)+C(s)+2O2(g)=Zn(g)+SO2(g)+CO2(g) ΔH=____________ kJ·mol-1。
Ⅱ. 湿法炼锌工艺如下:
(3)写出“浸出”主要反应的离子方程式:__________________________ 。
(4)“电解”获得锌的电极反应为______________________ 。
(5)该工艺中可循环利用的物质是______________________________ (填化学式)。
(1)以上三个反应中,一定是放热反应的是
(2)反应:ZnS(s)+C(s)+2O2(g)=Zn(g)+SO2(g)+CO2(g) ΔH=
Ⅱ. 湿法炼锌工艺如下:

(3)写出“浸出”主要反应的离子方程式:
(4)“电解”获得锌的电极反应为
(5)该工艺中可循环利用的物质是
您最近一年使用:0次
名校
9 . 氮的化合物合成、应用及氮的固定一直是科学研究的热点。
(1) 以CO2与NH3为原料合成化肥尿素的主要反应如下:
① 2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47 kJ·mol−1
② NH2CO2NH4(s)=CO (NH2)2(s)+H2O(g);ΔH=a kJ·mol−1
③ 2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);ΔH=-86.98 kJ·mol−1
则a为____ 。
(2) 尿素可用于湿法烟气脱氮工艺,其反应原理为:NO+NO2+H2O=2HNO2;2HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O。
① 当烟气中NO、NO2按上述反应中系数比时脱氮效果最佳。若烟气中V(NO)∶V(NO2)=5∶1时,可通入一定量的空气,同温同压下,V(空气)∶V(NO)=____ (空气中氧气的体积含量大约为20%)。
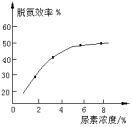
② 如图表示尿素含量对脱氮效率的影响,从经济因素上考虑,一般选择尿素浓度约为____ %。
(3)用稀硝酸吸收NOx,得到HNO3和HNO2(弱酸)的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:____ 。
(4)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图所示。
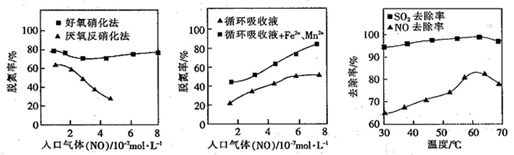
① 由图知,当废气中的NO含量增加时,宜选用____ 法提高脱氮的效率。
② 图Ⅱ中,循环吸收液加入Fe2+、Mn2+,提高了脱氮的效率,其可能原因为____ 。
(5)研究表明:NaClO/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。温度高于60℃后,NO去除率下降的原因为____ 。
(1) 以CO2与NH3为原料合成化肥尿素的主要反应如下:
① 2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47 kJ·mol−1
② NH2CO2NH4(s)=CO (NH2)2(s)+H2O(g);ΔH=a kJ·mol−1
③ 2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);ΔH=-86.98 kJ·mol−1
则a为
(2) 尿素可用于湿法烟气脱氮工艺,其反应原理为:NO+NO2+H2O=2HNO2;2HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O。
① 当烟气中NO、NO2按上述反应中系数比时脱氮效果最佳。若烟气中V(NO)∶V(NO2)=5∶1时,可通入一定量的空气,同温同压下,V(空气)∶V(NO)=
② 如图表示尿素含量对脱氮效率的影响,从经济因素上考虑,一般选择尿素浓度约为

(3)用稀硝酸吸收NOx,得到HNO3和HNO2(弱酸)的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:
(4)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图所示。

① 由图知,当废气中的NO含量增加时,宜选用
② 图Ⅱ中,循环吸收液加入Fe2+、Mn2+,提高了脱氮的效率,其可能原因为
(5)研究表明:NaClO/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。温度高于60℃后,NO去除率下降的原因为
您最近一年使用:0次
2018-12-16更新
|
337次组卷
|
2卷引用:【市级联考】江苏省南京市六校联合体2019届高三上学期12月联考化学试题
10 . (1) 已知: CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1 = akJ/mol;
CO(g) + H2O (g)=CO2(g) + H2 (g) △H2 = bkJ/mol;
2CO(g) + O2(g)= 2CO2(g) △H3 = ckJ/mol;
反应CO2(g)+ CH4(g)=2CO(g) + 2H2(g) 的△H =_____ kJ/mol;
(2) 科学家用氮化镓材料与铜组装如图10的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4。

①写出铜电极表面的电极反应式_____________ 。
②为提高该人工光合系统的工作效率,可向装置中加入少量_______ (选填“盐酸”或“硫酸”)。
(3) 天然气中的H2S 杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS 溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式___________ 。
(4) 将甲烷和硫反应可以制备CS2,其流程如图11所示:
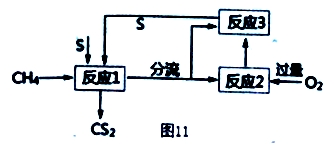
①写出发生反应1的化学反应方程式___________ 。
②反应1产生两种含硫的物质,为了提高CS2的产率,设计反应2和3实现硫单质循环利用,实验时需对反应1出来的气体分流,则进入反应2 和反应3 的气体物质的量之比为___________ 。
③当反应1中每有1molCS2生成时,反应2中需要消耗O2的物质的量为___________ 。
CO(g) + H2O (g)=CO2(g) + H2 (g) △H2 = bkJ/mol;
2CO(g) + O2(g)= 2CO2(g) △H3 = ckJ/mol;
反应CO2(g)+ CH4(g)=2CO(g) + 2H2(g) 的△H =
(2) 科学家用氮化镓材料与铜组装如图10的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4。

①写出铜电极表面的电极反应式
②为提高该人工光合系统的工作效率,可向装置中加入少量
(3) 天然气中的H2S 杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS 溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式
(4) 将甲烷和硫反应可以制备CS2,其流程如图11所示:

①写出发生反应1的化学反应方程式
②反应1产生两种含硫的物质,为了提高CS2的产率,设计反应2和3实现硫单质循环利用,实验时需对反应1出来的气体分流,则进入反应2 和反应3 的气体物质的量之比为
③当反应1中每有1molCS2生成时,反应2中需要消耗O2的物质的量为
您最近一年使用:0次



