名校
解题方法
1 . 已知氮元素及其化合物的转化关系如下图所示,回答下列问题。_______ 。
(2)反应④的离子方程式为_______ 。理论上如图N2合成1mol硝酸,至少需要氧气共_______ mol。
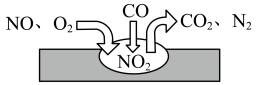
(3)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示,该过程的总反应化学方程式为_______ 。
①根据上图得知_______ (填字母)。
A.NaOH溶液浓度越大,氮氧化物的吸收率越大
B.NO2含量越大,氮氧化物的吸收率越大
②当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是_______ 。

(2)反应④的离子方程式为
(3)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示,该过程的总反应化学方程式为

①根据上图得知
A.NaOH溶液浓度越大,氮氧化物的吸收率越大
B.NO2含量越大,氮氧化物的吸收率越大
②当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是
您最近半年使用:0次
名校
解题方法
2 . 二甲醚(DME)被誉为“21世纪的清洁燃料”,由合成气制备二甲醚的主要原理如下:
①
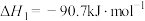

②
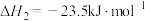

③
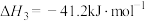

回答下列问题:
(1)反应 的平衡常数K=
的平衡常数K=________ (用 、
、 、
、 表示)。
表示)。
(2)在保持反应物投料不变的情况下,请写出一条提高甲醇产率的措施________ 。
(3)一定温度下,将0.2molCO和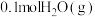 通入2L恒容密闭容器中,发生反应③,5min后达到化学平衡,平衡后测得
通入2L恒容密闭容器中,发生反应③,5min后达到化学平衡,平衡后测得 的体积分数为0.1。则0~5min内
的体积分数为0.1。则0~5min内
________ ,CO的转化率为________ 。
(4)将合成气以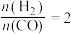 通入1L的反应器中,一定条件下发生反应:
通入1L的反应器中,一定条件下发生反应:
 ,其中CO的平衡转化率随温度、压强的变化关系如图1所示。下列说法正确的是
,其中CO的平衡转化率随温度、压强的变化关系如图1所示。下列说法正确的是________ (填字母)。 B.
B.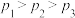 C.若在
C.若在 和316℃时,起始时
和316℃时,起始时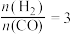 ,则平衡时,α(CO)小于50%
,则平衡时,α(CO)小于50%
(5)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和 制备二甲醚(DME)。观察图2,当
制备二甲醚(DME)。观察图2,当 约为
约为________ 时最有利于二甲醚的合成。
①

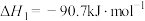

②

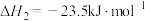

③

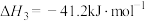

回答下列问题:
(1)反应
 的平衡常数K=
的平衡常数K= 、
、 、
、 表示)。
表示)。(2)在保持反应物投料不变的情况下,请写出一条提高甲醇产率的措施
(3)一定温度下,将0.2molCO和
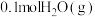 通入2L恒容密闭容器中,发生反应③,5min后达到化学平衡,平衡后测得
通入2L恒容密闭容器中,发生反应③,5min后达到化学平衡,平衡后测得 的体积分数为0.1。则0~5min内
的体积分数为0.1。则0~5min内
(4)将合成气以
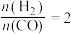 通入1L的反应器中,一定条件下发生反应:
通入1L的反应器中,一定条件下发生反应:
 ,其中CO的平衡转化率随温度、压强的变化关系如图1所示。下列说法正确的是
,其中CO的平衡转化率随温度、压强的变化关系如图1所示。下列说法正确的是
图1
A. B.
B.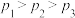 C.若在
C.若在 和316℃时,起始时
和316℃时,起始时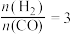 ,则平衡时,α(CO)小于50%
,则平衡时,α(CO)小于50%(5)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和
 制备二甲醚(DME)。观察图2,当
制备二甲醚(DME)。观察图2,当 约为
约为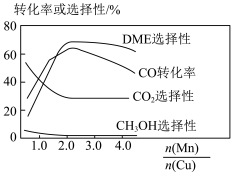
图2
您最近半年使用:0次
名校
3 . 工业及汽车尾气已成为城市空气的主要污染源,研究其反应机理对于环境治理有重要意义。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0 kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ/mol
4NO2(g)+O2(g)+2H2O(g)=4HNO3(g) △H=___________ kJ/mol。
(2)液氨催化还原NO是重要的烟气脱硝技术。使用Fe2O3为催化剂,可能的反应过程如图所示。___________ 。
②反应过程图中,虚线方框里的过程可描述为___________ 。
③氨氮比会直接影响该方法的脱硝率。350℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系如图所示。当 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是___________ 。
NO2被Na2CO3溶液吸收生成的三种盐分别是NaNO2、NaNO3和___________ 。(填化学式)
(4)NSR (NOX储存还原)可有效减少氮氧化物排放。工作原理:通过BaO和Ba(NO3)2的相互转化实现NOX的储存和还原,如图所示。___________ 。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0 kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ/mol
4NO2(g)+O2(g)+2H2O(g)=4HNO3(g) △H=
(2)液氨催化还原NO是重要的烟气脱硝技术。使用Fe2O3为催化剂,可能的反应过程如图所示。
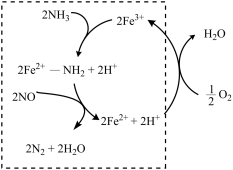
②反应过程图中,虚线方框里的过程可描述为
③氨氮比会直接影响该方法的脱硝率。350℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系如图所示。当
 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是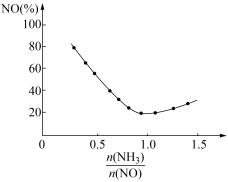
NO2被Na2CO3溶液吸收生成的三种盐分别是NaNO2、NaNO3和
(4)NSR (NOX储存还原)可有效减少氮氧化物排放。工作原理:通过BaO和Ba(NO3)2的相互转化实现NOX的储存和还原,如图所示。
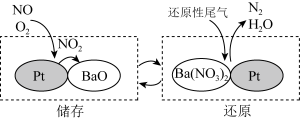
您最近半年使用:0次
名校
4 . 完成下列填空:
(1) 气态高能燃料乙硼烷
气态高能燃料乙硼烷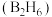 在氧气中燃烧,生成固态三氧化二硼和液态水放出
在氧气中燃烧,生成固态三氧化二硼和液态水放出 热量,其热化学方程式为:
热量,其热化学方程式为:___________ ;
(2)甲烷还原方法是在催化剂作用下可消除氮氧化物(主要为 和
和 )污染,
)污染, 和
和 的混合物反应体系主要发生如下反应:
的混合物反应体系主要发生如下反应:
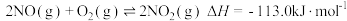 ①
①
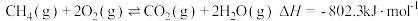 ②
②
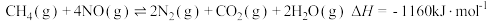 ③
③
则反应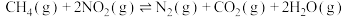 的
的
___________ 。
(3)天然气的一个重要用途是制取 ,其原理为:
,其原理为: 。
。
①该反应的平衡常数表达式为___________ 。
②在密闭容器中通入物质的量浓度均为 的
的 与
与 ,在一定条件下发生反应,测得
,在一定条件下发生反应,测得 的平衡转化率与温度及压强的关系如下图所示,则压强P1
的平衡转化率与温度及压强的关系如下图所示,则压强P1_______ P2(填"大于”或“小于”);压强为 时,在
时,在 点:v(正)
点:v(正)______ v(逆)(填“大于”、“小于”或“等于”)。 可以去除烟气中的
可以去除烟气中的 ,其反应原理如下:
,其反应原理如下: ;其他条件相同,以
;其他条件相同,以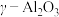 (一种多孔性物质,每克的内表面积高达数百平方米,具有良好的吸附性能)作为催化剂,研究表明,
(一种多孔性物质,每克的内表面积高达数百平方米,具有良好的吸附性能)作为催化剂,研究表明,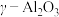 在240℃以上发挥催化作用。反应相同的时间,
在240℃以上发挥催化作用。反应相同的时间, 的去除率随反应温度的变化如下图所示。240℃以前,随着温度的升高,
的去除率随反应温度的变化如下图所示。240℃以前,随着温度的升高, 去除率降低的原因是
去除率降低的原因是___________ 。240℃以后,随着温度的升高, 去除率迅速增大的主要原因是
去除率迅速增大的主要原因是___________ 。 的资源化利用能有效减少
的资源化利用能有效减少 排放,实现自然界中的碳循环。
排放,实现自然界中的碳循环。 催化加氢合成甲烷过程中发生下列反应:
催化加氢合成甲烷过程中发生下列反应:
Ⅰ:
Ⅱ:
当 时,
时, 平衡转化率与温度和压强的关系如图所示。800℃时,不同压强下的
平衡转化率与温度和压强的关系如图所示。800℃时,不同压强下的 平衡转化率趋向于相等的原因是
平衡转化率趋向于相等的原因是___________ 。
(1)
 气态高能燃料乙硼烷
气态高能燃料乙硼烷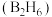 在氧气中燃烧,生成固态三氧化二硼和液态水放出
在氧气中燃烧,生成固态三氧化二硼和液态水放出 热量,其热化学方程式为:
热量,其热化学方程式为:(2)甲烷还原方法是在催化剂作用下可消除氮氧化物(主要为
 和
和 )污染,
)污染, 和
和 的混合物反应体系主要发生如下反应:
的混合物反应体系主要发生如下反应: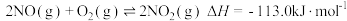 ①
①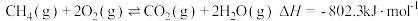 ②
②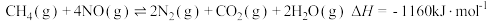 ③
③则反应
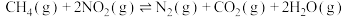 的
的
(3)天然气的一个重要用途是制取
 ,其原理为:
,其原理为: 。
。①该反应的平衡常数表达式为
②在密闭容器中通入物质的量浓度均为
 的
的 与
与 ,在一定条件下发生反应,测得
,在一定条件下发生反应,测得 的平衡转化率与温度及压强的关系如下图所示,则压强P1
的平衡转化率与温度及压强的关系如下图所示,则压强P1 时,在
时,在 点:v(正)
点:v(正)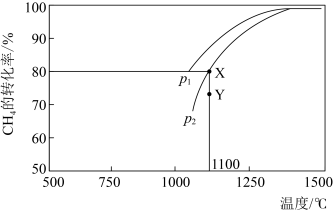
 可以去除烟气中的
可以去除烟气中的 ,其反应原理如下:
,其反应原理如下: ;其他条件相同,以
;其他条件相同,以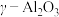 (一种多孔性物质,每克的内表面积高达数百平方米,具有良好的吸附性能)作为催化剂,研究表明,
(一种多孔性物质,每克的内表面积高达数百平方米,具有良好的吸附性能)作为催化剂,研究表明,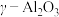 在240℃以上发挥催化作用。反应相同的时间,
在240℃以上发挥催化作用。反应相同的时间, 的去除率随反应温度的变化如下图所示。240℃以前,随着温度的升高,
的去除率随反应温度的变化如下图所示。240℃以前,随着温度的升高, 去除率降低的原因是
去除率降低的原因是 去除率迅速增大的主要原因是
去除率迅速增大的主要原因是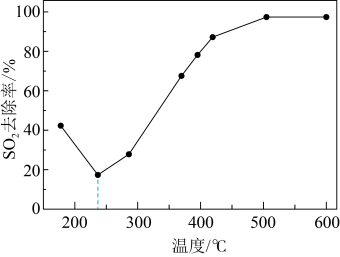
 的资源化利用能有效减少
的资源化利用能有效减少 排放,实现自然界中的碳循环。
排放,实现自然界中的碳循环。 催化加氢合成甲烷过程中发生下列反应:
催化加氢合成甲烷过程中发生下列反应:Ⅰ:

Ⅱ:

当
 时,
时, 平衡转化率与温度和压强的关系如图所示。800℃时,不同压强下的
平衡转化率与温度和压强的关系如图所示。800℃时,不同压强下的 平衡转化率趋向于相等的原因是
平衡转化率趋向于相等的原因是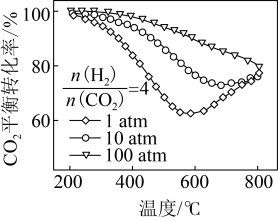
您最近半年使用:0次
名校
解题方法
5 . 我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和,而研发CO2的碳捕捉和碳利用技术则是关键。
Ⅰ.常温下,以NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
(1)用1L Na2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,再过滤,所用的Na2CO3溶液的物质的量浓度至少为___________ mol/L。[已知:常温下 ;忽略溶液体积变化]
;忽略溶液体积变化]
Ⅱ.CH4- CO2重整反应能够有效去除大气中CO2,是实现“碳中和”的重要途径之一,发生的反应如下:
重整反应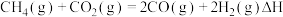
积炭反应Ⅰ: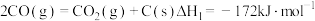
积炭反应Ⅱ:
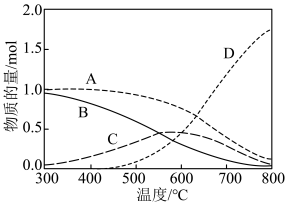
在恒压、起始投料比 条件下,体系中含碳组分、H2平衡时的物质的量随温度变化关系曲线如图所示。
条件下,体系中含碳组分、H2平衡时的物质的量随温度变化关系曲线如图所示。
(2)重整反应的反应热
___________ 。
(3)曲线C物质的量随温度的升高先升高后降低的原因是___________ 。
Ⅲ.铜基催化剂 (M为
(M为 等)是CO2加氢制甲醇常用的催化剂,部分合成路线如图所示。
等)是CO2加氢制甲醇常用的催化剂,部分合成路线如图所示。
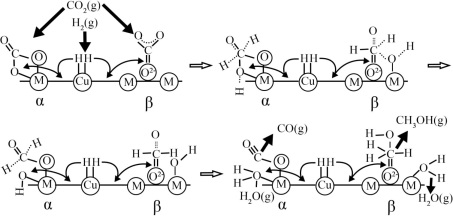
其中催化剂上有两个活动点位(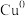 位点、氧化物载体位点),CO2分别在中碱位、强碱位
位点、氧化物载体位点),CO2分别在中碱位、强碱位 吸附发生反应。
吸附发生反应。
(4)请写出中碱位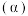 上发生反应的总化学方程式
上发生反应的总化学方程式___________ 。
Ⅳ.利用电化学可以将CO2有限转化为有机物。
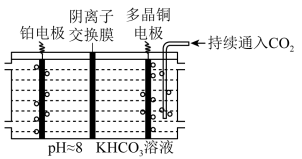
(5)多晶 是目前唯一被实验证实能高效催化CO2还原为烃类(如
是目前唯一被实验证实能高效催化CO2还原为烃类(如 )的金属。如图所示,电解装置中分别以多晶
)的金属。如图所示,电解装置中分别以多晶 和
和 为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后
为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后 浓度基本保持不变,温度控制在
浓度基本保持不变,温度控制在 左右。阴极生成
左右。阴极生成 的电极反应式为
的电极反应式为___________ 。
(6)装置工作时,阴极主要生成 ,还可能生成副产物降低电解效率。标准状况下,当阳极生成
,还可能生成副产物降低电解效率。标准状况下,当阳极生成 的体积为
的体积为 时,测得阴极区生成
时,测得阴极区生成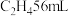 ,则电解效率
,则电解效率___________ 。(忽略电解前后溶液体积的变化)已知:电解效率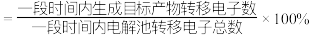 。
。
Ⅰ.常温下,以NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
(1)用1L Na2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,再过滤,所用的Na2CO3溶液的物质的量浓度至少为
 ;忽略溶液体积变化]
;忽略溶液体积变化] Ⅱ.CH4- CO2重整反应能够有效去除大气中CO2,是实现“碳中和”的重要途径之一,发生的反应如下:
重整反应
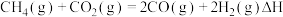
积炭反应Ⅰ:
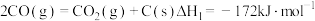
积炭反应Ⅱ:

在恒压、起始投料比
 条件下,体系中含碳组分、H2平衡时的物质的量随温度变化关系曲线如图所示。
条件下,体系中含碳组分、H2平衡时的物质的量随温度变化关系曲线如图所示。
(2)重整反应的反应热

(3)曲线C物质的量随温度的升高先升高后降低的原因是
Ⅲ.铜基催化剂
 (M为
(M为 等)是CO2加氢制甲醇常用的催化剂,部分合成路线如图所示。
等)是CO2加氢制甲醇常用的催化剂,部分合成路线如图所示。
其中催化剂上有两个活动点位(
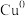 位点、氧化物载体位点),CO2分别在中碱位、强碱位
位点、氧化物载体位点),CO2分别在中碱位、强碱位 吸附发生反应。
吸附发生反应。(4)请写出中碱位
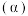 上发生反应的总化学方程式
上发生反应的总化学方程式Ⅳ.利用电化学可以将CO2有限转化为有机物。
(5)多晶
 是目前唯一被实验证实能高效催化CO2还原为烃类(如
是目前唯一被实验证实能高效催化CO2还原为烃类(如 )的金属。如图所示,电解装置中分别以多晶
)的金属。如图所示,电解装置中分别以多晶 和
和 为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后
为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后 浓度基本保持不变,温度控制在
浓度基本保持不变,温度控制在 左右。阴极生成
左右。阴极生成 的电极反应式为
的电极反应式为
(6)装置工作时,阴极主要生成
 ,还可能生成副产物降低电解效率。标准状况下,当阳极生成
,还可能生成副产物降低电解效率。标准状况下,当阳极生成 的体积为
的体积为 时,测得阴极区生成
时,测得阴极区生成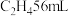 ,则电解效率
,则电解效率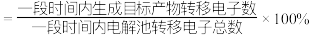 。
。
您最近半年使用:0次
2024-03-04更新
|
398次组卷
|
2卷引用:江苏省扬州中学2023-2024学年高三下学期阶段练习化学试题
名校
6 . 完成下列问题
(1)已知:①

②

则

___________ 。
(2)已知:①

②

则表示氨气燃烧热的热化学方程式为___________ ,该反应可设计为碱性条件下的燃料电池,负极电极反应式为___________ 。
(3)已知几种化学键的键能和热化学方程式如下:

 ,则a=
,则a=___________ 。
(4)4种不饱和烃分别与氢气发生加成反应生成1mol环己烷(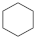 )的能量变化如图所示。根据图示判断4种有机反应物中最稳定的是
)的能量变化如图所示。根据图示判断4种有机反应物中最稳定的是___________ ;反应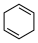 (l)=
(l)=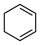 (l)的
(l)的
___________ 。

(1)已知:①


②


则


(2)已知:①


②


则表示氨气燃烧热的热化学方程式为
(3)已知几种化学键的键能和热化学方程式如下:
| 化学键 |  |  |  |  |  |
键能/( ) ) | 391 | 193 | 243 | a | 432 |

 ,则a=
,则a=(4)4种不饱和烃分别与氢气发生加成反应生成1mol环己烷(
 )的能量变化如图所示。根据图示判断4种有机反应物中最稳定的是
)的能量变化如图所示。根据图示判断4种有机反应物中最稳定的是 (l)=
(l)= (l)的
(l)的

您最近半年使用:0次
7 . 我国要在2030年前实现碳达峰、2060年前实现碳中和的目标,CO2的捕集与转化是研究的重要课题。
(1)CO2和CH4重整可制合成气CO和H2,其热化学反应方程式为CO2(g)+CH4(g)=2CO(g)+2H2(g) ΔH=+247 kJ·mol-1。
已知下列热化学反应方程式:
反应1:C(s)+2H2(g)=CH4(g) ΔH1
反应2:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-40.0 kJ·mol-1
反应3:C(s)+H2O(g)=CO(g)+H2(g) ΔH3=+132.0 kJ·mol-1
则ΔH1=___________ kJ·mol-1。
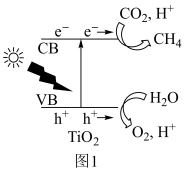
(2)光催化还原法实现CO2甲烷化可能的反应机理如图1所示。该过程可描述为:光照条件下,催化剂TiO2的价带(VB)中的电子激发至导带(CB)中,价带中形成电子空穴(h+),___________ 。
(3)一种电化学法将CO2转化为乙烯的原理如图2所示。
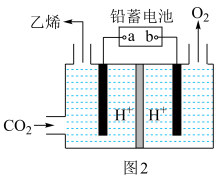
①阴极上的电极反应式为___________ 。
②以铅蓄电池为电源,每生成0.5 mol乙烯,理论上产生O2的物质的量为___________ 。
(1)CO2和CH4重整可制合成气CO和H2,其热化学反应方程式为CO2(g)+CH4(g)=2CO(g)+2H2(g) ΔH=+247 kJ·mol-1。
已知下列热化学反应方程式:
反应1:C(s)+2H2(g)=CH4(g) ΔH1
反应2:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-40.0 kJ·mol-1
反应3:C(s)+H2O(g)=CO(g)+H2(g) ΔH3=+132.0 kJ·mol-1
则ΔH1=
(2)光催化还原法实现CO2甲烷化可能的反应机理如图1所示。该过程可描述为:光照条件下,催化剂TiO2的价带(VB)中的电子激发至导带(CB)中,价带中形成电子空穴(h+),

(3)一种电化学法将CO2转化为乙烯的原理如图2所示。

①阴极上的电极反应式为
②以铅蓄电池为电源,每生成0.5 mol乙烯,理论上产生O2的物质的量为
您最近半年使用:0次
名校
8 . 化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_____ (填字母)。
A. 碳与水蒸气反应
B. 铝和氧化铁反应
C. CaCO3受热分解
D. 氢气还原三氧化钨制取钨
E. 锌与盐酸反应
(2)获取能量变化的途径
①已知:
则:SiCl4(g)+2H2(g)= Si(s)+4HCl(g)的反应热
_____ 
②已知在常温常压下:
i、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)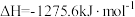
ii、H2O(l)=H2O(g)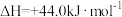
写出表示甲醇燃烧热的热化学方程式_____ 。
(3)用甲烷或其他有机物、氧气为原料可设计成原电池,以CnH2nOn、O2为原料,硫酸溶液为电解质设计成燃料电池,则负极的电极反应式为____________ 。
(4)最近科学家研制出超薄铁磁β-MnSe半导体,β-MnSe的晶胞结构如图所示。
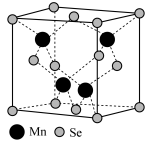
①β-MnSe中Mn的配位数为_______ 。
②Mn2+的价电子排布式为_______ 。
(1)下列反应中,属于放热反应的是
A. 碳与水蒸气反应
B. 铝和氧化铁反应
C. CaCO3受热分解
D. 氢气还原三氧化钨制取钨
E. 锌与盐酸反应
(2)获取能量变化的途径
①已知:
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能(kJ·mol-1) | 460 | 360 | 436 | 431 | 176 | 347 |


②已知在常温常压下:
i、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)
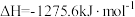
ii、H2O(l)=H2O(g)
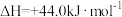
写出表示甲醇燃烧热的热化学方程式
(3)用甲烷或其他有机物、氧气为原料可设计成原电池,以CnH2nOn、O2为原料,硫酸溶液为电解质设计成燃料电池,则负极的电极反应式为
(4)最近科学家研制出超薄铁磁β-MnSe半导体,β-MnSe的晶胞结构如图所示。

①β-MnSe中Mn的配位数为
②Mn2+的价电子排布式为
您最近半年使用:0次
解题方法
9 . 回答下列问题
(1) 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下: ,则S(单斜,s)、S(斜方,s)相比,较稳定的是
,则S(单斜,s)、S(斜方,s)相比,较稳定的是___________ [填“S(单斜,s)”或“S(斜方、s)”]。
(2)下表中的数据表示破坏 化学键需消耗的能量(即键能,单位为
化学键需消耗的能量(即键能,单位为 )。
)。
热化学方程式: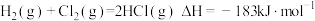 ,则
,则 键的键能为
键的键能为___________  。
。
(3)标准状况下,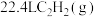 在
在 中完全燃烧生成
中完全燃烧生成 和
和 ,放出
,放出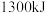 热量,请写出该反应的热化学方程式:
热量,请写出该反应的热化学方程式:___________ 。
(4)已知: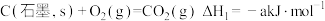
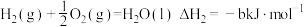
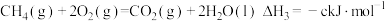
计算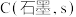 与
与 反应生成
反应生成 的
的 为
为___________ (用含a、b、c的式子表示) 。
。
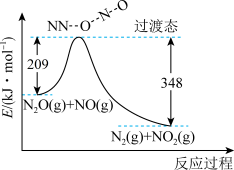
(5) 和
和 反应生成
反应生成 和
和 的能量变化如图所示。则反应过程中,每生成
的能量变化如图所示。则反应过程中,每生成 理论上放出的热量为
理论上放出的热量为___________
(1)
 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下: ,则S(单斜,s)、S(斜方,s)相比,较稳定的是
,则S(单斜,s)、S(斜方,s)相比,较稳定的是(2)下表中的数据表示破坏
 化学键需消耗的能量(即键能,单位为
化学键需消耗的能量(即键能,单位为 )。
)。| 化学键 |  |  |
| 键能 | 436 | 431 |
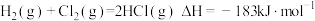 ,则
,则 键的键能为
键的键能为 。
。(3)标准状况下,
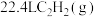 在
在 中完全燃烧生成
中完全燃烧生成 和
和 ,放出
,放出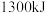 热量,请写出该反应的热化学方程式:
热量,请写出该反应的热化学方程式:(4)已知:
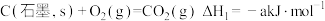
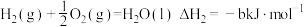
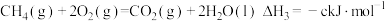
计算
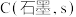 与
与 反应生成
反应生成 的
的 为
为 。
。(5)
 和
和 反应生成
反应生成 和
和 的能量变化如图所示。则反应过程中,每生成
的能量变化如图所示。则反应过程中,每生成 理论上放出的热量为
理论上放出的热量为
您最近半年使用:0次
名校
10 . N2O、NO和NO2等氮氧化物是空气污染物。含有氨氧化物的尾气需处理后才能排放。
(1)N2O的处理,N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化制作用下生成N2O的化学方程式为_____ 。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为NO+NO2+2OH-=2 +H2O、2NO2+2OH-=
+H2O、2NO2+2OH-= +
+ +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有_____ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是_____ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是_____ (填化学式)。
③用水吸收NOx的相关热化学方程式如下:
2NO2(g)+H2O(1)=HNO3(aq)+HNO2(aq) △H=-116.1kJ/mol;
3HNO2(aq)=HNO3(aq)+2NO(g)H2O(1) △H=+75.9kJ/mol
反应3NO2(g)+H2O(1)=2HNO3(aq)+NO(g)的△H=_____ kJ/mol。
④用稀硝酸吸收NO得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应_____ 。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO液中,HClO氧化NO生成Cl-和 ,其离子方程式为
,其离子方程式为_____ 。
(1)N2O的处理,N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化制作用下生成N2O的化学方程式为
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为NO+NO2+2OH-=2
 +H2O、2NO2+2OH-=
+H2O、2NO2+2OH-= +
+ +H2O
+H2O①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
③用水吸收NOx的相关热化学方程式如下:
2NO2(g)+H2O(1)=HNO3(aq)+HNO2(aq) △H=-116.1kJ/mol;
3HNO2(aq)=HNO3(aq)+2NO(g)H2O(1) △H=+75.9kJ/mol
反应3NO2(g)+H2O(1)=2HNO3(aq)+NO(g)的△H=
④用稀硝酸吸收NO得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO液中,HClO氧化NO生成Cl-和
 ,其离子方程式为
,其离子方程式为
您最近半年使用:0次



