解题方法
1 . 回答下列问题
(1)用做消化系统X射线检查的内服药剂“钡餐”的化学式为___________ 。
(2)酸雨的
___________ 5.6(填“>”、“<”、“=”)。
(3) 的电子式
的电子式___________ 。
(4)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅,化学方程式为___________ 。
(5)己知:①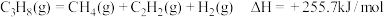
②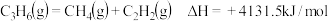
则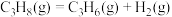 的
的
___________ 。
(1)用做消化系统X射线检查的内服药剂“钡餐”的化学式为
(2)酸雨的

(3)
 的电子式
的电子式(4)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅,化学方程式为
(5)己知:①
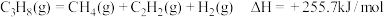
②
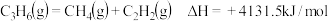
则
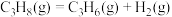 的
的
您最近一年使用:0次
名校
2 . 回答下列问题:
(1)肼( )常用于火箭或原电池的燃料。已知:
)常用于火箭或原电池的燃料。已知:
①

②
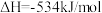
③
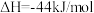
则反应

_______ kJ/mol,若将该反应设计成原电池,电解质溶液为稀硫酸,则正极的电极反应为_______ 。
(2)氢气的热值极高,是一种极为优越的能源。标准状况下, 完全燃烧可放出
完全燃烧可放出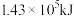 的热量,则表示
的热量,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_______ 。氢气直接燃烧的能量转换率远低于燃料电池,则碱性氢氧燃料电池的负极反应式为_______ 。
(3)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
反应Ⅲ:S(s)+O2(g)=SO2(g) ∆H3=-297kJ/mol
反应Ⅱ的热化学方程式:_______ 。
(4)火箭和导弹表面的薄层是耐高温物质。制得该物质的热化学方程式为: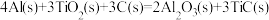
 。该反应中每转移1 mol电子放出的热量为
。该反应中每转移1 mol电子放出的热量为_______  。
。
(1)肼(
 )常用于火箭或原电池的燃料。已知:
)常用于火箭或原电池的燃料。已知:①


②

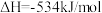
③

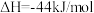
则反应


(2)氢气的热值极高,是一种极为优越的能源。标准状况下,
 完全燃烧可放出
完全燃烧可放出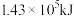 的热量,则表示
的热量,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(3)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

反应Ⅲ:S(s)+O2(g)=SO2(g) ∆H3=-297kJ/mol
反应Ⅱ的热化学方程式:
(4)火箭和导弹表面的薄层是耐高温物质。制得该物质的热化学方程式为:
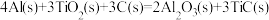
 。该反应中每转移1 mol电子放出的热量为
。该反应中每转移1 mol电子放出的热量为 。
。
您最近一年使用:0次
3 . 中国首次实现了利用二氧化碳人工合成淀粉,为全球的“碳达峰”、“碳中和”起到重大的支撑作用。其中最关键的一步是以 为原料制
为原料制 。在某
。在某 催化加氢制
催化加氢制 的反应体系中,发生的主要反应有:
的反应体系中,发生的主要反应有:
Ⅰ.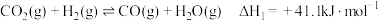
Ⅱ.

Ⅲ.
(1)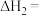
___________  。
。
(2) 时,往某密闭容器中按投料比
时,往某密闭容器中按投料比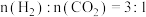 充入
充入 和
和 。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
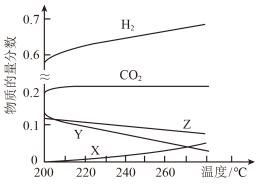
图中Y代表___________ (填化学式)。
(3)我国科研人员研究出在 催化剂上
催化剂上 氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为
氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为___________ 。分析在反应气中加入少量的水能够提升甲醇产率的可能原因是___________ 。

(4)恒压下, 和
和 以物质的量之比
以物质的量之比 投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。
。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。___________

 为原料制
为原料制 。在某
。在某 催化加氢制
催化加氢制 的反应体系中,发生的主要反应有:
的反应体系中,发生的主要反应有:Ⅰ.
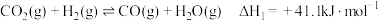
Ⅱ.


Ⅲ.

(1)
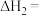
 。
。(2)
 时,往某密闭容器中按投料比
时,往某密闭容器中按投料比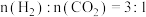 充入
充入 和
和 。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
图中Y代表
(3)我国科研人员研究出在
 催化剂上
催化剂上 氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为
氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为
(4)恒压下,
 和
和 以物质的量之比
以物质的量之比 投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。
。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。
您最近一年使用:0次
4 . 回答下列问题
(1)①写出小苏打的化学式___________ ;
②写出Fe2+的价电子排布式___________ 。
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式___________ 。
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=___________
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式___________
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
关于元素R的下列推断中,正确的是___________ (用相应的编号填写)
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
(1)①写出小苏打的化学式
②写出Fe2+的价电子排布式
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
| 元素 | 电离能/(kJ·mol-1) | |||||
| I1 | I2 | I3 | I4 | I5 | …… | |
| R | 740 | 1500 | 7700 | 10500 | 13630 | …… |
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
您最近一年使用:0次
解题方法
5 . 途径I: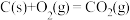
 。
。
途径Ⅱ:先制水煤气
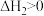 ,
,
再燃烧水煤气: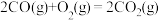
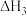 ,
,
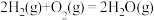
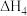 。
。
请回答下列问题:
(1)判断:途径I放出的热量______ (填“>”、“=”或“<”)途径Ⅱ放出的热量。
(2)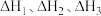 和
和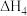 的数学关系式是
的数学关系式是______ 。
(3)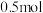 气态高能燃料乙硼烷(
气态高能燃料乙硼烷( )在氧气中燃烧生成固态三氧化二硼(
)在氧气中燃烧生成固态三氧化二硼( )和液态水,放出
)和液态水,放出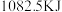 热量,其热化学方程式
热量,其热化学方程式______ 。
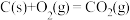
 。
。途径Ⅱ:先制水煤气

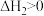 ,
,再燃烧水煤气:
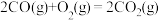
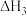 ,
,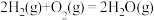
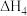 。
。请回答下列问题:
(1)判断:途径I放出的热量
(2)
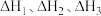 和
和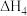 的数学关系式是
的数学关系式是(3)
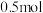 气态高能燃料乙硼烷(
气态高能燃料乙硼烷( )在氧气中燃烧生成固态三氧化二硼(
)在氧气中燃烧生成固态三氧化二硼( )和液态水,放出
)和液态水,放出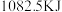 热量,其热化学方程式
热量,其热化学方程式
您最近一年使用:0次
6 . 请回答以下问题:
(1)在载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.

Ⅱ.
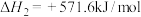
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式__________ 。
(2)在 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(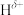 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(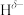 ),这三种元素电负性从大到小的顺序是
),这三种元素电负性从大到小的顺序是__________ 。
(3)100mLpH=10.00的 溶液中水电离出
溶液中水电离出 的物质的量为
的物质的量为__________ mol。
(4)已知:25℃时碳酸的 、
、 ,次氯酸的
,次氯酸的 。写出在NaClO溶液中通入
。写出在NaClO溶液中通入 气体的离子方程式
气体的离子方程式__________ 。
(5)据文献报道, 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是__________ 。
(6)锗(Ge)与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是__________ 。
(7)乙醇的挥发性比水的强,原因是__________ 。
(1)在载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.


Ⅱ.

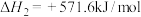
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式
(2)在
 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(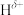 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(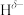 ),这三种元素电负性从大到小的顺序是
),这三种元素电负性从大到小的顺序是(3)100mLpH=10.00的
 溶液中水电离出
溶液中水电离出 的物质的量为
的物质的量为(4)已知:25℃时碳酸的
 、
、 ,次氯酸的
,次氯酸的 。写出在NaClO溶液中通入
。写出在NaClO溶液中通入 气体的离子方程式
气体的离子方程式(5)据文献报道,
 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是(6)锗(Ge)与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是
(7)乙醇的挥发性比水的强,原因是
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题
(1)家用液化气中主要成分之一是丁烷( )。常温常压时,当1g丁烷完全燃烧并生成
)。常温常压时,当1g丁烷完全燃烧并生成 和液态水时,放出热量50kJ。试写出该状态下表示丁烷燃烧热的热化学方程式:
和液态水时,放出热量50kJ。试写出该状态下表示丁烷燃烧热的热化学方程式:________ 。
(2)高炉炼铁基本反应: ,其平衡常数表达式为:
,其平衡常数表达式为:___________ 。
(3)处理含CO、 烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
①
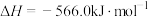
②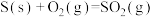

此反应的热化学方程式是___________ 。
(4)CO用于处理大气污染物 的原理为
的原理为
 ,有人提出上述反应可以用“
,有人提出上述反应可以用“ ”作催化剂,其总反应分两步进行:第一步:
”作催化剂,其总反应分两步进行:第一步: ;第二步:
;第二步:___________ (写离子反应方程式)。
(1)家用液化气中主要成分之一是丁烷(
 )。常温常压时,当1g丁烷完全燃烧并生成
)。常温常压时,当1g丁烷完全燃烧并生成 和液态水时,放出热量50kJ。试写出该状态下表示丁烷燃烧热的热化学方程式:
和液态水时,放出热量50kJ。试写出该状态下表示丁烷燃烧热的热化学方程式:(2)高炉炼铁基本反应:
 ,其平衡常数表达式为:
,其平衡常数表达式为:(3)处理含CO、
 烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:①

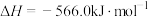
②
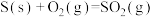

此反应的热化学方程式是
(4)CO用于处理大气污染物
 的原理为
的原理为
 ,有人提出上述反应可以用“
,有人提出上述反应可以用“ ”作催化剂,其总反应分两步进行:第一步:
”作催化剂,其总反应分两步进行:第一步: ;第二步:
;第二步:
您最近一年使用:0次
8 . 按要求填空:
(1)在25℃和101kPa下,16gCH3OH(l)在O2中完全燃烧,放出363.3kJ的热量,请写出表示该反应的热化学方程式:_____ 。
(2)研究表明,二氧化碳与氢气反应可以合成甲醇,反应如下:

①反应的平衡常数表达式为:_____ 。
②有利于提高平衡时甲醇产率的措施有_____ (填字母)
a.使用催化剂 b.缩小反应容器的容积 c.适当降低反应温度
(3)已知共价键的键能与热化学方程式信息如下表:
则 的
的
_____ (用含、a、b、c的式子表示)
(1)在25℃和101kPa下,16gCH3OH(l)在O2中完全燃烧,放出363.3kJ的热量,请写出表示该反应的热化学方程式:
(2)研究表明,二氧化碳与氢气反应可以合成甲醇,反应如下:


①反应的平衡常数表达式为:
②有利于提高平衡时甲醇产率的措施有
a.使用催化剂 b.缩小反应容器的容积 c.适当降低反应温度
(3)已知共价键的键能与热化学方程式信息如下表:
| 共价键 | H—H | H—O |
键能/( ) ) | a | b |
| 热化学方程式 |  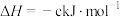 | |
 的
的
您最近一年使用:0次
9 . 碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。已知:
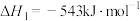 。
。
(1)该反应的熵变
___________ 0(填“>”“<”“=”),该反应自发进行的条件是___________ (填“低温”“高温”或“任意温度”)。
(2)反应
 ,则
,则
___________  (填“>”“<”“=”)。
(填“>”“<”“=”)。
(3)已知:①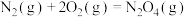
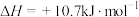
②
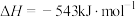
写出气态肼和 反应的热化学方程式:
反应的热化学方程式:___________ 。

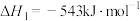 。
。(1)该反应的熵变

(2)反应

 ,则
,则
 (填“>”“<”“=”)。
(填“>”“<”“=”)。(3)已知:①
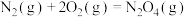
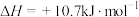
②

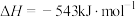
写出气态肼和
 反应的热化学方程式:
反应的热化学方程式:
您最近一年使用:0次
10 . 实现碳中和已经成为全球的广泛共识,化学科学在此过程中发挥着至关重要的作用。
(1) 加氢可制备甲酸(
加氢可制备甲酸( )。
)。
①工业上利用甲酸的能量关系转换图如图所示:
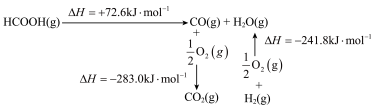
反应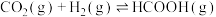 的焓变
的焓变
___________  。
。
②温度为 ℃时,将等物质的量的
℃时,将等物质的量的 和
和 充入体积为
充入体积为 的恒容密闭容器中发生反应:
的恒容密闭容器中发生反应: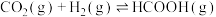
 。
。
实验测得;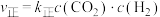 ,
, ,
, 、
、 为速率常数。保持其他条件不变,温度为
为速率常数。保持其他条件不变,温度为 ℃时,
℃时,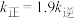 ,则
,则 ℃时平衡压强
℃时平衡压强_______ (填“>”、“<”或“=”) ℃时平衡压强,理由是
℃时平衡压强,理由是___________ 。
(2) 加氢还可制备甲醇
加氢还可制备甲醇 ,涉及的反应如下:
,涉及的反应如下:
ⅰ.
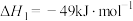
ⅱ.

在一定压强下,按照 投料,平衡时,CO和
投料,平衡时,CO和 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 的转化率随温度的变化如图:
的转化率随温度的变化如图:
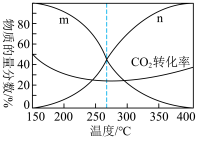
请回答:
①下列说法正确的是_______ (填字母)。
A.图中代表CO的曲线为n
B. 的平衡转化率可能大于
的平衡转化率可能大于 的平衡转化率
的平衡转化率
C.温度越低,越有利于工业生产
D.150~400℃范围内,温度升高, 的平衡产量先减小后增大
的平衡产量先减小后增大
②解释300~400℃范围内 转化率随温度升高而增大的原因:
转化率随温度升高而增大的原因:_______ 。
③在容积可变的密闭容器中充入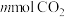 和
和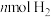 (
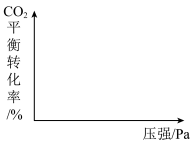
( ),在恒温恒压条件下只发生反应ⅰ,在图中画出
),在恒温恒压条件下只发生反应ⅰ,在图中画出 的平衡转化率随温度(
的平衡转化率随温度(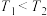 )、压强的变化图
)、压强的变化图_______ 。
(1)
 加氢可制备甲酸(
加氢可制备甲酸( )。
)。①工业上利用甲酸的能量关系转换图如图所示:

反应
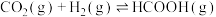 的焓变
的焓变
 。
。②温度为
 ℃时,将等物质的量的
℃时,将等物质的量的 和
和 充入体积为
充入体积为 的恒容密闭容器中发生反应:
的恒容密闭容器中发生反应: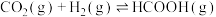
 。
。实验测得;
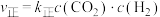 ,
, ,
, 、
、 为速率常数。保持其他条件不变,温度为
为速率常数。保持其他条件不变,温度为 ℃时,
℃时,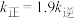 ,则
,则 ℃时平衡压强
℃时平衡压强 ℃时平衡压强,理由是
℃时平衡压强,理由是(2)
 加氢还可制备甲醇
加氢还可制备甲醇 ,涉及的反应如下:
,涉及的反应如下:ⅰ.

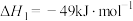
ⅱ.


在一定压强下,按照
 投料,平衡时,CO和
投料,平衡时,CO和 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 的转化率随温度的变化如图:
的转化率随温度的变化如图:
请回答:
①下列说法正确的是
A.图中代表CO的曲线为n
B.
 的平衡转化率可能大于
的平衡转化率可能大于 的平衡转化率
的平衡转化率C.温度越低,越有利于工业生产

D.150~400℃范围内,温度升高,
 的平衡产量先减小后增大
的平衡产量先减小后增大②解释300~400℃范围内
 转化率随温度升高而增大的原因:
转化率随温度升高而增大的原因:③在容积可变的密闭容器中充入
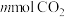 和
和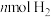 (
( ),在恒温恒压条件下只发生反应ⅰ,在图中画出
),在恒温恒压条件下只发生反应ⅰ,在图中画出 的平衡转化率随温度(
的平衡转化率随温度(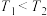 )、压强的变化图
)、压强的变化图
您最近一年使用:0次



