解题方法
1 . 研究化学反应中的能量变化具有重要的意义。回答下列问题:
(1)甲醇是人们开发和利用的一种新能源。已知:
2H2(g)+O2(g)=2H2O(1) △H1=-571.8kJ/mol
CH3OH(l)+ O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
①由上述热化学方程式可知甲醇的燃烧热△H=____________ 。
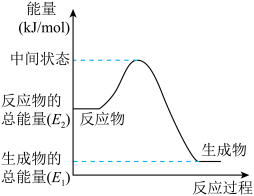
②上述第二个反应的能量变化如图所示,则△H2=___________ k/mol。(用E1、E2的相关式子表示)。.
(2)已知反应N2(g)+3H2(g) 2NH3(g),试根据表中所列键能数据估算该反应的△H=
2NH3(g),试根据表中所列键能数据估算该反应的△H=________ 。
(3)1molH2和1molCH4完全燃烧放出的热量分别为286kJ、890kJ,等质量的H2和CH4完全燃烧,放出热量较多的是__________ (填化学式)。
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态过氧化氢反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:_____________ 。
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是___________ 。
(1)甲醇是人们开发和利用的一种新能源。已知:
2H2(g)+O2(g)=2H2O(1) △H1=-571.8kJ/mol
CH3OH(l)+
 O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol①由上述热化学方程式可知甲醇的燃烧热△H=
②上述第二个反应的能量变化如图所示,则△H2=

(2)已知反应N2(g)+3H2(g)
 2NH3(g),试根据表中所列键能数据估算该反应的△H=
2NH3(g),试根据表中所列键能数据估算该反应的△H=| 化学键 | H-H | N-H | N≡N |
| 键能(kJ/mol) | 436 | 391 | 945 |
(3)1molH2和1molCH4完全燃烧放出的热量分别为286kJ、890kJ,等质量的H2和CH4完全燃烧,放出热量较多的是
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态过氧化氢反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
2 . 对于基元反应,如aA+bB cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
反应Ⅰ:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
反应Ⅱ:8NH3(g)+6NO2(g) 7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
反应Ⅲ:N2(g)+O2(g)=2NO(g)ΔH3=+182.6kJ·mol-1
对于基元反应Ⅳ:2NO(g)+O2(g) 2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
(1)ΔH4=______ kJ·mol-1
(2)计算653K时的平衡常数K=______ 。
(3)653K时,若NO的浓度为0.006mol·L-1,O2的浓度为0.290mol·L-1,则正反应速率为______ mol·L-1·s-1
 cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:反应Ⅰ:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1反应Ⅱ:8NH3(g)+6NO2(g)
 7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1反应Ⅲ:N2(g)+O2(g)=2NO(g)ΔH3=+182.6kJ·mol-1
对于基元反应Ⅳ:2NO(g)+O2(g)
 2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1(1)ΔH4=
(2)计算653K时的平衡常数K=
(3)653K时,若NO的浓度为0.006mol·L-1,O2的浓度为0.290mol·L-1,则正反应速率为
您最近半年使用:0次
3 . 已知下列反应的热化学方程式:
①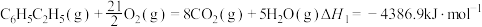
②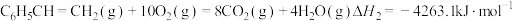
③
计算反应④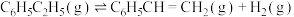 的
的
_____  ;
;
①
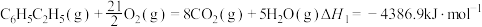
②
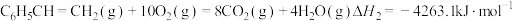
③

计算反应④
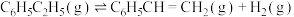 的
的
 ;
;
您最近半年使用:0次
4 . 利用化学反应为人类提供能量,研究反应中的能量变化意义重大。
(1) 和
和 可发生反应
可发生反应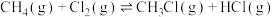 ,部分反应进程如图所示。
,部分反应进程如图所示。
___________  。
。
②图中第1步基元反应为___________ ;第2步反应的活化能为___________  。
。
(2)某实验小组用50mL配制好的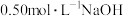 溶液和
溶液和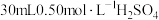 溶液进行中和反应热的测定。
溶液进行中和反应热的测定。___________ (填仪器名称)。
②实验中硫酸溶液相对NaOH溶液是过量的,目的是___________ 。
③实验数据如表所示:
近似认为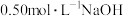 溶液和
溶液和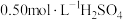 溶液的密度都是
溶液的密度都是 ,中和后混合溶液的比热容
,中和后混合溶液的比热容 ,则
,则
___________  (结果精确至0.1)。
(结果精确至0.1)。
(3)联氨(又称肼, ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
①已知12.8g的液态联氨在氧气中燃烧,生成气态 和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式
和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式___________ 。
②已知:a.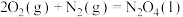

b.

c.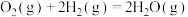

d.

上述反应热效应之间的关系式为
___________ 。
(1)
 和
和 可发生反应
可发生反应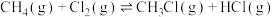 ,部分反应进程如图所示。
,部分反应进程如图所示。

 。
。②图中第1步基元反应为
 。
。(2)某实验小组用50mL配制好的
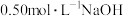 溶液和
溶液和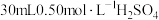 溶液进行中和反应热的测定。
溶液进行中和反应热的测定。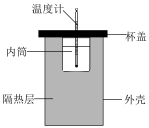
②实验中硫酸溶液相对NaOH溶液是过量的,目的是
③实验数据如表所示:
| 温度 实验次数 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | ||
 溶液 溶液 | NaOH溶液 | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 |
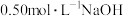 溶液和
溶液和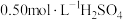 溶液的密度都是
溶液的密度都是 ,中和后混合溶液的比热容
,中和后混合溶液的比热容 ,则
,则
 (结果精确至0.1)。
(结果精确至0.1)。(3)联氨(又称肼,
 ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。①已知12.8g的液态联氨在氧气中燃烧,生成气态
 和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式
和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式②已知:a.
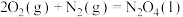

b.


c.
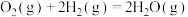

d.


上述反应热效应之间的关系式为

您最近半年使用:0次
名校
解题方法
5 . 由化学能产生热能是目前人类使用能源的主要途径。回答下列问题:
(1)如图表示反应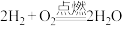 的能量变化。
的能量变化。

已知断开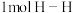 键、
键、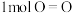 键和
键和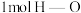 键分别需要消耗
键分别需要消耗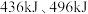 和
和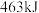 的能量。则反应过程(Ⅱ)中生成
的能量。则反应过程(Ⅱ)中生成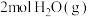 时放出能量
时放出能量______ kJ能量。
(2)已知某温度下 的溶解热为
的溶解热为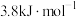 (吸热)
(吸热)

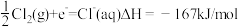
写出该温度下钠在氯气中燃烧的热化学方程式___________ 。
(3) 溶液与
溶液与 锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。(已知:反应前后,溶液的比热容均近似为
锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。(已知:反应前后,溶液的比热容均近似为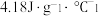 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。)请计算:
,忽略溶液体积、质量变化和金属吸收的热量。)请计算:
①该反应放出的热量
____ J。
②反应 的
的
_____  。
。
(1)如图表示反应
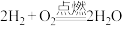 的能量变化。
的能量变化。
已知断开
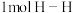 键、
键、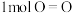 键和
键和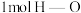 键分别需要消耗
键分别需要消耗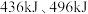 和
和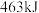 的能量。则反应过程(Ⅱ)中生成
的能量。则反应过程(Ⅱ)中生成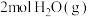 时放出能量
时放出能量(2)已知某温度下
 的溶解热为
的溶解热为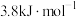 (吸热)
(吸热)
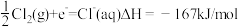
写出该温度下钠在氯气中燃烧的热化学方程式
(3)
 溶液与
溶液与 锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。(已知:反应前后,溶液的比热容均近似为
锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。(已知:反应前后,溶液的比热容均近似为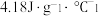 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。)请计算:
,忽略溶液体积、质量变化和金属吸收的热量。)请计算:①该反应放出的热量

②反应
 的
的
 。
。
您最近半年使用:0次
2023高三·全国·专题练习
6 . 磷与氯气反应时各状态间的能量变化如图所示。已知: 。
。

回答下列问题:
(1)依据图示写出各反应的焓变:
 ΔH1=
ΔH1=_______ ;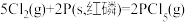 ΔH2=
ΔH2=________ ;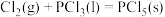 ΔH3=
ΔH3=___________ 。
(2)已知常温常压下:①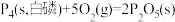
 ;②
;②
 ;则
;则
_____ (填“>”、“=”或“<”,下同) ;
;
(3)将1.86g红磷在2.24L(已换算成标准状况) 中引燃,生成了大量的白色烟雾,完全反应后,若红磷和
中引燃,生成了大量的白色烟雾,完全反应后,若红磷和 均无剩余且生成的每种产物均只有一种状态,此时放出的热量为
均无剩余且生成的每种产物均只有一种状态,此时放出的热量为_________ kJ。
 。
。
回答下列问题:
(1)依据图示写出各反应的焓变:
 ΔH1=
ΔH1=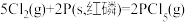 ΔH2=
ΔH2=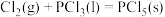 ΔH3=
ΔH3=(2)已知常温常压下:①
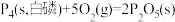
 ;②
;②
 ;则
;则
 ;
;(3)将1.86g红磷在2.24L(已换算成标准状况)
 中引燃,生成了大量的白色烟雾,完全反应后,若红磷和
中引燃,生成了大量的白色烟雾,完全反应后,若红磷和 均无剩余且生成的每种产物均只有一种状态,此时放出的热量为
均无剩余且生成的每种产物均只有一种状态,此时放出的热量为
您最近半年使用:0次
名校
解题方法
7 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。二氧化碳加氢制甲醇的总反应可表示为:


该反应一般认为通过如下步骤来实现:
反应①

反应②

回答下列问题:
(1)
___________ 
(2)有利于提高 转化为
转化为 平衡转化率的措施有
平衡转化率的措施有___________ (填编号)。
A.升高温度 B.降低温度 C.增大压强
D.降低压强 E.使用催化剂 F.增大 和
和 的初始投料比
的初始投料比
(3)二氧化碳加氢制甲醇的总反应按 投料,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
投料,在不同条件下达到平衡,设体系中甲醇的物质的量分数为 ,在
,在 下的
下的 随温度
随温度 变化,在
变化,在 下的
下的 随压强
随压强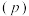 变化如图所示。
变化如图所示。
①图中对应在 下的
下的 随温度
随温度 变化的等压过程的曲线是
变化的等压过程的曲线是___________ (填“ ”或“
”或“ ”)。判断理由是
”)。判断理由是___________ 。
② 时,反应条件可能为
时,反应条件可能为___________ 或___________ 。
③ 时,计算
时,计算 的平衡转化率,写出计算过程
的平衡转化率,写出计算过程___________ 。


该反应一般认为通过如下步骤来实现:
反应①


反应②


回答下列问题:
(1)


(2)有利于提高
 转化为
转化为 平衡转化率的措施有
平衡转化率的措施有A.升高温度 B.降低温度 C.增大压强
D.降低压强 E.使用催化剂 F.增大
 和
和 的初始投料比
的初始投料比(3)二氧化碳加氢制甲醇的总反应按
 投料,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
投料,在不同条件下达到平衡,设体系中甲醇的物质的量分数为 ,在
,在 下的
下的 随温度
随温度 变化,在
变化,在 下的
下的 随压强
随压强 变化如图所示。
变化如图所示。
①图中对应在
 下的
下的 随温度
随温度 变化的等压过程的曲线是
变化的等压过程的曲线是 ”或“
”或“ ”)。判断理由是
”)。判断理由是②
 时,反应条件可能为
时,反应条件可能为③
 时,计算
时,计算 的平衡转化率,写出计算过程
的平衡转化率,写出计算过程
您最近半年使用:0次
8 . 根据已知,回答下列问题。
(1)在 、
、 下,
下, 甲烷燃烧生成
甲烷燃烧生成 和液态水时放热
和液态水时放热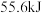 。则表示甲烷燃烧热的热化学方程式为
。则表示甲烷燃烧热的热化学方程式为______ 。
(2)常温常压下,断裂 (理想)气体分子化学键所吸收的能量或形成
(理想)气体分子化学键所吸收的能量或形成 (理想)气体分子化学键所放出的能量称为键能,下表是一些键能数
(理想)气体分子化学键所放出的能量称为键能,下表是一些键能数
根据键能数据计算以下反应的反应热: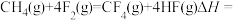
______ 。
(3)随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A.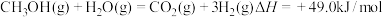
B.
由上述方程式可知, 的燃烧热
的燃烧热______ (填“大于”、“等于”或“小于”)
(4)火箭的常规燃料是液态四氧化二氮和液态肼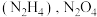 作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:


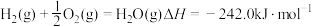
请写出肼和氟气反应的热化学方程式:______ 。
(1)在
 、
、 下,
下, 甲烷燃烧生成
甲烷燃烧生成 和液态水时放热
和液态水时放热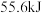 。则表示甲烷燃烧热的热化学方程式为
。则表示甲烷燃烧热的热化学方程式为(2)常温常压下,断裂
 (理想)气体分子化学键所吸收的能量或形成
(理想)气体分子化学键所吸收的能量或形成 (理想)气体分子化学键所放出的能量称为键能,下表是一些键能数
(理想)气体分子化学键所放出的能量称为键能,下表是一些键能数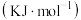
化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
C-H | 414 | C-F | 489 | H-F | 565 |
| 436 |
| 391 |
| 158 |
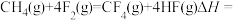
(3)随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A.
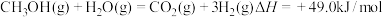
B.

由上述方程式可知,
 的燃烧热
的燃烧热
(4)火箭的常规燃料是液态四氧化二氮和液态肼
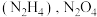 作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。已知:


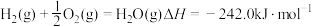
请写出肼和氟气反应的热化学方程式:
您最近半年使用:0次
名校
9 . 对碳及其氧化物的化学研究有助于人类充分利用化石燃料,消除碳氧化物对环境的负面影响。用 代替
代替 与燃料
与燃料 反应,既可以提高燃烧效率,又能得到高纯
反应,既可以提高燃烧效率,又能得到高纯 ,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①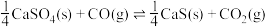
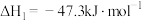
②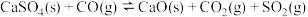
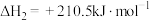
③
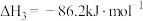
(1)反应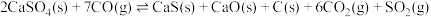 的
的
___________ (用 表示)。
表示)。
(2)向盛有 的真空恒容容器中充入
的真空恒容容器中充入 ,反应①于
,反应①于 达到平衡(
达到平衡( ),平衡时
),平衡时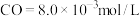 ,
, 的平衡转化率为
的平衡转化率为___________ 。(忽略副反应,结果保留2位有效数字)。
(3)其它条件不变时,升高温度戒缩小容器的体积,均能使反应②的平衡发生移动,请在下列坐标中作出该反应的平衡常数K随温度(T)、压强(P,缩小容器体积)变化而变化的示意图_______ :
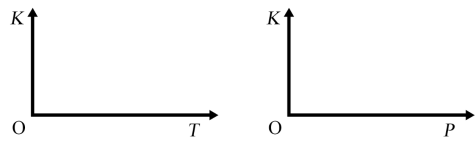
(4)某温度下,测得 的
的 溶液的
溶液的 为11,将该温度下
为11,将该温度下 的
的 溶液
溶液 与
与 的
的 溶液,
溶液, 混合,通过计算填写以下不同情况时两溶液的体积比:
混合,通过计算填写以下不同情况时两溶液的体积比:
①若所得混合溶液为中性,且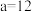 ,
,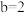 ,则
,则
___________ 。
②若所得混合溶液为中性,且 ,则
,则
___________ 。
③若所得混合溶液的 ,且
,且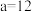 ,
,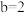 ,则
,则
___________ 。
 代替
代替 与燃料
与燃料 反应,既可以提高燃烧效率,又能得到高纯
反应,既可以提高燃烧效率,又能得到高纯 ,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。①
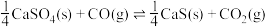
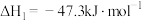
②
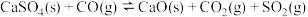
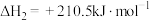
③

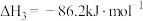
(1)反应
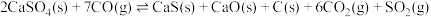 的
的
 表示)。
表示)。(2)向盛有
 的真空恒容容器中充入
的真空恒容容器中充入 ,反应①于
,反应①于 达到平衡(
达到平衡( ),平衡时
),平衡时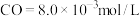 ,
, 的平衡转化率为
的平衡转化率为(3)其它条件不变时,升高温度戒缩小容器的体积,均能使反应②的平衡发生移动,请在下列坐标中作出该反应的平衡常数K随温度(T)、压强(P,缩小容器体积)变化而变化的示意图

(4)某温度下,测得
 的
的 溶液的
溶液的 为11,将该温度下
为11,将该温度下 的
的 溶液
溶液 与
与 的
的 溶液,
溶液, 混合,通过计算填写以下不同情况时两溶液的体积比:
混合,通过计算填写以下不同情况时两溶液的体积比:①若所得混合溶液为中性,且
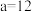 ,
,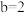 ,则
,则
②若所得混合溶液为中性,且
 ,则
,则
③若所得混合溶液的
 ,且
,且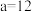 ,
,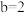 ,则
,则
您最近半年使用:0次
名校
10 . 已知几种含碳物质间的转化及能量变化关系如图所示。
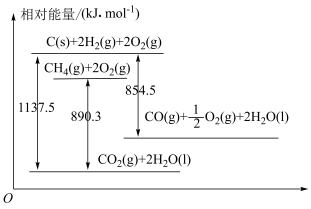
(1)写出表示CO燃烧热的热化学方程式:___________ 。
(2)反应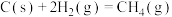

___________  ,该反应中反应物的总键能
,该反应中反应物的总键能___________ (填“大于”、“小于”或“等于”)生成物的总键能。若18gC(s)与 反应,完全转化成
反应,完全转化成 ,需要
,需要___________ (填“吸收”或“放出”)___________ kJ能量。
(3)在25℃、101kPa下,30g由 和CO组成的混合气体完全燃烧生成
和CO组成的混合气体完全燃烧生成 和液态水,放出热量1031.8kJ。则混合气体中
和液态水,放出热量1031.8kJ。则混合气体中 和CO的物质的量分别为
和CO的物质的量分别为___________ mol、___________ mol。

(1)写出表示CO燃烧热的热化学方程式:
(2)反应
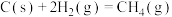

 ,该反应中反应物的总键能
,该反应中反应物的总键能 反应,完全转化成
反应,完全转化成 ,需要
,需要(3)在25℃、101kPa下,30g由
 和CO组成的混合气体完全燃烧生成
和CO组成的混合气体完全燃烧生成 和液态水,放出热量1031.8kJ。则混合气体中
和液态水,放出热量1031.8kJ。则混合气体中 和CO的物质的量分别为
和CO的物质的量分别为
您最近半年使用:0次
2023-11-21更新
|
135次组卷
|
2卷引用:河南省新乡市2023-2024学年高二上学期期中考试化学试题






