1 . 依据下列含硫物质转化的热化学方程式,得出的相关结论正确的是
①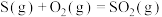

②

③

④

⑤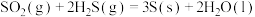

①
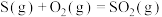

②


③


④


⑤
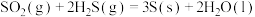

A.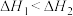 | B.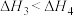 |
C.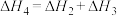 | D.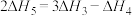 |
您最近一年使用:0次
2022-11-25更新
|
146次组卷
|
3卷引用:河北省邯郸市部分学校2022-2023学年高三上学期11月月考化学试题
名校
2 . 如图是金属镁和卤素单质( )反应的能量变化示意图。下列说法错误的是
)反应的能量变化示意图。下列说法错误的是
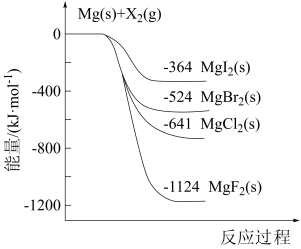
 )反应的能量变化示意图。下列说法错误的是
)反应的能量变化示意图。下列说法错误的是
A.工业上可通过电解熔融状态下的 制取金属Mg,Mg是阴极产物 制取金属Mg,Mg是阴极产物 |
B.标准状况条件下,11.2L (g)与足量的Mg充分反应,吸热562kJ (g)与足量的Mg充分反应,吸热562kJ |
C.热稳定性: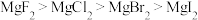 |
D.由图可知: 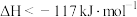 |
您最近一年使用:0次
名校
解题方法
3 . 丙烯是一种重要的有机化工原料,工业上以丁烯、乙烯为原料制取丙烯的反应如下: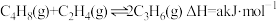 ,一定温度下,向体积为
,一定温度下,向体积为 密闭容器中充入
密闭容器中充入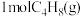 和
和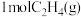 ,测得
,测得 的体积分数随时间的变化如图中线Ⅰ所示。
的体积分数随时间的变化如图中线Ⅰ所示。
已知几种气体的燃烧热如下表所示
下列说法正确的是
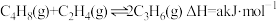 ,一定温度下,向体积为
,一定温度下,向体积为 密闭容器中充入
密闭容器中充入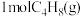 和
和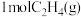 ,测得
,测得 的体积分数随时间的变化如图中线Ⅰ所示。
的体积分数随时间的变化如图中线Ⅰ所示。
已知几种气体的燃烧热如下表所示
| 气体 |  | 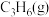 |  |
燃烧热/ / / | 1411 | 2049 | 2539 |
A. 燃烧的热化学方程式可表示为 燃烧的热化学方程式可表示为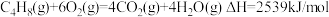 |
B.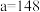 |
| C.该温度下反应的平衡常数为64 |
| D.图中线II可能是其他条件一定,反应在更高温度时进行 |
您最近一年使用:0次
22-23高三上·江苏南通·开学考试
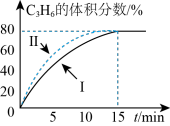
4 . 丙烯是一种重要的有机化工原料,工业上以丁烯、乙烯为原料制取丙烯的反应如下: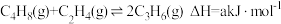 ,一定温度下,向体积为V L密闭容器中充入1 mol C4H8(g)和1 mol C2H4(g),测得C3H6的体积分数随时间的变化如图中线I所示。
,一定温度下,向体积为V L密闭容器中充入1 mol C4H8(g)和1 mol C2H4(g),测得C3H6的体积分数随时间的变化如图中线I所示。

已知几种气体的燃烧热如下表所示
下列说法正确的是
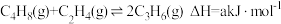 ,一定温度下,向体积为V L密闭容器中充入1 mol C4H8(g)和1 mol C2H4(g),测得C3H6的体积分数随时间的变化如图中线I所示。
,一定温度下,向体积为V L密闭容器中充入1 mol C4H8(g)和1 mol C2H4(g),测得C3H6的体积分数随时间的变化如图中线I所示。
已知几种气体的燃烧热如下表所示
| 气体 | C2H4(g) | C3H6(g) | C4H8(g) |
| 燃烧热/kJ/mol | 1411 | 2049 | 2539 |
| A.C4H8(g)燃烧的热化学方程式可表示为C4H8(g)+6O2(g)=4CO2(g)+4H2O(g) △H=-2539 kJ/mol |
| B.a=148 |
| C.该温度下反应的平衡常数为64 |
| D.图中线Ⅱ可能是其他条件一定,反应在更高温度时进行 |
您最近一年使用:0次
名校
5 . 黄铁矿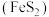 是一种重要的含铁矿物,在潮湿空气中会被缓慢氧化:
是一种重要的含铁矿物,在潮湿空气中会被缓慢氧化: 。工业上常选择黄铁矿为原料制备硫酸,其中发生的反应有:
。工业上常选择黄铁矿为原料制备硫酸,其中发生的反应有: ;
; 。
。 的反应机理如下:
的反应机理如下:
反应Ⅰ: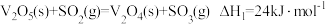
反应Ⅱ:
反应中的能量变化如题图,下列说法不正确的是

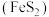 是一种重要的含铁矿物,在潮湿空气中会被缓慢氧化:
是一种重要的含铁矿物,在潮湿空气中会被缓慢氧化: 。工业上常选择黄铁矿为原料制备硫酸,其中发生的反应有:
。工业上常选择黄铁矿为原料制备硫酸,其中发生的反应有: ;
; 。
。 的反应机理如下:
的反应机理如下:反应Ⅰ:
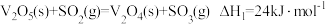
反应Ⅱ:

反应中的能量变化如题图,下列说法不正确的是

A. | B.反应Ⅰ的 |
C.通入过量空气,可提高 的平衡转化率 的平衡转化率 | D.反应速率由反应Ⅰ决定 |
您最近一年使用:0次
2022-09-13更新
|
275次组卷
|
2卷引用:江苏省扬州市江都区邵伯高级中学2022-2023学年高三上学期期初考试化学试题
解题方法
6 . 通过反应Ⅰ:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)可将有机氯化工业的副产品HCl转化为Cl2,在0.2MPa、反应物起始物质的量比 =2条件下,不同温度时HCl平衡转化率如图所示。向反应体系中加入CuCl2,能加快反应速率。
=2条件下,不同温度时HCl平衡转化率如图所示。向反应体系中加入CuCl2,能加快反应速率。
反应Ⅱ:2CuCl2(s)+O2(g)═2CuO(s)+2Cl2(g) △H=125.6kJ·mol﹣1
反应Ⅲ:CuO(s)+2HCl(g)═CuCl2(s)+H2O(g) △H=﹣120.0kJ·mol﹣1
下列说法正确的是

 =2条件下,不同温度时HCl平衡转化率如图所示。向反应体系中加入CuCl2,能加快反应速率。
=2条件下,不同温度时HCl平衡转化率如图所示。向反应体系中加入CuCl2,能加快反应速率。反应Ⅱ:2CuCl2(s)+O2(g)═2CuO(s)+2Cl2(g) △H=125.6kJ·mol﹣1
反应Ⅲ:CuO(s)+2HCl(g)═CuCl2(s)+H2O(g) △H=﹣120.0kJ·mol﹣1
下列说法正确的是

| A.X点的v(正)<v(逆) |
| B.升高温度和增大压强均能提高反应Ⅰ中HCl的平衡转化率 |
C.在0.2MPa、500℃条件下,若起始 <2,HCl的转化率可能达到Y点的 <2,HCl的转化率可能达到Y点的 |
| D.保持其他条件不变,500℃时,使用CuCl2,能使HCl转化率从X点的值升至Y点的值 |
您最近一年使用:0次
7 . 以CO和H2为原料合成甲醇是工业上的成熟方法,直接以CO2为原料生产甲醇是目前的研究热点。我国科学家用CO2人工合成淀粉时,第一步就需要CO2转化为甲醇。
已知:①CO(g)+2H2(g) CH3OH(g) △H1=-90.5kJ·mol-1
CH3OH(g) △H1=-90.5kJ·mol-1
②CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.1kJ·mol-1
CO2(g)+H2(g) △H2=-41.1kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) △H3=-483.6kJ·mol-1
下列说法正确的是
已知:①CO(g)+2H2(g)
 CH3OH(g) △H1=-90.5kJ·mol-1
CH3OH(g) △H1=-90.5kJ·mol-1②CO(g)+H2O(g)
 CO2(g)+H2(g) △H2=-41.1kJ·mol-1
CO2(g)+H2(g) △H2=-41.1kJ·mol-1③2H2(g)+O2(g)=2H2O(g) △H3=-483.6kJ·mol-1
下列说法正确的是
| A.若温度不变,反应①中生成1molCH3OH(l)时,放出的热量大于90.5kJ |
| B.对于②反应,选用高效催化剂,可降低反应的焓变 |
C.CO2与H2合成甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.4kJ·mol-1 CH3OH(g)+H2O(g) △H=-49.4kJ·mol-1 |
| D.以CO2和H2O为原料合成甲醇,同时生成O2,该反应放出能量 |
您最近一年使用:0次
名校
解题方法
8 . 向密闭容器中充入 ,发生反应:
,发生反应: ,达到平衡状态。该反应经过以下两步基元反应完成:i.
,达到平衡状态。该反应经过以下两步基元反应完成:i. ,ii.
,ii. 。下列分析不正确的是
。下列分析不正确的是
 ,发生反应:
,发生反应: ,达到平衡状态。该反应经过以下两步基元反应完成:i.
,达到平衡状态。该反应经过以下两步基元反应完成:i. ,ii.
,ii. 。下列分析不正确的是
。下列分析不正确的是A. 、 、 |
B. |
| C.恒温时,缩小体积,气体颜色变深,是平衡正向移动导致的 |
| D.恒容时,升高温度,气体颜色加深,同时电子发生了转移 |
您最近一年使用:0次
名校
解题方法
9 . 科研小组在相同条件下分别通过反应处理等量的NO:
Ⅰ.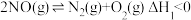 ,
,
Ⅱ.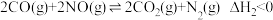 。实验测得NO转化率与时间的关系如图所示,下列说法错误的是
。实验测得NO转化率与时间的关系如图所示,下列说法错误的是

Ⅰ.
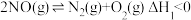 ,
,Ⅱ.
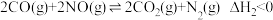 。实验测得NO转化率与时间的关系如图所示,下列说法错误的是
。实验测得NO转化率与时间的关系如图所示,下列说法错误的是
| A.反应Ⅱ为熵减反应 |
| B.2 mol NO(g)的能量高于1 molN2(g)和1 molO2(g)的能量之和 |
| C.反应Ⅰ的热力学趋势大于反应Ⅱ的热力学趋势 |
D.M点反应Ⅰ的平均速率 (NO)大于N点反应Ⅱ的平均速率 (NO)大于N点反应Ⅱ的平均速率 (NO) (NO) |
您最近一年使用:0次
名校
10 . 氢能是清洁的绿色能源。现有一种太阳能两步法甲烷蒸气重整制氢工艺,反应原理为
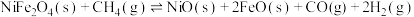

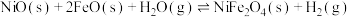

第Ⅰ、Ⅱ步反应的 关系如图所示。下列有关说法正确的是
关系如图所示。下列有关说法正确的是


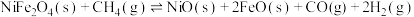

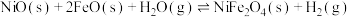

第Ⅰ、Ⅱ步反应的
 关系如图所示。下列有关说法正确的是
关系如图所示。下列有关说法正确的是

A.  |
B.1000℃时,反应 平衡常数 平衡常数 |
C.1000℃时,只考虑反应I时,第Ⅰ步反应平衡时 的平衡分压 的平衡分压 ,则第Ⅰ步反应平衡时混合气体中 ,则第Ⅰ步反应平衡时混合气体中 的体积分数为58.8% 的体积分数为58.8% |
D. 改变反应历程,降低了反应活化能,提升了反应物的平衡转化率 改变反应历程,降低了反应活化能,提升了反应物的平衡转化率 |
您最近一年使用:0次



