名校
解题方法
1 . 已知H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ·mol-1,则反应HCl(g)=  H2(g)+
H2(g)+ Cl2(g)的ΔH为
Cl2(g)的ΔH为
 H2(g)+
H2(g)+ Cl2(g)的ΔH为
Cl2(g)的ΔH为| A.+184.6 kJ·mol-1 | B.-92.3 kJ·mol-1 |
| C.-369.2 kJ·mol-1 | D.+92.3 kJ·mol-1 |
您最近一年使用:0次
2023-08-26更新
|
1494次组卷
|
86卷引用:江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高二下学期期中考试化学试题
江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高二下学期期中考试化学试题(已下线)2013届江苏省淮阴中学高一下学期期初考试化学试卷江苏省东台市创新高级中学2018-2019学年高二下学期3月月考化学试题江苏省沭阳县2018-2019学年高二下学期期中调研测试化学试题安徽省安庆市九一六学校2020-2021学年高二下学期开学考试化学试题山西省沁源县第一中学2020-2021学年高二下学期开学考试化学试题贵州省龙里县九八五实验学校2020-2021学年高二上学期1月月考化学试题辽宁省恒仁满族自治县第二高级中学2020-2021学年高二上学期期末考试化学试题(已下线)1.1.2 反应热的测量与计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)云南省玉溪第一中学2021-2022学年高二上学期第一次月考化学试题吉林省通化县综合高级中学2021-2022学年高二上学期期中考试化学试题安徽省宣城市六校2021-2022学年高二上学期期中联考化学试题河南省中原名校2021-2022学年高二上学期12月联考化学试题福建省三明第一中学2021-2022学年高二上学期第二次月考化学试题海南省白沙中学2021-2022学年高二上学期第一次月考化学试题(已下线)09-10年福州格致中学高一下学期第三学段质量检查化学卷(已下线)2010年内蒙古赤峰市田家炳中学高二上学期期中考试化学试卷(已下线)2010-2011学年广东省中山市桂山中学高二下期中考试化学试卷(已下线)2010—2011学年吉林省长春外国语学校高一下学期期末考试化学试卷理(已下线)2011-2012年河南省长葛市第三实验高中高二上学期第一次月考化学试卷(已下线)2011-2012年广东省广雅中学高二上学期期中考试化学(理)试卷(已下线)2011-2012学年山东省济南外国语学校高二上学期期中考试化学(理)试卷(已下线)2011-2012学年福建泉州晋江市季延中学高二下学期期中化学试卷(已下线)2012-2013学年福建省晋江市季延中学高二下学期期中考试化学试卷2014-2015学年内蒙古巴市一中高二10月月考化学试卷2014-2015学年甘肃省民乐一中高二上学期第一次月考化学试卷2015-2016学年青海省高级中学高二上9月质检化学试卷2015-2016学年贵州省遵义航天中学高二上期末化学试卷2015-2016学年浙江省温州市瑞安市龙翔中学高二上第三次月考化学卷2016-2017学年北大附中河南分校高二上第一次月考化学卷2016-2017学年贵州省贵阳六中高二上10月月考化学卷(已下线)1.3.1 盖斯定律吉林省汪清县第六中学2017-2018学年高二9月月考化学试题陕西省西安市电子科技中学2017-2018学年高二上学期第一次月考化学试题广东省阳东广雅学校2017-2018学年高二9月月考化学试题河北省邢台第三中学2017-2018学年高二9月月考化学试题天津市杨柳青一中2017-2018第一学期高二第一次化学月考高中化学人教版 选修四 第一章 化学反应与能量 第三节 化学反应热的计算 化学反应热的计算第一课时(盖斯定律)安徽省滁州市(九校)2017-2018学年高二上学期期末考试化学试题四川省成都七中实验学校2018-2019学年高二上学期10月月考化学试题黑龙江省伊春市第二中学2018-2019学年高二(理)上学期期中考试化学试题陕西省黄陵中学2018-2019学年高二(普通班)上学期期末考试化学试题【区级联考】北京市西城区2018-2019学年高二上学期期末考试化学试题【校级联考】河北省鸡泽县第一中学2018-2019学年高一下学期3月月考化学试题步步为赢 高二化学暑假作业:作业七 化学反应与能量陕西省吴起高级中学2018-2019学年高一下学期第二次月考基础卷化学试题吉林省吉林地区普通高中友好学校联合体第三十一届2019-2020学年高二上学期期中考试化学试题河北省邢台市第八中学2019-2020学年高二上学期第一次月考化学试题甘肃省白银市会宁县第四中学2019-2020学年高二上学期期中考试化学试题内蒙古呼和浩特开来中学2019-2020学年高二上学期期中考试化学试题湖南省永州市双牌县第二中学2019-2020学年高二上学期期中考试化学试题(选考)安徽省黄山市“八校联盟”2019-2020学年高二上学期期中考试化学试题河北省保定市易县中学2019-2020学年高一(B部)下学期3月月考化学试题辽宁省大连市普兰店市第一中学2019-2020学年高二上学期期末考试化学试题湖南省长沙市雨花区2018-2019学年高二上学期期末考试化学(理)试题福建省永安市第三中学2020-2021学年高二10月月考化学(学考班)试题吉林省松原市乾安县第七中学2020-2021学年高二上学期第一次教学质量检测化学试题吉林省通化县综合高级中学2020-2021学年高二上学期期中考试化学试题甘肃省兰州市第四片区2020-2021学年高二上学期期中考试化学(理)试题宁夏长庆高级中学2020-2021学年高二上学期第一次月考化学试题福建省三明市三地三校2020-2021学年高二上学期期中联考化学试题北京市第四十三中学2020-2021学年高二上学期12月月考化学试题河南正阳县高级中学2020-2021学年高二上学期第三次素质检测化学试题陕西省咸阳百灵中学2020-2021学年高二上学期期中考试化学试题广东省东莞市二中2020-2021学年上学期高二10月考试化学试题海南省海南鑫源高级中学2019-2020学年高二上学期期末考试化学试题河北省石家庄市2019~2020学年高二上学期期末考试化学试题湖南省郴州市湘南中学2019-2020学年高二上学期期中考试化学试题(高考班)云南省曲靖市宣威市第七中学2021-2022学年高二下学期2月考试化学试题河南省温县第一高级中学2021-2022学年高二上学期1月月考化学试题福建省莆田华侨中学2021-2022学年高二上学期期中考试化学试题福建省莆田华侨中学2021-2022学年高二上学期期中考试化学试题北京市第七中学2022-2023学年高二上学期期中化学试题广东省广州市从化区从化中学2022-2023学年高二上学期期中考试化学试题第3课时 反应焓变的计算【定心卷】1.1.3 热化学方程式随堂练习-人教版2023-2024学年选择性必修1江西省抚州市乐安县第二中学2023-2024学年高二上学期11月期中化学试题(已下线)BBWYhjhx1102陕西省西安市鄠邑区2023-2024学年高二上学期期中质量检测化学试题北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题四川省泸州市泸县第五中学2023-2024学年高二上学期12月月考化学试题云南省宣威市第三中学2023-2024学年高二上学期第四次月考化学试题江西省金溪县第一中学、广昌一中、南丰一中2023-2024学年高二上学期第一次月考化学试题新疆乌鲁木齐市六校联考2023-2024学年高二上学期期末考试化学试题河北省石家庄康福外国语学校2023-2024学年高二上学期期中考试化学试题宁夏开元学校2023-2024学年高二学年下学期开学收心测试化学试题
解题方法
2 . 回答下列小题
(1)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意如图:
。两步反应的能量变化示意如图:
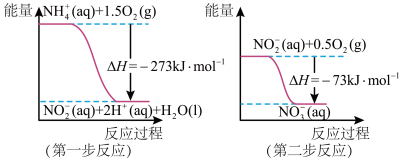
①第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是___________ 。
②1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___________ 。
(2)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463kJ·mol-1,O=O键能为498kJ·mol-1,计算H—H键能为___________ kJ·mol-1.
(3)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=___________ kJ·mol-1.
(1)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意如图:
。两步反应的能量变化示意如图:
①第一步反应是
②1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(2)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463kJ·mol-1,O=O键能为498kJ·mol-1,计算H—H键能为
(3)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=
您最近一年使用:0次
3 . 由于雾霾严重,长沙市19年12月15、16日在部分路段施行了限行。已知汽车尾气排放出的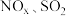 等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
(1)汽车尾气中的 和
和 在一定温度和催化剂条件下可发生如下反应:
在一定温度和催化剂条件下可发生如下反应:
已知:① 燃烧热的
燃烧热的
② ,则
,则
___________
(2)某研究小组对反应 进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比
进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比 进行多组实验(各次实验的温度可能相同,也可能不同),测定
进行多组实验(各次实验的温度可能相同,也可能不同),测定 的平衡转化率
的平衡转化率 ,部分实验结果如图1所示。
,部分实验结果如图1所示。

①如果将图中B点的平衡状态改变为C点的平衡状态,应采取的措施是___________
②图中A、C两点对应的实验温度分别为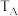 和
和 ,通过判断:
,通过判断: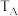
___________  (填“>”“=”或“<”)
(填“>”“=”或“<”)
(3)一定条件下,将 与
与 以体积比1:1置于恒温恒容的密闭容器中发生反应:
以体积比1:1置于恒温恒容的密闭容器中发生反应: ,下列能说明反应达到平衡状态的是
,下列能说明反应达到平衡状态的是___________ (填字母)。
a、混合气体的密度保持不变b、 的物质的量保持不变
的物质的量保持不变
c、容器内混合气体原子总数不变d、每生成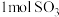 的同时消耗
的同时消耗
(4)工业废气也是产生雾霾的重要原因,某厂采用湿法 氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。
氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。
① 水解时生成
水解时生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式___________
②过二硫酸钾可通过电解 溶液的方法制得。电解液中含硫微粒主要存在形式与
溶液的方法制得。电解液中含硫微粒主要存在形式与 的关系如图2所示。
的关系如图2所示。

已知在阳极放电的离子主要是 ,阳极区电解质溶液的
,阳极区电解质溶液的 范围为
范围为___________ ﹔阳极的电极反应式为___________ 。
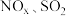 等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。(1)汽车尾气中的
 和
和 在一定温度和催化剂条件下可发生如下反应:
在一定温度和催化剂条件下可发生如下反应:
已知:①
 燃烧热的
燃烧热的
②
 ,则
,则
(2)某研究小组对反应
 进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比
进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比 进行多组实验(各次实验的温度可能相同,也可能不同),测定
进行多组实验(各次实验的温度可能相同,也可能不同),测定 的平衡转化率
的平衡转化率 ,部分实验结果如图1所示。
,部分实验结果如图1所示。
①如果将图中B点的平衡状态改变为C点的平衡状态,应采取的措施是
②图中A、C两点对应的实验温度分别为
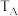 和
和 ,通过判断:
,通过判断: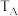
 (填“>”“=”或“<”)
(填“>”“=”或“<”)(3)一定条件下,将
 与
与 以体积比1:1置于恒温恒容的密闭容器中发生反应:
以体积比1:1置于恒温恒容的密闭容器中发生反应: ,下列能说明反应达到平衡状态的是
,下列能说明反应达到平衡状态的是a、混合气体的密度保持不变b、
 的物质的量保持不变
的物质的量保持不变c、容器内混合气体原子总数不变d、每生成
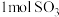 的同时消耗
的同时消耗
(4)工业废气也是产生雾霾的重要原因,某厂采用湿法
 氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。
氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。①
 水解时生成
水解时生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式②过二硫酸钾可通过电解
 溶液的方法制得。电解液中含硫微粒主要存在形式与
溶液的方法制得。电解液中含硫微粒主要存在形式与 的关系如图2所示。
的关系如图2所示。
已知在阳极放电的离子主要是
 ,阳极区电解质溶液的
,阳极区电解质溶液的 范围为
范围为
您最近一年使用:0次
4 . 在丁烯(C4H8)催化裂解为丙烯(C3H6)、乙烯(C2H4)的反应体系中,主要发生反应的热化学方程式为:反应I: △H1=a kJ/mol;反应II:
△H1=a kJ/mol;反应II: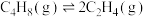 △H2=b kJ/mol。在0.1 MPa的恒压密闭容器中,丁烯催化裂解体系中各组分
△H2=b kJ/mol。在0.1 MPa的恒压密闭容器中,丁烯催化裂解体系中各组分平衡时 的质量分数随温度变化的关系如图所示。下列说法错误 的是
 △H1=a kJ/mol;反应II:
△H1=a kJ/mol;反应II: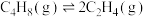 △H2=b kJ/mol。在0.1 MPa的恒压密闭容器中,丁烯催化裂解体系中各组分
△H2=b kJ/mol。在0.1 MPa的恒压密闭容器中,丁烯催化裂解体系中各组分
A.反应: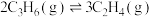  kJ/mol kJ/mol |
| B.由图可知:a<0<b |
| C.在催化剂许可的前提下,温度控制在450℃左右有利于制取丙烯 |
| D.其他条件相同时,适当充入惰性气体,有利于提高乙烯和丙烯的产量 |
您最近一年使用:0次
解题方法
5 . 回答下列问题:
(1)已知: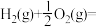
 ,
,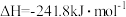
 ,
,
写出焦炭与水蒸气反应的热化学方程式_______ 。
(2)氢化亚铜( )是一种难溶物质,用
)是一种难溶物质,用 溶液和“另一物质”在40~50℃时反应可生成氢化亚铜。
溶液和“另一物质”在40~50℃时反应可生成氢化亚铜。 不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;
不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;  在酸性条件下发生反应:
在酸性条件下发生反应: 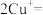
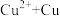 。根据以上信息,结合自己所掌握的化学知识,回答下列问题:
。根据以上信息,结合自己所掌握的化学知识,回答下列问题:
①用 溶液和“另一物质”制
溶液和“另一物质”制 的反应中,用氧化还原观点分析,“另一物质”在反应中作
的反应中,用氧化还原观点分析,“另一物质”在反应中作_______ (填“氧化剂”或“还原剂”)。
② 写出 在氯气中燃烧的化学方程式:
在氯气中燃烧的化学方程式:_______ 。
③ 溶解在稀盐酸中生成的气体是
溶解在稀盐酸中生成的气体是_______ (填化学式)。
④ 如果把 溶解在足量的稀硝酸中,生成的气体只有
溶解在足量的稀硝酸中,生成的气体只有 ,请写出
,请写出 溶解在足量稀硝酸中反应的离子方程式:
溶解在足量稀硝酸中反应的离子方程式:_______ 。
(1)已知:
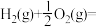
 ,
,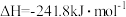
 ,
,
写出焦炭与水蒸气反应的热化学方程式
(2)氢化亚铜(
 )是一种难溶物质,用
)是一种难溶物质,用 溶液和“另一物质”在40~50℃时反应可生成氢化亚铜。
溶液和“另一物质”在40~50℃时反应可生成氢化亚铜。 不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;
不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;  在酸性条件下发生反应:
在酸性条件下发生反应: 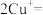
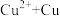 。根据以上信息,结合自己所掌握的化学知识,回答下列问题:
。根据以上信息,结合自己所掌握的化学知识,回答下列问题:①用
 溶液和“另一物质”制
溶液和“另一物质”制 的反应中,用氧化还原观点分析,“另一物质”在反应中作
的反应中,用氧化还原观点分析,“另一物质”在反应中作② 写出
 在氯气中燃烧的化学方程式:
在氯气中燃烧的化学方程式:③
 溶解在稀盐酸中生成的气体是
溶解在稀盐酸中生成的气体是④ 如果把
 溶解在足量的稀硝酸中,生成的气体只有
溶解在足量的稀硝酸中,生成的气体只有 ,请写出
,请写出 溶解在足量稀硝酸中反应的离子方程式:
溶解在足量稀硝酸中反应的离子方程式:
您最近一年使用:0次
6 . 氯及含氯物质在生产、生活中具有广泛的应用。Deacon催化氧化法将HCl转化为Cl2的反应为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g) △H=-116kJ·mol-1
研究发现CuCl2(s)催化反应的过程如下:
反应i:CuCl2(s)=CuCl(s)+ Cl2(g) △H1=+83kJ·mol-l
Cl2(g) △H1=+83kJ·mol-l
反应ii:CuCl(s)+ O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) △H2=-20kJ·mol-l
Cl2(g) △H2=-20kJ·mol-l
反应iii:……
下列关于Deacon催化氧化法制Cl2的说法正确的是
研究发现CuCl2(s)催化反应的过程如下:
反应i:CuCl2(s)=CuCl(s)+
 Cl2(g) △H1=+83kJ·mol-l
Cl2(g) △H1=+83kJ·mol-l反应ii:CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) △H2=-20kJ·mol-l
Cl2(g) △H2=-20kJ·mol-l反应iii:……
下列关于Deacon催化氧化法制Cl2的说法正确的是
| A.总反应中反应物的键能总和大于生成物的键能总和 |
| B.反应ii中,生成22.4LCl2转移2mole- |
| C.推断反应iii应为CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) △H3=-242kJ·mol-1 |
| D.由反应过程可知催化剂参与反应,通过改变反应路径提高反应速率 |
您最近一年使用:0次
7 . 利用太阳能光解水,制备的H2用于还原CO2合成甲醇,可实现资源的再利用。
(1)中国科学家研究的复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光高效分解水,其原理如图1所示。反应I的化学方程式为_____ 。
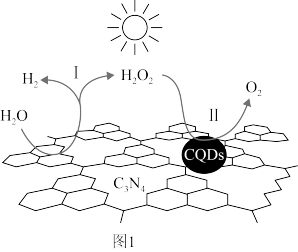
(2)H2和CO、CO2在催化剂的作用下合成甲醇的主要反应如下:
第一步:CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41 kJ·mol-1
CO(g)+H2O(g) △H1=+41 kJ·mol-1
第二步:CO(g)+2H2(g) CH3OH(g) △H2=-99 kJ·mol-1
CH3OH(g) △H2=-99 kJ·mol-1
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=
CH3OH(g)+H2O(g) △H=_____ 。
②第二步反应中的相关化学键的键能(E)数据如表,试计算x=_____ 。(提示:CO中的化学键与N2中的化学键类似)
(3)在水溶液中电解CO2生成甲醇的原理如图2所示。
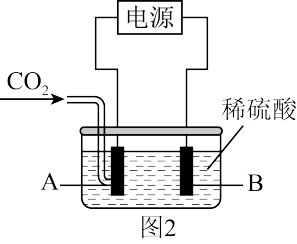
①写出A电极生成甲醇的电极反应式:____ 。
②A极生成1 mol甲醇时,B极生成气体在标准状况下的体积是_____ 。
(4)金刚石和石墨燃烧反应中的能量变化如图3所示。

图3
由图3可知:石墨的燃烧热△H=____ 。
(5)燃煤烟气中的NOx、SO2经处理后可被吸收。若烟气主要成分为NO、SO2,可通过电解法除去,其原理如图4所示。
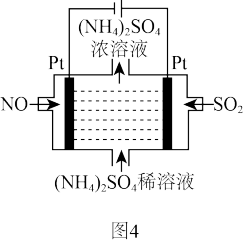
阴极的电极反应式为____ 。电解过程得到的产物为_____ 。
(1)中国科学家研究的复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光高效分解水,其原理如图1所示。反应I的化学方程式为

(2)H2和CO、CO2在催化剂的作用下合成甲醇的主要反应如下:
第一步:CO2(g)+H2(g)
 CO(g)+H2O(g) △H1=+41 kJ·mol-1
CO(g)+H2O(g) △H1=+41 kJ·mol-1第二步:CO(g)+2H2(g)
 CH3OH(g) △H2=-99 kJ·mol-1
CH3OH(g) △H2=-99 kJ·mol-1CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=
CH3OH(g)+H2O(g) △H=②第二步反应中的相关化学键的键能(E)数据如表,试计算x=
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/kJ·mol-1 | 436 | x | 1076 | 465 | 413 |

①写出A电极生成甲醇的电极反应式:
②A极生成1 mol甲醇时,B极生成气体在标准状况下的体积是
(4)金刚石和石墨燃烧反应中的能量变化如图3所示。

图3
由图3可知:石墨的燃烧热△H=
(5)燃煤烟气中的NOx、SO2经处理后可被吸收。若烟气主要成分为NO、SO2,可通过电解法除去,其原理如图4所示。

阴极的电极反应式为
您最近一年使用:0次
解题方法
8 . 请回答下列问题:
(1)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图1所示是高铁电池的模拟实验装置。


①该电池放电时正极反应式为_______ 。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向_______ (填“左”或“右”)移动;
③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有_______ 。
(2)铜是人类最早使用的金属,它与人类生产、生活关系密切,请运用所学知识解释下列与铜有关的化学现象。

①如图甲,在硫酸型酸雨地区,不纯的铜制品发生电化学腐蚀,Cu发生_______ (填“氧化”或“还原”)反应,写出正极的电极反应式:_______ 。
②如图乙,将螺旋状的铜丝在酒精灯上灼烧,铜丝变黑色,然后将红热的铜丝插入NH4Cl固体中,过一会取出,发现插入部分黑色变为光亮的红色,查阅资料可知,该过程有N2生成,写出由黑色变为光亮红色过程中反应的化学方程式:_______ 。
(3)一定温度下,反应H2+Cl2=2HCl中的某一基元反应为H2+Cl=HCl+H,其能量变化如图所示。H…H…Cl表示反应物分子旧化学键没有完全断裂、新化学键没有完全形成的过渡态。

该基元反应的活化能为_______ kJ/mol,ΔH为_______ kJ/mol。
(4)键能也可以用于估算化学反应的反应热(ΔH)。下表是部分化学键的键能数据:
已知白磷的标准燃烧热为-2378kJ/mol,白磷的结构为正四面体,白磷完全燃烧的产物结构如图所示,则上表中X=_______ 。

(5)已知:Ⅰ.C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ/mol
Ⅱ.2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ/mol
Ⅲ.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599.2kJ/mol
则由C(石墨,s)和H2(g)反应生成1mol C2H2(g)的焓变为_______ 。
(1)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图1所示是高铁电池的模拟实验装置。


①该电池放电时正极反应式为
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
(2)铜是人类最早使用的金属,它与人类生产、生活关系密切,请运用所学知识解释下列与铜有关的化学现象。

①如图甲,在硫酸型酸雨地区,不纯的铜制品发生电化学腐蚀,Cu发生
②如图乙,将螺旋状的铜丝在酒精灯上灼烧,铜丝变黑色,然后将红热的铜丝插入NH4Cl固体中,过一会取出,发现插入部分黑色变为光亮的红色,查阅资料可知,该过程有N2生成,写出由黑色变为光亮红色过程中反应的化学方程式:
(3)一定温度下,反应H2+Cl2=2HCl中的某一基元反应为H2+Cl=HCl+H,其能量变化如图所示。H…H…Cl表示反应物分子旧化学键没有完全断裂、新化学键没有完全形成的过渡态。

该基元反应的活化能为
(4)键能也可以用于估算化学反应的反应热(ΔH)。下表是部分化学键的键能数据:
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/(kJ/mol) | 172 | 335 | 498 | X |

(5)已知:Ⅰ.C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ/mol
Ⅱ.2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ/mol
Ⅲ.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599.2kJ/mol
则由C(石墨,s)和H2(g)反应生成1mol C2H2(g)的焓变为
您最近一年使用:0次
名校
9 .  (主要指
(主要指 和
和 )是大气主要污染物之一。
)是大气主要污染物之一。
(1)用水吸收 的相关热化学方程式如下:
的相关热化学方程式如下:

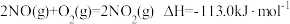
在上述吸收过程中调整 与
与 的比例进行反应可以达到最大程度的吸收,反应
的比例进行反应可以达到最大程度的吸收,反应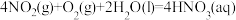 的
的
_______  。
。
(2)NH3的选择性催化还原法是应用最为广泛的脱硝技术,反应原理: ,当生成1molN2时,转移的电子为
,当生成1molN2时,转移的电子为_______ mol。
(3)用间接电化学法同时去除烟气中 和
和 ,装置如下图所示。
,装置如下图所示。

①电极M上的电极反应式为_______ 。
②写出吸收池中NO被吸收的离子方程式_______ 。
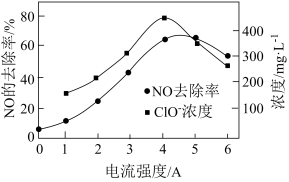
(4)电解氧化法可将废气中NO转变为硝态氮。电解 溶液,NO的去除率、溶液中相关成的浓度与电流强度的关系如图所示。电流强度在
溶液,NO的去除率、溶液中相关成的浓度与电流强度的关系如图所示。电流强度在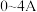 时,随着电流强度的增大,NO的去除率升高的原因是
时,随着电流强度的增大,NO的去除率升高的原因是_______
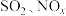 (主要指
(主要指 和
和 )是大气主要污染物之一。
)是大气主要污染物之一。(1)用水吸收
 的相关热化学方程式如下:
的相关热化学方程式如下:
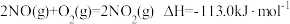
在上述吸收过程中调整
 与
与 的比例进行反应可以达到最大程度的吸收,反应
的比例进行反应可以达到最大程度的吸收,反应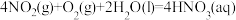 的
的
 。
。(2)NH3的选择性催化还原法是应用最为广泛的脱硝技术,反应原理:
 ,当生成1molN2时,转移的电子为
,当生成1molN2时,转移的电子为(3)用间接电化学法同时去除烟气中
 和
和 ,装置如下图所示。
,装置如下图所示。
①电极M上的电极反应式为
②写出吸收池中NO被吸收的离子方程式
(4)电解氧化法可将废气中NO转变为硝态氮。电解
 溶液,NO的去除率、溶液中相关成的浓度与电流强度的关系如图所示。电流强度在
溶液,NO的去除率、溶液中相关成的浓度与电流强度的关系如图所示。电流强度在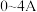 时,随着电流强度的增大,NO的去除率升高的原因是
时,随着电流强度的增大,NO的去除率升高的原因是
您最近一年使用:0次
2022-05-04更新
|
160次组卷
|
2卷引用:江苏省连云港市东海县2021-2022学年高二上学期期中考试化学试题(选修)
10 . 十九大报告提出要对环境问题进行全面、系统的可持续治理。绿色能源堤实施可持续发展的重要途径,利用生物乙醇来制取绿色能源氢气的部分反应过程如图所示:
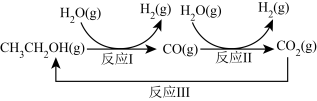
(1)已知:CO(g)+H2O(g) CO2(g)+H2(g) △H1=-41kJ/mol
CO2(g)+H2(g) △H1=-41kJ/mol
CH3CH2OH(g)+3H2O(g) 2CO2(g)+6H2(g) △H2=+174.1kJ/mol
2CO2(g)+6H2(g) △H2=+174.1kJ/mol
请写出反应Ⅰ的热化学方程式:________ 。
(2)反应Ⅱ,在进气比[n(CO):n(H2O)]不同时,测得相应的CO平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)
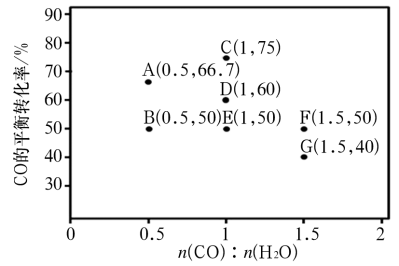
①若A、E和G三点对应的反应温度相同,则平衡常数KA=KE=KG=_______ (填数值)。在该温度下,要提高CO平衡转化率,除了改变进气比之外,还可采取的措施是:________ 。
②比较A、B两点对应的反应速率大小:vA_______ vB(填“<”“=”或“>”)。
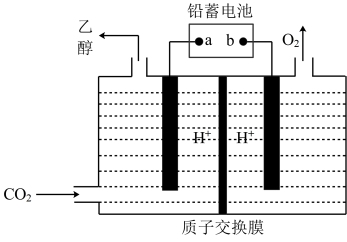
(3)以铅蓄电池为电源可将CO2转化为乙醇,其原理如图所示,电解所用电极材料均为惰性电极。该电解池阴极上的电极反应式为:_______ ;每生成0.5mol乙醇,理论上需消耗铅蓄电池中_______ mol硫酸。

(1)已知:CO(g)+H2O(g)
 CO2(g)+H2(g) △H1=-41kJ/mol
CO2(g)+H2(g) △H1=-41kJ/molCH3CH2OH(g)+3H2O(g)
 2CO2(g)+6H2(g) △H2=+174.1kJ/mol
2CO2(g)+6H2(g) △H2=+174.1kJ/mol请写出反应Ⅰ的热化学方程式:
(2)反应Ⅱ,在进气比[n(CO):n(H2O)]不同时,测得相应的CO平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)

①若A、E和G三点对应的反应温度相同,则平衡常数KA=KE=KG=
②比较A、B两点对应的反应速率大小:vA
(3)以铅蓄电池为电源可将CO2转化为乙醇,其原理如图所示,电解所用电极材料均为惰性电极。该电解池阴极上的电极反应式为:

您最近一年使用:0次
2022-04-12更新
|
255次组卷
|
2卷引用:江苏省海安高级中学2021-2022学年高二上学期阶段测试(二)化学试题



