解题方法
1 . 在碳循环中,以 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。
_______ 0(填“>”、“<”或“=”)。从图像分析决定生产尿素的总反应的反应速率的步骤是第_______ 步反应,并说明理由______________ 。
 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。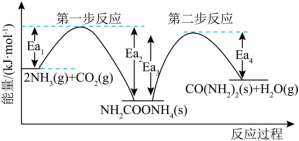

您最近一年使用:0次
解题方法
2 . 我国科学家利用两种不同的纳米催化剂(Co3O4/Pt、N- Co3O4/Pt)在室温水汽条件下实现高效CO催化氧化(C16O+ 16O2=C16O2),其反应历程中相对能量的变化如下图所示(TS1、TS2、TS3分别代表过渡态1、过渡态2、过渡态3)。下列说法错误的是
16O2=C16O2),其反应历程中相对能量的变化如下图所示(TS1、TS2、TS3分别代表过渡态1、过渡态2、过渡态3)。下列说法错误的是
 16O2=C16O2),其反应历程中相对能量的变化如下图所示(TS1、TS2、TS3分别代表过渡态1、过渡态2、过渡态3)。下列说法错误的是
16O2=C16O2),其反应历程中相对能量的变化如下图所示(TS1、TS2、TS3分别代表过渡态1、过渡态2、过渡态3)。下列说法错误的是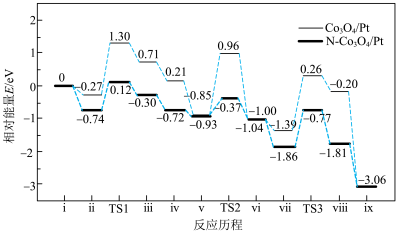
| A.效果较好的催化剂是N-Co3O4/Pt |
| B.若利用H218O进行同位素标记实验,检测到以上反应中有C16O18O和C18O2生成,说明O-H键断裂 |
C.反应:C16O(g)+ 16O2(g)=C16O2 (g)的∆H<0 16O2(g)=C16O2 (g)的∆H<0 |
| D.若ⅱ表示H2O被吸附在催化剂表面,则Co3O4/Pt更容易吸附H2O |
您最近一年使用:0次
3 . 化学反应过程中释放或吸收的热量在生活、生产、科技及科研中应用广泛。
(1)制作冷敷袋可利用______ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”为生活带来便利,它可利用下面______ (填字母)反应放热加热食物。
(3)已知:2molH2与足量O2充分燃烧生成液态水时放出572kJ热量。
①该反应的能量变化可用图中的______ (填字母)表示。
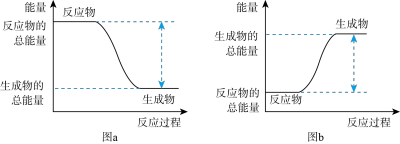
②写出H2燃烧生成液态水的热化学反应方程式____________ 。
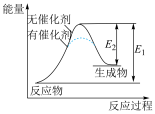
(4)某反应过程中能量变化如图所示,下列有关叙述正确的是______。
(5)计算化学反应中的能量变化有多种途径。
①通过化学键的键能计算。已知:
计算可得:H2(g)+Cl2(g)=2HCl(g) ΔH =______ kJ/mol
②通过盖斯定律计算。已知:
2Na(s)+ O2(g)=Na2O (s) ΔH=-414kJ/mol
O2(g)=Na2O (s) ΔH=-414kJ/mol
2Na(s)+O2(g)=Na2O2(s) ΔH=-511kJ/mol
写出Na2O2与Na反应生成Na2O的热化学方程式:__________________ 。
(6)化学能与其他能量间的转换在生活中处处可见,比如某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用30%H2SO4溶液作电解质溶液,其简易装置如图所示。
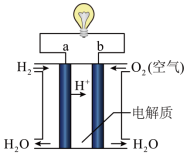
在这个燃料电池中,正极的电极反应为____________ 。若在标况下,消耗了33.6L的氢气,此时电路中转移的电子数目为______ 个(用阿伏加德罗常数表示)。
(1)制作冷敷袋可利用
(2)“即热饭盒”为生活带来便利,它可利用下面______ (填字母)反应放热加热食物。
| A.浓硫酸和水 | B.生石灰和水 | C.纯碱和水 | D.食盐和白醋 |
(3)已知:2molH2与足量O2充分燃烧生成液态水时放出572kJ热量。
①该反应的能量变化可用图中的

②写出H2燃烧生成液态水的热化学反应方程式
(4)某反应过程中能量变化如图所示,下列有关叙述正确的是______。

| A.该反应为放热反应 |
| B.催化剂改变了化学反应的热效应 |
| C.催化剂不改变化学反应过程 |
| D.反应中断开化学键吸收的总能量高于形成化学键放出的总能量 |
(5)计算化学反应中的能量变化有多种途径。
①通过化学键的键能计算。已知:
| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能(kJ/mol) | 436 | 247 | 434 |
②通过盖斯定律计算。已知:
2Na(s)+
 O2(g)=Na2O (s) ΔH=-414kJ/mol
O2(g)=Na2O (s) ΔH=-414kJ/mol 2Na(s)+O2(g)=Na2O2(s) ΔH=-511kJ/mol
写出Na2O2与Na反应生成Na2O的热化学方程式:
(6)化学能与其他能量间的转换在生活中处处可见,比如某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用30%H2SO4溶液作电解质溶液,其简易装置如图所示。

在这个燃料电池中,正极的电极反应为
您最近一年使用:0次
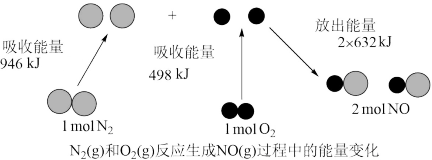
4 . 下图表示 (g)和
(g)和 (g)反应生成NO(g)过程中的能量变化,下列说法不正确的是
(g)反应生成NO(g)过程中的能量变化,下列说法不正确的是
 (g)和
(g)和 (g)反应生成NO(g)过程中的能量变化,下列说法不正确的是
(g)反应生成NO(g)过程中的能量变化,下列说法不正确的是
A. 化学性质稳定,是因为断开 化学性质稳定,是因为断开 分子中的化学键需要吸收较多能量 分子中的化学键需要吸收较多能量 |
B.1mol  (g)和1mol (g)和1mol  (g)所具有的能量之和比2mol NO(g)的能量高 (g)所具有的能量之和比2mol NO(g)的能量高 |
C.1mol  (g)和1mol (g)和1mol  (g)后应生成2mol NO(g),需吸收能量180kJ (g)后应生成2mol NO(g),需吸收能量180kJ |
D.NO(g)分解为 (g)和 (g)和 (g)是放热反应 (g)是放热反应 |
您最近一年使用:0次
5 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ/mol
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ/mol
总反应的△H=_______ kJ/mol;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是_______ (填标号),判断的理由是_______ 。
A.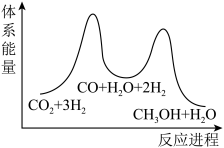 B.
B.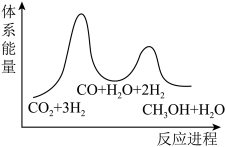
C.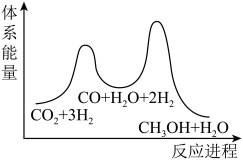 D.
D.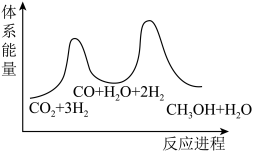
(2)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
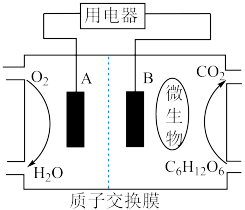
①B为生物燃料电池的_______ (填“正”或“负”)极。
②正极反应式为_______ 。
③电池工作过程中,H+将移向_______ (填“正”或“负”)极。
④在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是_______ 。
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ/mol
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ/mol
总反应的△H=
A.
 B.
B.
C.
 D.
D.
(2)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①B为生物燃料电池的
②正极反应式为
③电池工作过程中,H+将移向
④在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是
您最近一年使用:0次
6 . 化学反应过程中伴随着能量变化。
(1)下列变化中属于吸热反应的是___________ 。
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③甲烷在氧气中的燃烧反应 ④ 固体溶于水 ⑤
固体溶于水 ⑤ 与
与 反应
反应
其中⑤中发生的化学方程式为___________ 。
(2)有机物M经过太阳光光照可转化成N,转化过程如下:
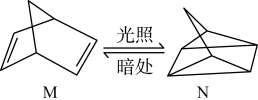
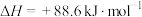 ,则M、N相比,较稳定的是
,则M、N相比,较稳定的是___________ 。
(3)在25℃、101kPa下。液态甲醇( )的燃烧热为726.5kJ/mol,已知:
)的燃烧热为726.5kJ/mol,已知:
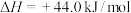 ,写出该条件下甲醇燃烧生成水蒸气的热化学方程式
,写出该条件下甲醇燃烧生成水蒸气的热化学方程式___________ 。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③甲烷在氧气中的燃烧反应 ④
 固体溶于水 ⑤
固体溶于水 ⑤ 与
与 反应
反应其中⑤中发生的化学方程式为
(2)有机物M经过太阳光光照可转化成N,转化过程如下:

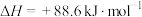 ,则M、N相比,较稳定的是
,则M、N相比,较稳定的是(3)在25℃、101kPa下。液态甲醇(
 )的燃烧热为726.5kJ/mol,已知:
)的燃烧热为726.5kJ/mol,已知:
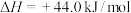 ,写出该条件下甲醇燃烧生成水蒸气的热化学方程式
,写出该条件下甲醇燃烧生成水蒸气的热化学方程式
您最近一年使用:0次
解题方法
7 . 工业上用 和
和 合成甲醇涉及以下反应:①
合成甲醇涉及以下反应:① ;②
;②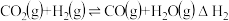 。在催化剂作用下,将
。在催化剂作用下,将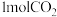 和
和 混合充入一恒容密闭容器中进行反应,达到平衡时,
混合充入一恒容密闭容器中进行反应,达到平衡时, 的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列说法不正确的是
的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列说法不正确的是
 和
和 合成甲醇涉及以下反应:①
合成甲醇涉及以下反应:① ;②
;②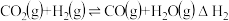 。在催化剂作用下,将
。在催化剂作用下,将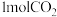 和
和 混合充入一恒容密闭容器中进行反应,达到平衡时,
混合充入一恒容密闭容器中进行反应,达到平衡时, 的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列说法不正确的是
的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列说法不正确的是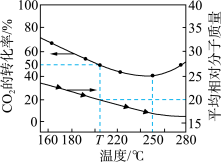
| A.反应①为放热反应 |
B.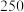 ℃以后反应①的选择性减小 ℃以后反应①的选择性减小 |
C. ℃,达平衡时反应②的选择性为 ℃,达平衡时反应②的选择性为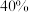 |
D. ℃,达平衡时 ℃,达平衡时 的分压是 的分压是 的 的 倍 倍 |
您最近一年使用:0次
8 . 下列有关反应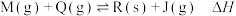 的说法正确的是
的说法正确的是
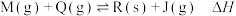 的说法正确的是
的说法正确的是A.该反应的 |
B. 反应物的总能量一生成物的总能量 反应物的总能量一生成物的总能量 |
| C.J的生成速率和Q的消耗速率相等说明该反应达到平衡状态 |
D.该反应的平衡常数表达式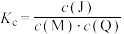 |
您最近一年使用:0次
9 .  与
与 发生反应生成
发生反应生成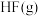 的过程中能量变化如图所示[
的过程中能量变化如图所示[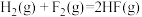
 ]。下列说法正确的是
]。下列说法正确的是
 与
与 发生反应生成
发生反应生成 的过程中能量变化如图所示[
的过程中能量变化如图所示[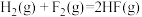
 ]。下列说法正确的是
]。下列说法正确的是
| A.过程Ⅰ放出热量 |
B.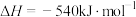 |
| C.过程II涉及极性键断裂 |
D.过程III可表示为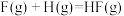 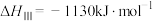 |
您最近一年使用:0次
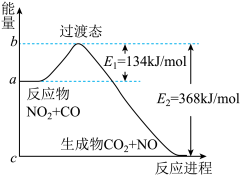
10 . 可逆反应NO2(g)+CO(g) CO2(g)+NO(g)反应过程中的能量变化如图所示,下列说法正确的是
CO2(g)+NO(g)反应过程中的能量变化如图所示,下列说法正确的是
 CO2(g)+NO(g)反应过程中的能量变化如图所示,下列说法正确的是
CO2(g)+NO(g)反应过程中的能量变化如图所示,下列说法正确的是
| A.因为该反应△H<0,反应的反应物总能量小于生成物总能量 |
| B.若反应开始时加入催化剂,则使E1、E2 都减小 |
| C.正反应的活化能是368 kJ/mol |
| D.1molNO2与1molCO混合经充分反应放热234kJ |
您最近一年使用:0次



