名校
解题方法
1 . 下列实验方案或装置能达到目的的是
| 选项 | 目的 | 实验方案或装置 |
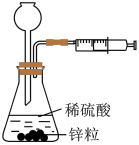
| A | 定量测量化学反应速率 |
|
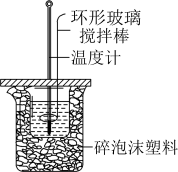
| B | 测定酸碱中和热 |
|
| C | 探究浓度影响化学平衡移动的因素 | 水煤气的反应C(s)+H2O(g) CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。 CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。 |
| D | 探究浓度对反应速率的影响 | 分别向两支盛有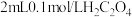 溶液的试管中分别加入 溶液的试管中分别加入 和 和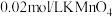 溶液,比较溶液褪色快慢 溶液,比较溶液褪色快慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示。已知v(A)、v(B)、v(C)之间有以下关系:2v(B)=3v(A)、3v(C)=2v(B),则此反应可表示为
| A.2A+3B=2C | B.3A+B=2C | C.A+3B=2C | D.A+B=C |
您最近一年使用:0次
名校
解题方法
3 . 某反应物的浓度是1.0mol/L,经过20s后,它的浓度变成了0.2mol/L,在这20s内它的化学反应速率为
| A.0.01mol/(L·s) | B.0.04mol/(L·s) | C.0.08mol/(L·s) | D.0.05mol/(L·s) |
您最近一年使用:0次
2024-04-05更新
|
468次组卷
|
2卷引用:宁夏石嘴山市平罗中学2023-2024学年高二下学期4月月考化学试题
4 . 2007年10月24日我国自主研发的第一颗月球探测卫星“嫦娥一号”的成功发射“嫦娥一号”三级火箭所用的燃料是高性能、高纯度的液氢燃料和液氧氧化剂,氢气不仅是一种高能燃料,也是一种可再生的绿色能源。
(1)氢气的燃烧热为285.8kJ/mol,写出其燃烧热的热化学方程式:_______ 。
(2)实验测得1mol 与1mol
与1mol 完全反应放出184.6kJ的热量,又知1mol
完全反应放出184.6kJ的热量,又知1mol 分子中化学键断裂时需要吸收436kJ的能量,1mol
分子中化学键断裂时需要吸收436kJ的能量,1mol 分子中化学键断裂需要吸收243kJ的能量。则1molHCl分子中化学键断裂时需要吸收
分子中化学键断裂需要吸收243kJ的能量。则1molHCl分子中化学键断裂时需要吸收_______ 的能量。
(3) 可转化为甲醇:
可转化为甲醇:
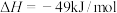

①在一恒温恒容密闭容器中充入1mol 和3mol
和3mol 进行上述反应。测得
进行上述反应。测得 和
和 浓度随时间变化如图所示。问答:0~10min内,氢气的平均反应速率为
浓度随时间变化如图所示。问答:0~10min内,氢气的平均反应速率为_______ ; 的转化率为
的转化率为_______ 。
②拟据下列v-t图象,填写下列空白:

下列时刻所改变的外界条件是
_______ ;
_______ ;
_______ ;反应速率最快的时间段为_______ 。
(1)氢气的燃烧热为285.8kJ/mol,写出其燃烧热的热化学方程式:
(2)实验测得1mol
 与1mol
与1mol 完全反应放出184.6kJ的热量,又知1mol
完全反应放出184.6kJ的热量,又知1mol 分子中化学键断裂时需要吸收436kJ的能量,1mol
分子中化学键断裂时需要吸收436kJ的能量,1mol 分子中化学键断裂需要吸收243kJ的能量。则1molHCl分子中化学键断裂时需要吸收
分子中化学键断裂需要吸收243kJ的能量。则1molHCl分子中化学键断裂时需要吸收(3)
 可转化为甲醇:
可转化为甲醇:
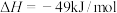

①在一恒温恒容密闭容器中充入1mol
 和3mol
和3mol 进行上述反应。测得
进行上述反应。测得 和
和 浓度随时间变化如图所示。问答:0~10min内,氢气的平均反应速率为
浓度随时间变化如图所示。问答:0~10min内,氢气的平均反应速率为 的转化率为
的转化率为②拟据下列v-t图象,填写下列空白:

下列时刻所改变的外界条件是



您最近一年使用:0次
名校
解题方法
5 . CH3OH也可由CO2和H2合成。在体积为1L的密闭容器中,充入lmolCO2和3molH2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:___________ mol/(L·min)。
(2)10min时,CH3OH的物质的量为___________ mol,10min内,以H2表示的化学反应速率是___________ mol/(L·min)。
(3)到达平衡时,CO2的转化率为___________ 。
(4)3min时,v(正)___________ v(逆)(填“大于”、“等于”、“小于”),此时化学反应朝___________ 进行(填“正方向”或“逆方向”)。
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:
(2)10min时,CH3OH的物质的量为
(3)到达平衡时,CO2的转化率为
(4)3min时,v(正)
您最近一年使用:0次
2024-02-25更新
|
703次组卷
|
2卷引用:宁夏石嘴山市平罗中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
6 . 对于反应3A(g)+B(s) 2C(g)+2D(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是
2C(g)+2D(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是
 2C(g)+2D(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是
2C(g)+2D(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是| A.v(A)=0.1mol·(L·s)-1 | B.v(B)=6mol·(L·min)-1 |
| C.v(C)=8mol·(L·min)-1 | D.v(D)=4mol·(L·min)-1 |
您最近一年使用:0次
2024-02-24更新
|
636次组卷
|
5卷引用:宁夏石嘴山市平罗中学2023-2024学年高二下学期4月月考化学试题
名校
7 . 重要的化工原料丁烯(C4H8)可由丁烷(C4H10)催化脱氢制备,反应如下:
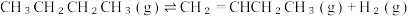 △H
△H
已知:i.该工艺过程的副产物有炭(C),生成的积炭会附着在催化剂表面,影响催化效果。
ii.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
iii.CH2=CHCH2CH3(g)+6O2 (g)=4CO2 (g)+4H2O(l) △H1
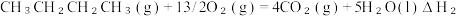
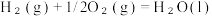 △H3
△H3
(1)用△H1、△H2、△H3表示丁烷催化脱氢反应的反应热△H=_______ 。
(2)寻找高效的催化剂是脱氢反应重要的研究课题之一、
①催化剂使用 段时间后活性会下降,通入适量氢气可使其改善,氢气的作用是_______ 。
②其他条件相同时,以SiO₂为载体与不同质量百分比的CrOx组合,催化效果相关数据如表。
下列说法正确的是_______ (填序号)。[收率=(生成某产物的原料量/投入的原料量)×100%]
a.脱氢反应中SiO2不起催化作用 b. CrOx的含量越高,反应的催化效果越好
c. CrOx的含量对丁烷脱氢反应的焓变有影响 d. 正丁烯收率越高,则原料的利用率越高
(3)其他条件相同,30min时测得正丁烷转化率、正丁烯收率随温度的变化如图1。
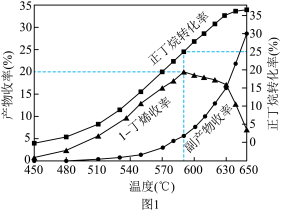
① 实际生产温度选择590℃, 由图1说明其理由是_______ 。
②590℃时,向体积为 1L 的密闭容器中充入3mol正丁烷气体,据图1计算0~30min内生成正丁烯的平均反应速率为_______ mol/(L·min)。
(4)利用电解装置可以将尾气中的 NO 转化为尿素[CO(NH2) 2,其中碳的化合价为+4 价,属于非电解质],工作原理如图2所示。
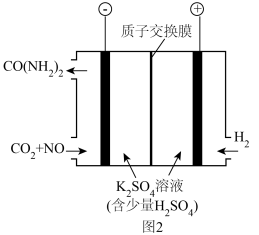
①阴极的电极反应式为_______ 。
②反应 段时间后,阳极区的pH基本不变,结合化学用语解释原因为_______ 。
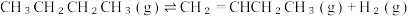 △H
△H已知:i.该工艺过程的副产物有炭(C),生成的积炭会附着在催化剂表面,影响催化效果。
ii.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
iii.CH2=CHCH2CH3(g)+6O2 (g)=4CO2 (g)+4H2O(l) △H1
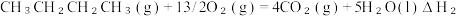
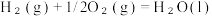 △H3
△H3(1)用△H1、△H2、△H3表示丁烷催化脱氢反应的反应热△H=
(2)寻找高效的催化剂是脱氢反应重要的研究课题之一、
①催化剂使用 段时间后活性会下降,通入适量氢气可使其改善,氢气的作用是
②其他条件相同时,以SiO₂为载体与不同质量百分比的CrOx组合,催化效果相关数据如表。
| 实验组 | 催化剂组成 | 正丁烷转化率 /% | 正丁烯收率 /% |
| 1 | 无催化剂 | 5 | 0.35 |
| 2 | SiO2 | 5 | 0.35 |
| 3 | SiO2+9%CrOx | 25.5 | 18.3 |
| 4 | SiO2+15% CrOx | 27.5 | 20.65 |
| 5 | SiO2+21%CrOx | 24 | 17.87 |
a.脱氢反应中SiO2不起催化作用 b. CrOx的含量越高,反应的催化效果越好
c. CrOx的含量对丁烷脱氢反应的焓变有影响 d. 正丁烯收率越高,则原料的利用率越高
(3)其他条件相同,30min时测得正丁烷转化率、正丁烯收率随温度的变化如图1。

① 实际生产温度选择590℃, 由图1说明其理由是
②590℃时,向体积为 1L 的密闭容器中充入3mol正丁烷气体,据图1计算0~30min内生成正丁烯的平均反应速率为
(4)利用电解装置可以将尾气中的 NO 转化为尿素[CO(NH2) 2,其中碳的化合价为+4 价,属于非电解质],工作原理如图2所示。

①阴极的电极反应式为
②反应 段时间后,阳极区的pH基本不变,结合化学用语解释原因为
您最近一年使用:0次
名校
解题方法
8 . 反应2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0,分别向1L的密闭容器中通入3molNO和一定量的CO,在不同温度下NO的平衡转化率与投料比的关系如图所示。下列说法错误的是
N2(g)+2CO2(g) ΔH<0,分别向1L的密闭容器中通入3molNO和一定量的CO,在不同温度下NO的平衡转化率与投料比的关系如图所示。下列说法错误的是
 N2(g)+2CO2(g) ΔH<0,分别向1L的密闭容器中通入3molNO和一定量的CO,在不同温度下NO的平衡转化率与投料比的关系如图所示。下列说法错误的是
N2(g)+2CO2(g) ΔH<0,分别向1L的密闭容器中通入3molNO和一定量的CO,在不同温度下NO的平衡转化率与投料比的关系如图所示。下列说法错误的是
| A.T1温度下,反应开始至B点用时2min,N2的平均反应速率为0.9mol/(L·min) |
| B.T1温度下,A 点容器内的压强是反应开始时的0.8倍 |
| C.当容器内气体的平均相对分子质量不变时,说明反应达到平衡状态 |
| D.T1>T2 |
您最近一年使用:0次
2024-01-06更新
|
132次组卷
|
3卷引用:宁夏石嘴山市第三中学2023-2024学年高三上学期第四次月考理科综合试卷
名校
解题方法
9 . 把0.6 mol X气体和0.4 mol Y气体混合于容积为2 L的容器中,使其发生如下反应:
 。2 min末生成0.2 molW,若测知以Z浓度变化表示的平均反应速率为0.1 mol/(L·min),则n的值为
。2 min末生成0.2 molW,若测知以Z浓度变化表示的平均反应速率为0.1 mol/(L·min),则n的值为

 。2 min末生成0.2 molW,若测知以Z浓度变化表示的平均反应速率为0.1 mol/(L·min),则n的值为
。2 min末生成0.2 molW,若测知以Z浓度变化表示的平均反应速率为0.1 mol/(L·min),则n的值为| A.4 | B.3 | C.2 | D.1 |
您最近一年使用:0次
2023-12-30更新
|
182次组卷
|
4卷引用:宁夏石嘴山市平罗中学2023-2024学年高二下学期4月月考化学试题
名校
10 . 氮及其化合物在工农业生产、生活中有着重要作用,以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2L的密闭容器中加入0.2mol的 和0.6mol的
和0.6mol的 在一定条件下发生反应:
在一定条件下发生反应:
 ,若在5min时反应达到平衡,此时测得
,若在5min时反应达到平衡,此时测得 的物质的量为0.2mol,则前5min平均反应速率
的物质的量为0.2mol,则前5min平均反应速率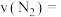
________ 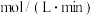 ,平衡时
,平衡时 的转化率为
的转化率为________ %。
(2)平衡后,若提高 的转化率,可以采取的措施有________(填字母序号)。
的转化率,可以采取的措施有________(填字母序号)。
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:
 ,其化学平衡常数K与温度T的关系如表所示:
,其化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
①试比较 、
、 的大小,
的大小,
________  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
②400℃时,反应 的化学平衡常数为
的化学平衡常数为________ 。当测得 、
、 和
和 物质的量分别为3mol、2mol和1mol时,则该反应的
物质的量分别为3mol、2mol和1mol时,则该反应的
________  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
③下列可用于判断 反应达到平衡状态的依据是
反应达到平衡状态的依据是________ (填字母序号)。
A.容器中气体压强不再变化 B.容器中气体的密度不再变化
C.容器中气体平均摩尔质量不再变化 D.
(1)若在一容积为2L的密闭容器中加入0.2mol的
 和0.6mol的
和0.6mol的 在一定条件下发生反应:
在一定条件下发生反应:
 ,若在5min时反应达到平衡,此时测得
,若在5min时反应达到平衡,此时测得 的物质的量为0.2mol,则前5min平均反应速率
的物质的量为0.2mol,则前5min平均反应速率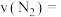
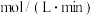 ,平衡时
,平衡时 的转化率为
的转化率为(2)平衡后,若提高
 的转化率,可以采取的措施有________(填字母序号)。
的转化率,可以采取的措施有________(填字母序号)。| A.加入催化剂 | B.增大容器体积 |
| C.降低反应体系的温度 | D.通入一定量He |

 ,其化学平衡常数K与温度T的关系如表所示:
,其化学平衡常数K与温度T的关系如表所示:T/℃ | 200 | 300 | 400 |
K |
|
| 0.5 |
①试比较
 、
、 的大小,
的大小,
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。②400℃时,反应
 的化学平衡常数为
的化学平衡常数为 、
、 和
和 物质的量分别为3mol、2mol和1mol时,则该反应的
物质的量分别为3mol、2mol和1mol时,则该反应的
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。③下列可用于判断
 反应达到平衡状态的依据是
反应达到平衡状态的依据是A.容器中气体压强不再变化 B.容器中气体的密度不再变化
C.容器中气体平均摩尔质量不再变化 D.

您最近一年使用:0次