1 . 某温度下,在2L密闭容器中投入6molA、4molB发生反应:3A(g)+B(g) 2C(g),C的物质的量随时间变化的曲线如图所示。
2C(g),C的物质的量随时间变化的曲线如图所示。

(1)从反应开始到2min末,用C表示的反应速率为________ ,用B表示的反应速率为 ________ 。
(2)2min末,A的浓度为________ 。
 2C(g),C的物质的量随时间变化的曲线如图所示。
2C(g),C的物质的量随时间变化的曲线如图所示。
(1)从反应开始到2min末,用C表示的反应速率为
(2)2min末,A的浓度为
您最近一年使用:0次
解题方法
2 . 在容积为1.00L的密闭容器中,通入一定量的N2O4,发生反应:N2O4(g) 2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
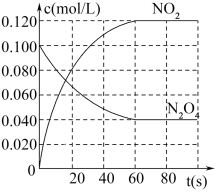
请回答:
(1)60s内,v(N2O4)=___ mol/(L•s)。
(2)若升高温度,混合气体的颜色变深,则正反应是___ (填“放热”或吸热”)反应。
(3)100℃时,该反应的化学平衡常数数值为___ 。
(4)平衡时,N2O4的转化率是___ 。
 2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
请回答:
(1)60s内,v(N2O4)=
(2)若升高温度,混合气体的颜色变深,则正反应是
(3)100℃时,该反应的化学平衡常数数值为
(4)平衡时,N2O4的转化率是
您最近一年使用:0次
2022-09-18更新
|
480次组卷
|
3卷引用:新疆霍城县第二中学2022-2023学年高二上学期(线上)期中考试化学试题
名校
解题方法
3 . 某温度时,在2L恒容密闭容器中X、Y、Z三种气体的物质的量随时间的变化关系如图所示。

(1)由图中的数据分析可知,该反应的化学方程式为_______ 。
(2)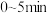 内Z的平均反应速率为
内Z的平均反应速率为_______ 。
(3)已知TiO2(s)+2C(s)+2Cl2(g)⇌TiCl4(g)+2CO(g)。若反应容器的容积为2L,4min后,测得固体的质量减少了10.4g,则Cl2的平均反应速率为_______ mol/(L·min)。(Ti的相对原子质量48)

(1)由图中的数据分析可知,该反应的化学方程式为
(2)
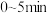 内Z的平均反应速率为
内Z的平均反应速率为(3)已知TiO2(s)+2C(s)+2Cl2(g)⇌TiCl4(g)+2CO(g)。若反应容器的容积为2L,4min后,测得固体的质量减少了10.4g,则Cl2的平均反应速率为
您最近一年使用:0次
4 . I.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
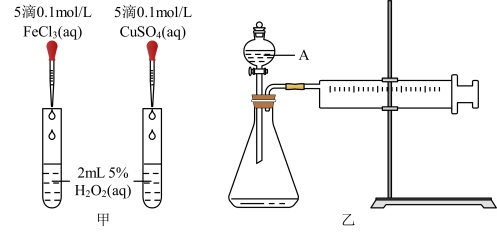
(1)定性分析:如图甲可通过观察__________ 的快慢,定性比较得出结论。有同学提出将FeCl3改为0. 05mol·L-1 Fe2 (SO4)3更为合理,其理由是____________ 。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是________ 。
II.某温度时,在一个2L的密闭容器中, A、B、C三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(3)该反应的化学方程式为________ ;
(4)从开始至2min,A的平均反应速率为________ ;

(1)定性分析:如图甲可通过观察
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是
II.某温度时,在一个2L的密闭容器中, A、B、C三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(3)该反应的化学方程式为
(4)从开始至2min,A的平均反应速率为
您最近一年使用:0次
名校
解题方法
5 . 某温度时,在0.5L密闭容器中,某一可逆反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析可得:

(1)该可逆反应的化学方程式为_______ 。
(2)若降低温度,则该反应的正反应速率_______ (填“加快”“减慢”或“不变”,下同), 若缩小体积加压,正反应速率_______ 。
(3)第8min时,正、逆反应速率的大小关系为v正_______ (填“>” “<”或“=”)v逆。
(4)0~4 min内,用B的浓度变化来表示该反应的平均反应速率为_______ mol·L-1·min-1
(5)能判断该反应在一定温 度下达到化学平衡状态的依据是_______。
(6)平衡时A的转化率(反应中已消耗A的物质的量占反应起始时A物质的量的百分数)为_______ 。

(1)该可逆反应的化学方程式为
(2)若降低温度,则该反应的正反应速率
(3)第8min时,正、逆反应速率的大小关系为v正
(4)0~4 min内,用B的浓度变化来表示该反应的平均反应速率为
(5)能判断该反应在一定温 度下达到化学平衡状态的依据是_______。
| A.容器各组分浓度不变 |
| B.混合气体中A的物质的量不再改变 |
| C.容器中反应体系温度不再改变 |
| D.c(A)=c(B) |
您最近一年使用:0次
2022-05-08更新
|
451次组卷
|
2卷引用:新疆乌苏市第一中学2021-2022学年高一下学期期中考试化学试题(加强班)
解题方法
6 . 一定条件下,在2L密闭容器中发生反应:3A(g)+B(g) 2C(g)。开始时加入4molA、6molB、2molC,2min末测得C的物质的量是3mol。
2C(g)。开始时加入4molA、6molB、2molC,2min末测得C的物质的量是3mol。
(1)用A的浓度变化表示反应的平均速率___ 。
(2)在2min末B的浓度为___ ?
 2C(g)。开始时加入4molA、6molB、2molC,2min末测得C的物质的量是3mol。
2C(g)。开始时加入4molA、6molB、2molC,2min末测得C的物质的量是3mol。(1)用A的浓度变化表示反应的平均速率
(2)在2min末B的浓度为
您最近一年使用:0次
2021-05-08更新
|
142次组卷
|
2卷引用:新疆巴楚县第一中学2021-2022学年高一下学期期中考试化学试题
7 . 某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量n(mol)随时间t(min)变化的曲线如图所示。
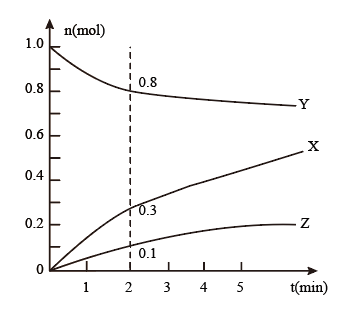
(1)由图中数据分析:该反应的化学方程式为_________ 。
(2)反应开始至2min,用Z表示的平均反应速率为______ 。用X表示的平均反应速率为______ 。
(3)判断:第5分钟时,反应是否达到平衡?_______ .第5分钟时,Z的生成速率与Z的消耗速率之比_________ 1(填”大于”、“小于”或“相等”)

(1)由图中数据分析:该反应的化学方程式为
(2)反应开始至2min,用Z表示的平均反应速率为
(3)判断:第5分钟时,反应是否达到平衡?
您最近一年使用:0次
2021-04-29更新
|
184次组卷
|
2卷引用:新疆柯坪县柯坪湖州国庆中学2021-2022学年高一下学期期中考试化学试题
8 . 恒温恒容下,将2molA气体和2molB气体通入体积为2L的密闭容器中发生如下反应:2A(g)+B(g) xC(g)+2D(s),2min时反应达到平衡状态。此时剩余1.2molB,并测得C的浓度为1.2mol•L-1。
xC(g)+2D(s),2min时反应达到平衡状态。此时剩余1.2molB,并测得C的浓度为1.2mol•L-1。
(1)A的转化率与B的转化率之比为___ ;物质A的化学反应速率为___ ;x=___ ;
(2)保持温度和容积不变,向平衡体系中再充入2molA和2molB气体,达到新平衡时B的物质的量为___ 。
(3)此反应在该温度时的化学平衡常数为___ 。
 xC(g)+2D(s),2min时反应达到平衡状态。此时剩余1.2molB,并测得C的浓度为1.2mol•L-1。
xC(g)+2D(s),2min时反应达到平衡状态。此时剩余1.2molB,并测得C的浓度为1.2mol•L-1。(1)A的转化率与B的转化率之比为
(2)保持温度和容积不变,向平衡体系中再充入2molA和2molB气体,达到新平衡时B的物质的量为
(3)此反应在该温度时的化学平衡常数为
您最近一年使用:0次
名校
解题方法
9 . 向2L密闭容器中通入amol气体A和bmol气体B,在一定条件下发生反应:xA(g)+yB(g) pC(g)+qD(g)。已知:平均反应速率v(C)=
pC(g)+qD(g)。已知:平均反应速率v(C)= v(A);反应2min时,A的物质的量减少
v(A);反应2min时,A的物质的量减少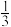 amol,B的物质的量减少
amol,B的物质的量减少 mol,有amolD生成。回答下列问题:
mol,有amolD生成。回答下列问题:
(1)反应2min内,v(B)=______ 。
(2)化学方程式中,x=______ ,q=______ 。
(3)反应平衡时,D为2amol,则B的转化率为______ 。
 pC(g)+qD(g)。已知:平均反应速率v(C)=
pC(g)+qD(g)。已知:平均反应速率v(C)= v(A);反应2min时,A的物质的量减少
v(A);反应2min时,A的物质的量减少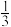 amol,B的物质的量减少
amol,B的物质的量减少 mol,有amolD生成。回答下列问题:
mol,有amolD生成。回答下列问题:(1)反应2min内,v(B)=
(2)化学方程式中,x=
(3)反应平衡时,D为2amol,则B的转化率为
您最近一年使用:0次
2021-03-03更新
|
444次组卷
|
4卷引用:新疆疏勒县第一中学2020--2021学年高二下学期期末考试化学试题
新疆疏勒县第一中学2020--2021学年高二下学期期末考试化学试题湖北省武汉市外国语学校2019-2020学年高一下学期期中考试化学试题河北省张家口市宣化第一中学2020-2021学年高一下学期期中考试化学试题(已下线)6.2.2 化学反应的限度-2021-2022学年高一化学课后培优练(人教版2019必修第二册)
10 . 某温度时,在0.5L密闭容器中,某一可逆反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析可得:

(1)该反应的化学方程式为_________________ 。
(2)若降低温度,则该反应的正反应速率_________ (填“加快”“减慢”或“不变”,下同),逆反应速率_______ 。
(3)第4min时,正、逆反应速率的大小关系为
_________ (填”>””<”或”=”) 。
。
(4)0~4min内,用B的浓度变化来表示该反应的平均反应速率为________  。
。
(5)能判断该反应在一定温度下达到化学平衡状态的依据是__________ 。
A.容器中压强不变 B.混合气体中A的浓度不再改变 C.容器中气体密度不变 D.
(6)平衡时A的转化率为__________ 。
(7)平衡时混合气体中B的体积分数约为______________ 。
(8)反应达到平衡,此时体系内压强与开始时的压强之比为__________ 。

(1)该反应的化学方程式为
(2)若降低温度,则该反应的正反应速率
(3)第4min时,正、逆反应速率的大小关系为

 。
。(4)0~4min内,用B的浓度变化来表示该反应的平均反应速率为
 。
。(5)能判断该反应在一定温度下达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中A的浓度不再改变 C.容器中气体密度不变 D.

(6)平衡时A的转化率为
(7)平衡时混合气体中B的体积分数约为
(8)反应达到平衡,此时体系内压强与开始时的压强之比为
您最近一年使用:0次



