1 . 一定温度下,在10L密闭容器中加入5molSO2和3molO2,发生反应:2SO2(g)+O2(g) 2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。
2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。
(1)反应生成了____ molSO3,v(SO2)=____ 。
(2)平衡时SO3的浓度是____ ,SO2的转化率是____ 。
(3)平衡时容器内气体的总物质的量为___ mol。
(4)物质的浓度不再改变标志着该反应已达平衡,下列还可以说明该反应已达平衡的是___ (填序号)。
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2)
⑤n(SO3):n(O2):n(SO2)=2:1:2
(5)该温度下,SO3(g) SO2(g)+
SO2(g)+ O2(g)的平衡常数K=
O2(g)的平衡常数K=___ 。
 2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。
2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。(1)反应生成了
(2)平衡时SO3的浓度是
(3)平衡时容器内气体的总物质的量为
(4)物质的浓度不再改变标志着该反应已达平衡,下列还可以说明该反应已达平衡的是
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2)
⑤n(SO3):n(O2):n(SO2)=2:1:2
(5)该温度下,SO3(g)
 SO2(g)+
SO2(g)+ O2(g)的平衡常数K=
O2(g)的平衡常数K=
您最近一年使用:0次
2022-04-11更新
|
532次组卷
|
2卷引用:贵州省黔西南州金成实验学校2022-2023学年高二上学期9月月考化学试题
解题方法
2 . 为了更好地利用化学反应中物质和能量的变化,在化学研究和工业生产中还需要关注化学反应的快慢和限度。能量、速率与限度是认识和研究化学反应的重要因素。
Ⅰ.某温度下,在2 L的恒容密闭容器中,A、B、C(均为气体)三种物质的物质的量随时间的变化曲线如图所示。

(1)该反应的化学方程式为___________ 。
(2)能说明此时反应已达到了平衡状态的是___________ (填标号)。
a.A、B、C三种物质的浓度保持不变
b.气体A的消耗速率等于气体C的生成速率
c.混合气体的密度不变
d.总压强不变
Ⅱ.某温度下,向2.0 L的恒容密闭容器中充入2.0 molN2和2.0 molH2,发生反应,一段时间后反应达到平衡状态,实验数据如下表所示:
(3)0~50 s内的平均反应速率v(N2)=___________  。
。
(4)键能指在标准状况下,将1 mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为 ,已知N≡N键的键能为946 kJ/mol,H-H键的键能为436 kJ/mol,N-H键的键能为391 kJ/mol。则生成1 mol NH3的过程中
,已知N≡N键的键能为946 kJ/mol,H-H键的键能为436 kJ/mol,N-H键的键能为391 kJ/mol。则生成1 mol NH3的过程中___________ (填“吸收”或“放出”)的能量为___________  。
。
(5)为加快反应速率,可采取的措施是___________ (填标号)。
a.升高温度 b.增大容器体积 c.恒容时充入He d.加入合适催化剂
Ⅰ.某温度下,在2 L的恒容密闭容器中,A、B、C(均为气体)三种物质的物质的量随时间的变化曲线如图所示。

(1)该反应的化学方程式为
(2)能说明此时反应已达到了平衡状态的是
a.A、B、C三种物质的浓度保持不变
b.气体A的消耗速率等于气体C的生成速率
c.混合气体的密度不变
d.总压强不变
Ⅱ.某温度下,向2.0 L的恒容密闭容器中充入2.0 molN2和2.0 molH2,发生反应,一段时间后反应达到平衡状态,实验数据如下表所示:
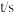 | 0 | 50 | 150 | 250 | 350 |
| n(NH3)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
 。
。(4)键能指在标准状况下,将1 mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为
 ,已知N≡N键的键能为946 kJ/mol,H-H键的键能为436 kJ/mol,N-H键的键能为391 kJ/mol。则生成1 mol NH3的过程中
,已知N≡N键的键能为946 kJ/mol,H-H键的键能为436 kJ/mol,N-H键的键能为391 kJ/mol。则生成1 mol NH3的过程中 。
。(5)为加快反应速率,可采取的措施是
a.升高温度 b.增大容器体积 c.恒容时充入He d.加入合适催化剂
您最近一年使用:0次
解题方法
3 . 某温度下,在一个体积为2L的固定不变的密闭容器中充入2molSO2和1molO2,发生2SO2(g)+O2(g) 2SO3(g)反应。5min后反应达到化学平衡状态,平衡时测得容器中混合气体为2.4mol。求:
2SO3(g)反应。5min后反应达到化学平衡状态,平衡时测得容器中混合气体为2.4mol。求:
(1)以SO3的浓度变化表示该反应的化学反应速率为________
(2)该反应中SO2的平衡转化率为________
(3)该反应的平衡常数K值为________
 2SO3(g)反应。5min后反应达到化学平衡状态,平衡时测得容器中混合气体为2.4mol。求:
2SO3(g)反应。5min后反应达到化学平衡状态,平衡时测得容器中混合气体为2.4mol。求:(1)以SO3的浓度变化表示该反应的化学反应速率为
(2)该反应中SO2的平衡转化率为
(3)该反应的平衡常数K值为
您最近一年使用:0次
2020-11-09更新
|
153次组卷
|
3卷引用:贵州省龙里县九八五实验学校2020-2021学年高二上学期1月月考化学试题
4 . 某温度时,在2 L密闭容器中,X、Y、Z三种物质的物质的量n(mol)随时间t(min)变化的曲线如图所示。由图中数据分析:
(1)该反应的化学方程式__________ ;
(2)反应开始至2 min末Z的反应速率为________ ,X的转化率为________ 。

(1)该反应的化学方程式
(2)反应开始至2 min末Z的反应速率为
您最近一年使用:0次
2020-10-16更新
|
193次组卷
|
2卷引用:贵州省毕节市实验高级中学2020-2021学年高二上学期第一次月考化学试题
名校
解题方法
5 . 400℃时,将一定量的SO2和14molO2压入一个盛有催化剂的10L密闭容器中进行反应:2SO2+O2⇌2SO3。已知2min时,容器中剩余2molSO2和12molO2。试计算:
(1)SO2的起始物质的量浓度__________________ 。
(2)2min内SO3的反应速率____________________ 。
(1)SO2的起始物质的量浓度
(2)2min内SO3的反应速率
您最近一年使用:0次
2020-07-13更新
|
153次组卷
|
2卷引用:贵州省思南中学2019-2020学年高一下学期期末考试化学试题
名校
解题方法
6 . 将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g) ⇌xC(g)+2D(g),5 min后测得c(D)=0.5 mol/L,c(A):c(B)=1:2,C的反应速率是0.15 mol/(L·min)。
(1)B的反应速率v(B)=___ ,x=___ 。
(2)A在5 min末的浓度是_______ 。
(3)此时容器内的压强与开始时之比为:___ 。
(1)B的反应速率v(B)=
(2)A在5 min末的浓度是
(3)此时容器内的压强与开始时之比为:
您最近一年使用:0次
2020-06-04更新
|
496次组卷
|
5卷引用:贵州省贵阳市第三实验中学2019-2020学年高二上学期第一次月考化学试题
贵州省贵阳市第三实验中学2019-2020学年高二上学期第一次月考化学试题河北省石家庄市辛集市第二中学2019-2020学年高一下学期期末考试化学试题(已下线)第02章 化学反应速率和化学平衡(B卷提升篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)(已下线)第二章 化学反应速率和化学平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)甘肃省兰州市教育局第四片区2020-2021学年高一下学期期中考试化学试题
名校
解题方法
7 . 如图是:600℃ 时,在2L密闭容器里A、B、C三种气体在密闭容器中反应时浓度的变化,其中A为有色气体,B、C是无色气体。请从图中分析并填空:

(1)该反应的化学反应方程式为_____
(2)反应达到平衡状态时,反应物的转化率为_____
(3)当反应进行到第_____ min,该反应达到平衡。
(4)反应从开始至2分钟末,B的物质的量_____ ,用B的浓度变化表示的平均反应速率为v(B)=_
(5)下列描述能表示反应达平衡状态的是_____ (填选项)。
a.容器中A与B的物质的量相等
b.容器内气体的颜色不再改变
c.各物质的浓度保持不变

(1)该反应的化学反应方程式为
(2)反应达到平衡状态时,反应物的转化率为
(3)当反应进行到第
(4)反应从开始至2分钟末,B的物质的量
(5)下列描述能表示反应达平衡状态的是
a.容器中A与B的物质的量相等
b.容器内气体的颜色不再改变
c.各物质的浓度保持不变
您最近一年使用:0次
2020-04-15更新
|
282次组卷
|
3卷引用:贵州省铜仁市伟才学校2019-2020学年高一下学期期中考试化学试题
解题方法
8 . 汽车尾气无害化处理反应为2NO(g)+2CO(g) N2(g)+2CO2(g)。在催化剂作用下向体积不变的2L密闭容器中充入4molNO和2molCO,5min达到化学平衡状态,生成0.6molN2。
N2(g)+2CO2(g)。在催化剂作用下向体积不变的2L密闭容器中充入4molNO和2molCO,5min达到化学平衡状态,生成0.6molN2。
(1)用CO表示这段时间的反应速率___ 。
(2)求NO的转化率___ 。
 N2(g)+2CO2(g)。在催化剂作用下向体积不变的2L密闭容器中充入4molNO和2molCO,5min达到化学平衡状态,生成0.6molN2。
N2(g)+2CO2(g)。在催化剂作用下向体积不变的2L密闭容器中充入4molNO和2molCO,5min达到化学平衡状态,生成0.6molN2。(1)用CO表示这段时间的反应速率
(2)求NO的转化率
您最近一年使用:0次
名校
9 . 将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5求:
xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5求:
(1)此时A的浓度为______ ;
(2)反应开始前放入容器中A、B的物质的量是_____________ ;
(3)B的平均反应速率是_________________ ;
(4)x值为____________ 。
 xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5求:
xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5求: (1)此时A的浓度为
(2)反应开始前放入容器中A、B的物质的量是
(3)B的平均反应速率是
(4)x值为
您最近一年使用:0次
2019-06-28更新
|
298次组卷
|
5卷引用:贵州省毕节市实验高级中学2019-2020学年高一下学期期中考试化学试题
10 . 研究化学反应时,既要考虑物质变化与能量变化,也要关注反应的快慢与限度。回答下列问题:
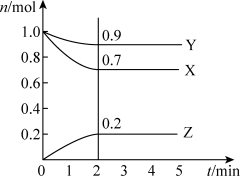
(1)某温度时,在2 L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:(A、B均为气体)
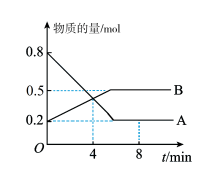
①该反应的化学方程式为____________________ ;
②反应开始至4 min时,B的平均反应速率为________ ;
③4 min时,反应是否达到平衡状态?________ (填“是”或“否”),8 min时,v(正)________ v(逆)(填“>”、“<”或“=”)。
(2)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
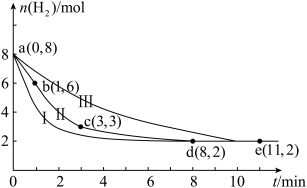
①a—b,b—c,c—d,d—e四段中,平均反应速率最大的时间段是___________ ,该时间段内CO2的平均反应速率是________ 。
②若在反应中加入了催化剂,则反应过程将变为图中的曲线_____ (填“Ⅰ”或“Ⅱ”或“Ⅲ”)。
③平衡时CO2的转化率是_________ ;反应前后容器内的压强比是__________ 。
(1)某温度时,在2 L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:(A、B均为气体)

①该反应的化学方程式为
②反应开始至4 min时,B的平均反应速率为
③4 min时,反应是否达到平衡状态?
(2)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
①a—b,b—c,c—d,d—e四段中,平均反应速率最大的时间段是
②若在反应中加入了催化剂,则反应过程将变为图中的曲线
③平衡时CO2的转化率是
您最近一年使用:0次
2019-05-14更新
|
441次组卷
|
4卷引用:贵州省黔西南州赛文高级中学 2021-2022学年高二上学期期中考试化学试题



