1 . 某小组利用不同膜反应器(可选择性地让某些气体通过而离开体系)研究HI的分解率,工作原理如图所示。图a、b和c反应区温度维持恒定且相等,仅发生反应 且在反应区内进行。投料均为1mol的
且在反应区内进行。投料均为1mol的 ,反应同时开始,80s时图b反应区处于瞬时平衡状态,其化学平衡常数
,反应同时开始,80s时图b反应区处于瞬时平衡状态,其化学平衡常数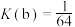 。
。
下列说法正确的是
 且在反应区内进行。投料均为1mol的
且在反应区内进行。投料均为1mol的 ,反应同时开始,80s时图b反应区处于瞬时平衡状态,其化学平衡常数
,反应同时开始,80s时图b反应区处于瞬时平衡状态,其化学平衡常数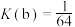 。
。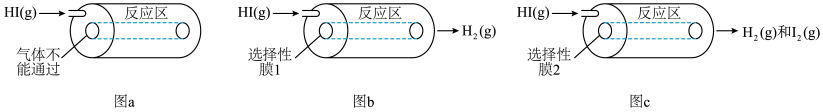
| 图a装置 | 图b装置 | 图c装置 | |
80s时反应区 的物质的量/mol 的物质的量/mol | 0.10 | 0.30 | x |
A.图a装置的化学平衡常数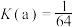 |
B.图a装置中,80s时 分解率为10% 分解率为10% |
| C.图c装置中,x一定大于0.3 |
D.图b装置中,前80s内 的平均渗透速率约为 的平均渗透速率约为 mol·s mol·s |
您最近一年使用:0次
解题方法
2 . 体积均为2L的多个恒容密闭容器,分别充入1mol CO(g)和1mol  (g)发生反应
(g)发生反应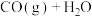

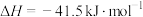 ,在不同温度下反应50s,测得正、逆反应的平衡常数的自然对数
,在不同温度下反应50s,测得正、逆反应的平衡常数的自然对数 (
( 或
或 )、
)、 体积分数与热力学温度的倒数关系如图所示,下列说法错误的是
体积分数与热力学温度的倒数关系如图所示,下列说法错误的是
 (g)发生反应
(g)发生反应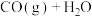

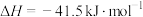 ,在不同温度下反应50s,测得正、逆反应的平衡常数的自然对数
,在不同温度下反应50s,测得正、逆反应的平衡常数的自然对数 (
( 或
或 )、
)、 体积分数与热力学温度的倒数关系如图所示,下列说法错误的是
体积分数与热力学温度的倒数关系如图所示,下列说法错误的是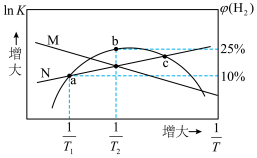
A.曲线N表示 的变化情况 的变化情况 |
B.0~50s,a点对应容器中的反应的平均速率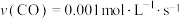 |
| C.b点时一定处于平衡状态 |
D.c点时, |
您最近一年使用:0次
解题方法
3 . 700℃时,向容积为2L的密闭容器中充入一定量的CO(g)和H2O(g),发生反应CO(g)+H2O(g) CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):
下列说法正确的是
 CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A.反应在0~t1min内的平均速率为v(H2)=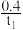 mol·L-1·min-1 mol·L-1·min-1 |
| B.若800℃时该反应的平衡常数为0.64,则逆反应为吸热反应 |
| C.保持其他条件不变,向平衡体系中再通入0.20molH2O(g)和0.40molH2(g),则v正>v逆 |
| D.保持其他条件不变,起始时向容器中充入0.60molCO(g)和1.20molH2O(g),达到平衡时n(CO2)=0.40mol |
您最近一年使用:0次
4 . 丙酮的溴代反应(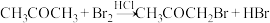 )的速率方程为:
)的速率方程为: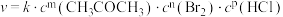 ,其中k为速率常数,与温度有关;“
,其中k为速率常数,与温度有关;“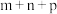 ”为反应级数。某温度时,获得如下实验数据:
”为反应级数。某温度时,获得如下实验数据:
分析该组实验数据所得出的结论错误的是
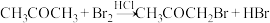 )的速率方程为:
)的速率方程为: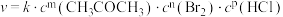 ,其中k为速率常数,与温度有关;“
,其中k为速率常数,与温度有关;“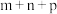 ”为反应级数。某温度时,获得如下实验数据:
”为反应级数。某温度时,获得如下实验数据:| 实验序号 | 初始浓度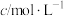 | 溴颜色消失所需时间t/s | ||
 | HCl |  | ||
| ① | 0.80 | 0.20 | 0.0010 | 200 |
| ② | 1.60 | 0.20 | 0.0010 | 100 |
| ③ | 0.80 | 0.40 | 0.0010 | 100 |
| ④ | 0.80 | 0.20 | 0.0020 | 400 |
A.增大 ,能延长溶液颜色消失的时间 ,能延长溶液颜色消失的时间 |
| B.实验②和③的平均速率相等 |
C.实验①在200s内的平均速率 |
| D.反应级数为2 |
您最近一年使用:0次
名校
解题方法
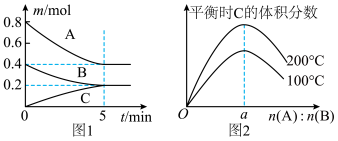
5 . 在体积为 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应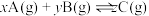 ,图1表示
,图1表示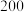 ℃时容器中
℃时容器中 、
、 、
、 物质的量随时间的变化关系,图2表示不同温度下平衡时
物质的量随时间的变化关系,图2表示不同温度下平衡时 的体积分数随起始
的体积分数随起始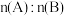 的变化关系。则下列结论正确的是
的变化关系。则下列结论正确的是
 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应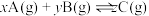 ,图1表示
,图1表示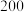 ℃时容器中
℃时容器中 、
、 、
、 物质的量随时间的变化关系,图2表示不同温度下平衡时
物质的量随时间的变化关系,图2表示不同温度下平衡时 的体积分数随起始
的体积分数随起始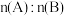 的变化关系。则下列结论正确的是
的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率 |
B.由图2可知反应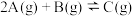 ,正反应吸热且a=2 ,正反应吸热且a=2 |
C.若在图1所示的平衡状态下再向体系中充入 和 和 ,此时 ,此时 |
D.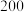 ℃时,向空容器中充入 ℃时,向空容器中充入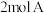 和 和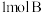 ,达到平衡时 ,达到平衡时 的体积分数小于0.5 的体积分数小于0.5 |
您最近一年使用:0次
2023-04-27更新
|
327次组卷
|
7卷引用:湖南省衡阳县2023届高三3月教学质量诊断性检测考试化学试题
湖南省衡阳县2023届高三3月教学质量诊断性检测考试化学试题上海市实验学校2021-2022学年高三下学期3月月考化学试题(已下线)卷11 化学反应速率和平衡选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省常德市澧县一中2021-2022学年高三下学期期中考试化学试题湖南省常德市澧县第一中学2021-2022学年高三下学期期中考试化学试题上海市建平中学2023届高三下学期3月月考化学试题山西省实验中学2023-2024学年高二上学期第一次月考化学试题
解题方法
6 . 在起始温度均为T℃、容积均为 的密闭容器A(恒温)、B(绝热)中均加入
的密闭容器A(恒温)、B(绝热)中均加入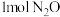 和
和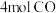 ,发生反应
,发生反应
 。已知:
。已知: 、
、 分别是正、逆反应速率常数,
分别是正、逆反应速率常数,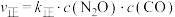 ,
,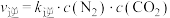 ,A、B容器中
,A、B容器中 的转化率随时间的变化关系如图所示。下列说法错误的是
的转化率随时间的变化关系如图所示。下列说法错误的是

 的密闭容器A(恒温)、B(绝热)中均加入
的密闭容器A(恒温)、B(绝热)中均加入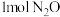 和
和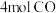 ,发生反应
,发生反应
 。已知:
。已知: 、
、 分别是正、逆反应速率常数,
分别是正、逆反应速率常数,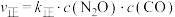 ,
,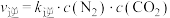 ,A、B容器中
,A、B容器中 的转化率随时间的变化关系如图所示。下列说法错误的是
的转化率随时间的变化关系如图所示。下列说法错误的是
A.曲线M表示B容器中 的转化率随时间的变化 的转化率随时间的变化 |
B.用 的浓度变化表示曲线N在 的浓度变化表示曲线N在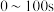 内的反应速率为 内的反应速率为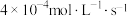 |
C.Q点 大于P点 大于P点 |
D.T℃时, |
您最近一年使用:0次
名校
解题方法
7 . T℃时,含等浓度的 与
与 的混合溶液中发生反应
的混合溶液中发生反应
 ,
, 时刻,改变某一外界条件继续反应至
时刻,改变某一外界条件继续反应至 时刻,溶液中
时刻,溶液中 和
和 随时间的变化关系如图所示。下列说法正确的是
随时间的变化关系如图所示。下列说法正确的是

已知:T℃时,该反应的化学平衡常数K=1。
 与
与 的混合溶液中发生反应
的混合溶液中发生反应
 ,
, 时刻,改变某一外界条件继续反应至
时刻,改变某一外界条件继续反应至 时刻,溶液中
时刻,溶液中 和
和 随时间的变化关系如图所示。下列说法正确的是
随时间的变化关系如图所示。下列说法正确的是
已知:T℃时,该反应的化学平衡常数K=1。
A.若 时刻未改变外界条件,则此时该反应处于平衡状态 时刻未改变外界条件,则此时该反应处于平衡状态 |
B.若 时刻反应达到平衡,则 时刻反应达到平衡,则 时刻改变的条件可能为升温 时刻改变的条件可能为升温 |
C.若始终保持温度不变,则平均反应速率: ( ( 表示0~ 表示0~ s内 s内 的平均反应速率, 的平均反应速率, 表示0~ 表示0~ s内 s内 的平均反应速率) 的平均反应速率) |
D. 内 内 的平均反应速率为 的平均反应速率为 |
您最近一年使用:0次
2023-01-11更新
|
333次组卷
|
3卷引用:湖南省衡阳市2023届高三上学期第一次统一考试(一模)化学试题
8 . 在起始温度均为 、容积均为
、容积均为 的恒容密闭容器A(恒温)、B(绝热)中均加入
的恒容密闭容器A(恒温)、B(绝热)中均加入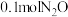 和
和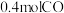 ,发生反应
,发生反应 ,已知:
,已知: 、
、 分别是正、逆反应速率常数,
分别是正、逆反应速率常数, ,
, ,A、B容器中
,A、B容器中 的转化率随时间的变化关系如图所示。下列说法错误的是
的转化率随时间的变化关系如图所示。下列说法错误的是

 、容积均为
、容积均为 的恒容密闭容器A(恒温)、B(绝热)中均加入
的恒容密闭容器A(恒温)、B(绝热)中均加入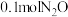 和
和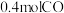 ,发生反应
,发生反应 ,已知:
,已知: 、
、 分别是正、逆反应速率常数,
分别是正、逆反应速率常数, ,
, ,A、B容器中
,A、B容器中 的转化率随时间的变化关系如图所示。下列说法错误的是
的转化率随时间的变化关系如图所示。下列说法错误的是
A.曲线N表示B容器中 的转化率随时间的变化 的转化率随时间的变化 |
B.用 的浓度变化表示曲线N在 的浓度变化表示曲线N在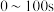 内的反应速率为 内的反应速率为 |
C.Q点 小于P点 小于P点 |
D. 时, 时, |
您最近一年使用:0次
9 . “碳中和”“碳达峰”是我国向全世界做出的郑重承诺。在容积为1L的恒容密闭容器中通入1mol  、4mol
、4mol  的混合气体,发生反应:
的混合气体,发生反应: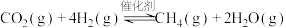
 ,8min时反应刚好达到平衡,测得此时容器内
,8min时反应刚好达到平衡,测得此时容器内 为0.4mol。下列说法正确的是
为0.4mol。下列说法正确的是
 、4mol
、4mol  的混合气体,发生反应:
的混合气体,发生反应: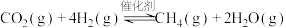
 ,8min时反应刚好达到平衡,测得此时容器内
,8min时反应刚好达到平衡,测得此时容器内 为0.4mol。下列说法正确的是
为0.4mol。下列说法正确的是| A.该反应的逆反应为吸热反应 |
B.升高温度, 的生成速率增大,消耗速率减小 的生成速率增大,消耗速率减小 |
C.0~8min内的平均反应速率 |
D.平衡体系中 (g)的物质的量分数为 (g)的物质的量分数为 |
您最近一年使用:0次
名校
10 . 一定条件下, 密闭容器中投入少量的粗镍和
密闭容器中投入少量的粗镍和 气体(假设固体杂质不和
气体(假设固体杂质不和 反应)模拟羰基化法精炼镍的实验:
反应)模拟羰基化法精炼镍的实验: 。反应时间和容器中气体总物质的量关系如图所示。下列分析正确的是
。反应时间和容器中气体总物质的量关系如图所示。下列分析正确的是

 密闭容器中投入少量的粗镍和
密闭容器中投入少量的粗镍和 气体(假设固体杂质不和
气体(假设固体杂质不和 反应)模拟羰基化法精炼镍的实验:
反应)模拟羰基化法精炼镍的实验: 。反应时间和容器中气体总物质的量关系如图所示。下列分析正确的是
。反应时间和容器中气体总物质的量关系如图所示。下列分析正确的是
| A.如升温,该反应逆反应速率增大,正反应速率减小 |
B.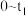 时刻平均反应速率: 时刻平均反应速率: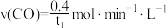 |
C. 时刻到达平衡,且剩余固体均为杂质 时刻到达平衡,且剩余固体均为杂质 |
D. 时刻后,恒温压缩容器体积, 时刻后,恒温压缩容器体积, 转化率增大、平衡常数不变 转化率增大、平衡常数不变 |
您最近一年使用:0次
2022-10-27更新
|
446次组卷
|
4卷引用:湖南省郴州市2022-2023学年高三上学期第一次教学质量监测化学试题



