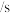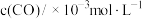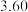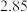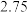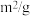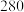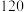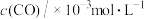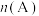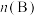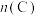名校
1 . 利用催化技术可将汽车尾气中的CO和NO转化为 和
和 ,化学方程式:
,化学方程式: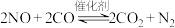 。
。
(1)某温度下,在恒容的密闭容器中通入CO和NO,测得不同时间CO的浓度如下表:
用CO的浓度变化表示0-2s的平均反应速率为______  。
。
(2)下列可说明反应达到平衡状态的是______ 。
a.CO的浓度不再改变
b.容器中的气体质量保持不变
c.NO、CO、 、
、 的浓度之比为2∶2∶2∶1
的浓度之比为2∶2∶2∶1
d.相同时间内,反应消耗2molNO同时消耗
(3)反应物初始浓度相同时,实验温度为280℃和360℃,进行以下实验:
【实验分析与结论】
①补全表格a.______ ,b.______ ,c.______ 。
②测得 ,对比实验Ⅰ、Ⅲ,可得结论:
,对比实验Ⅰ、Ⅲ,可得结论:______ 。
③通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验Ⅰ、Ⅱ,
______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
 和
和 ,化学方程式:
,化学方程式: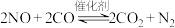 。
。(1)某温度下,在恒容的密闭容器中通入CO和NO,测得不同时间CO的浓度如下表:
时间 |
|
|
|
| …… |
|
|
|
|
| …… |
 。
。(2)下列可说明反应达到平衡状态的是
a.CO的浓度不再改变
b.容器中的气体质量保持不变
c.NO、CO、
 、
、 的浓度之比为2∶2∶2∶1
的浓度之比为2∶2∶2∶1d.相同时间内,反应消耗2molNO同时消耗

(3)反应物初始浓度相同时,实验温度为280℃和360℃,进行以下实验:
实验编号 | 实验目的 |
| 同种催化剂的比表面积 | 达平衡时所用的时间 |
Ⅰ | 对照实验 |
|
|
|
Ⅱ |
|
|
|
|
Ⅲ | 研究温度对尾气转化速率的影响 |
|
|
|
①补全表格a.
②测得
 ,对比实验Ⅰ、Ⅲ,可得结论:
,对比实验Ⅰ、Ⅲ,可得结论:③通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验Ⅰ、Ⅱ,

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
名校
2 .  常用作有机反应中的还原剂,受热发生反应:
常用作有机反应中的还原剂,受热发生反应: 。一定温度时,向
。一定温度时,向 密闭容器中充入
密闭容器中充入 ,体系中
,体系中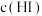 与反应时间t的关系如图。下列说法中,
与反应时间t的关系如图。下列说法中,不正确 的是
 常用作有机反应中的还原剂,受热发生反应:
常用作有机反应中的还原剂,受热发生反应: 。一定温度时,向
。一定温度时,向 密闭容器中充入
密闭容器中充入 ,体系中
,体系中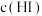 与反应时间t的关系如图。下列说法中,
与反应时间t的关系如图。下列说法中,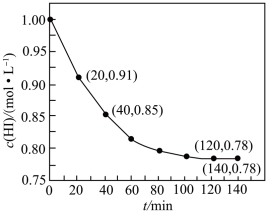
A. 的还原性与 的还原性与 价碘元素有关 价碘元素有关 |
B.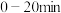 时, 时, 的反应速率为 的反应速率为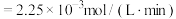 |
C. 时,有 时,有 的 的 发生分解 发生分解 |
D.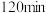 时,反应达到了平衡状态 时,反应达到了平衡状态 |
您最近一年使用:0次
名校
3 . 在恒温恒容密闭容器中充入一定量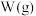 ,发生如下反应:
,发生如下反应: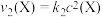 和
和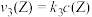 ,其中
,其中 、
、 分别为反应②和③的速率常数,反应③的活化能大于反应②。测得
分别为反应②和③的速率常数,反应③的活化能大于反应②。测得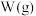 的浓度随时间的变化如下表。
的浓度随时间的变化如下表。
下列说法正确的是
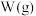 ,发生如下反应:
,发生如下反应: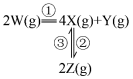
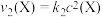 和
和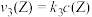 ,其中
,其中 、
、 分别为反应②和③的速率常数,反应③的活化能大于反应②。测得
分别为反应②和③的速率常数,反应③的活化能大于反应②。测得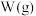 的浓度随时间的变化如下表。
的浓度随时间的变化如下表。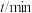 | 0 | 1 | 2 | 3 | 4 | 5 |
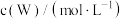 | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 | 0.028 |
A.0~2min内,W的平均反应速率为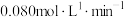 |
| B.若增大容器容积,平衡时Z的产率增大 |
C.若 ,平衡时 ,平衡时 |
D.若升高温度,平衡时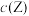 减小 减小 |
您最近一年使用:0次
名校
解题方法
4 . 利用催化技术可将汽车尾气中的CO和NO转化为CO2和N2化学方程式: 。
。
(1)某温度下,在容积不变的密闭容器中通入CO和NO,测得不同时间CO浓度如下表:
用CO的浓度变化表示0~2s的平均反应速率为________  。
。
(2)反应物初始浓度相同时,实验温度为280℃和360℃,进行以下实验:
【实验分析与结论】
①补全表格a.__________ ,b.__________ ,c__________ 。
②测得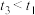 ,对比实验Ⅰ、Ⅲ,可得结论:催化剂的比表面积相同时,
,对比实验Ⅰ、Ⅲ,可得结论:催化剂的比表面积相同时,________ 。
③通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验Ⅰ、Ⅱ,
______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)除催化剂、温度外,还有哪些因素可以加快该反应的化学反应速率_____ (至少填2种)。
 。
。(1)某温度下,在容积不变的密闭容器中通入CO和NO,测得不同时间CO浓度如下表:
时间/s | 0 | 1 | 2 | 3 | …… |
| 3.60 | 3.05 | 2.85 | 2.75 | …… |
 。
。(2)反应物初始浓度相同时,实验温度为280℃和360℃,进行以下实验:
实验编号 | 实验目的 | T/℃ | 同种催化剂的比表面积m2/g | 达平衡时所用的时间/s |
Ⅰ | 对照实验 | 280 | 80 |
|
Ⅱ | a | 280 | 120 |
|
Ⅲ | 研究温度对尾气转化速率的影响 | b | c |
|
①补全表格a.
②测得
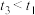 ,对比实验Ⅰ、Ⅲ,可得结论:催化剂的比表面积相同时,
,对比实验Ⅰ、Ⅲ,可得结论:催化剂的比表面积相同时,③通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验Ⅰ、Ⅱ,

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)除催化剂、温度外,还有哪些因素可以加快该反应的化学反应速率
您最近一年使用:0次
名校
5 . 某小组模拟汽车尾气处理。某温度下,将一定量 和
和 投入体积为
投入体积为 、盛有催化剂的密闭容器中,发生反应:
、盛有催化剂的密闭容器中,发生反应: 。测得
。测得 的物质的量浓度随时间变化的关系如图所示。下列说法
的物质的量浓度随时间变化的关系如图所示。下列说法不正确 的是
 和
和 投入体积为
投入体积为 、盛有催化剂的密闭容器中,发生反应:
、盛有催化剂的密闭容器中,发生反应: 。测得
。测得 的物质的量浓度随时间变化的关系如图所示。下列说法
的物质的量浓度随时间变化的关系如图所示。下列说法
A. 段 段 的反应速率 的反应速率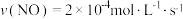 |
B.达平衡时,理论上该反应放出的热量约为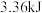 |
C.该温度下,反应的平衡常数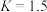 |
| D.升高温度,该反应的平衡常数减小 |
您最近一年使用:0次
6 . 一定温度下,在1 L的恒容密闭容器中发生反应: ,反应过程中的部分数据如下表所示:
,反应过程中的部分数据如下表所示:
下列说法不正确 的是
 ,反应过程中的部分数据如下表所示:
,反应过程中的部分数据如下表所示:时间(t/min) | 物质的量(n/mol) | ||
|
|
| |
0 | 2.0 | 2.4 | 0 |
5 | 0.8 | ||
10 | 1.6 | ||
15 | 1.6 | ||
A.0~5 min用A表示的平均反应速率为 |
| B.此温度下,反应的平衡常数K为1.6 |
| C.物质B的平衡转化率约为33% |
| D.15 min后,再加入A、B、C各1.6 mol,平衡不移动 |
您最近一年使用:0次
名校
解题方法
7 . 探究浓度对化学反应速率的影响。
利用反应: ,反应过程中溶液出现乳白色浑浊,比较浑浊现象出现时间的长短,判断反应进行的快慢。实验数据如下表。
,反应过程中溶液出现乳白色浑浊,比较浑浊现象出现时间的长短,判断反应进行的快慢。实验数据如下表。
(1)乳白色浑浊的主要成分是___________ 。
(2)实验1、2探究 溶液浓度对化学反应速率的影响。
溶液浓度对化学反应速率的影响。
①
___________ 。
②“实验2”中加入 水的主要目的是
水的主要目的是___________ 。
(3)实验1、3探究 溶液的浓度对化学反应速率的影响。则
溶液的浓度对化学反应速率的影响。则
___________ ,
___________ ,
___________ 。
(4)该实验能说明增大反应物的浓度,化学反应速率增大。实验依据是___________ 。
(5)用 传感器测得实验1在
传感器测得实验1在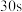 时
时 为
为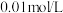 ,则该反应在
,则该反应在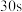 内的化学反应速率
内的化学反应速率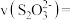
___________  。有同学校认为这样的计算结果误差较大,理由是
。有同学校认为这样的计算结果误差较大,理由是___________ 。
利用反应:
 ,反应过程中溶液出现乳白色浑浊,比较浑浊现象出现时间的长短,判断反应进行的快慢。实验数据如下表。
,反应过程中溶液出现乳白色浑浊,比较浑浊现象出现时间的长短,判断反应进行的快慢。实验数据如下表。| 实验编号 | 加入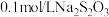 溶液的体积 溶液的体积 | 加入水的体积 | 加入 溶液的体积 溶液的体积 | 溶液出现浑浊的时间(S) |
 |  |  | ||
| 1 | 2 | 0 | 2 |  |
| 2 | 1 |  | 2 |  |
| 3 |  |  |  |  |
(2)实验1、2探究
 溶液浓度对化学反应速率的影响。
溶液浓度对化学反应速率的影响。①

②“实验2”中加入
 水的主要目的是
水的主要目的是(3)实验1、3探究
 溶液的浓度对化学反应速率的影响。则
溶液的浓度对化学反应速率的影响。则


(4)该实验能说明增大反应物的浓度,化学反应速率增大。实验依据是
(5)用
 传感器测得实验1在
传感器测得实验1在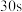 时
时 为
为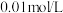 ,则该反应在
,则该反应在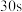 内的化学反应速率
内的化学反应速率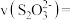
 。有同学校认为这样的计算结果误差较大,理由是
。有同学校认为这样的计算结果误差较大,理由是
您最近一年使用:0次
名校
8 . 一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质量的变化如图所示。下列推断合理的是
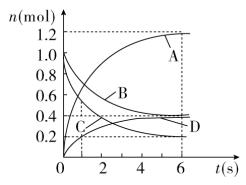
A.该反应的化学方程式为: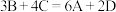 |
B.反应进行到1s时, |
| C.反应进行到6s时,B的平均反应速率为0.05 mol/(L·s) |
| D.反应进行到6s时,各物质的反应速率相等 |
您最近一年使用:0次
名校
9 . 某化学小组选用酸性高锰酸钾溶液和草酸( )溶液,探究外界条件对化学反应速率的影响,进行了如下了三组实验:
)溶液,探究外界条件对化学反应速率的影响,进行了如下了三组实验:
(1)实验原理的离子方程式:____________ 。
(2)实验2中的
______ ,目的是____________ 。
(3)根据上表中的实验数据,可以得到的结论是____________ 。
(4)利用实验1中数据计算,用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为
______ mol/(L⋅min)。
 )溶液,探究外界条件对化学反应速率的影响,进行了如下了三组实验:
)溶液,探究外界条件对化学反应速率的影响,进行了如下了三组实验:实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
a mol/L |
| 0.05 mol/L | 3 mol/L稀硫酸 | ||
1 | 3.0 | 1.0 | 4.0 | 2.0 | 4.0 |
2 | 2.0 | v | 4.0 | 2.0 | 5.2 |
3 | 1.0 | 3.0 | 4.0 | 2.0 | 6.4 |
(2)实验2中的

(3)根据上表中的实验数据,可以得到的结论是
(4)利用实验1中数据计算,用
 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为
您最近一年使用:0次
2024-05-04更新
|
176次组卷
|
2卷引用:北京交大附中2023-2024学年高一下学期期中考试化学试题
名校
解题方法
10 . 工业制硫酸的一步重要反应是SO2的催化氧化。在2L密闭容器中,充入SO2和足量O2,在催化剂、500℃的条件下发生反应。SO2、SO3的物质的量随时间的变化如图。下列说法不正确 的是
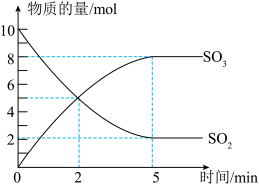
| A.在上述条件下,SO2不可能100%地转化为SO3 |
| B.反应到2min时,正逆反应速率相等 |
| C.反应开始至5min末,以SO2浓度的变化表示该反应的平均反应速率是0.8mol/(L·min) |
| D.使用催化剂是为了加快反应速率,提高生产效率 |
您最近一年使用:0次
2024-05-04更新
|
303次组卷
|
2卷引用:北京市陈经纶中学2023-2024学年高一下学期期中诊断化学试卷