1 . 对SO2、NOx、CO2和CO进行回收利用是节能减排的重要课题。某温度下,向恒容密闭容器中充入NO2、SO2发生反应:NO2(g)+SO2(g)⇌SO3(g)+NO(g)。
(1)①只改变下列某一反应条件时,能使上述反应速率加快的是___________ (填序号)。
a.使用高效催化剂 b.向容器中充入氩气 c.降低温度 d.减小NO的物质的量
②下列能说明反应达到平衡状态的是___________ (填字母)。
a.混合气体的密度保持不变
b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变
d.每生成1molSO3的同时消耗1molNO
(2)在体积为 密闭容器中充入
密闭容器中充入 和
和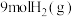 ,发生反应
,发生反应 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
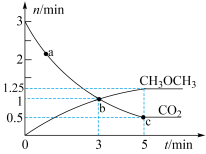
①反应到达3min时,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②0~5min内,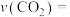
___________  。
。
③反应达到平衡状态时, 的体积分数为
的体积分数为___________ %(保留1位小数)。
④a、b、c三点中代表达到平衡的是___________ ,a点的正反应速率___________ (填>、<或=)b点的逆反应速率。
(1)①只改变下列某一反应条件时,能使上述反应速率加快的是
a.使用高效催化剂 b.向容器中充入氩气 c.降低温度 d.减小NO的物质的量
②下列能说明反应达到平衡状态的是
a.混合气体的密度保持不变
b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变
d.每生成1molSO3的同时消耗1molNO
(2)在体积为
 密闭容器中充入
密闭容器中充入 和
和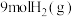 ,发生反应
,发生反应 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
①反应到达3min时,

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②0~5min内,
 。
。③反应达到平衡状态时,
 的体积分数为
的体积分数为④a、b、c三点中代表达到平衡的是
您最近一年使用:0次
解题方法
2 . 大气中氮氧化物( )是造成灰霾、光化学烟雾的重要原因,对氮氧化物的研究具有重要意义。回答下列问题:
)是造成灰霾、光化学烟雾的重要原因,对氮氧化物的研究具有重要意义。回答下列问题:
(1)已知在催化条件下 与CO发生反应:
与CO发生反应: 。
。
①在 ℃,将
℃,将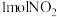 和1molCO加入容积为0.5L的密闭容器中发生上述反应,2min末,测得CO为0.8mol。在0~2min内,用
和1molCO加入容积为0.5L的密闭容器中发生上述反应,2min末,测得CO为0.8mol。在0~2min内,用 浓度变化表示的化学反应速率为
浓度变化表示的化学反应速率为_______ 。
②研究表明,在 ℃,
℃, 与CO还会发生副反应
与CO还会发生副反应 。若在
。若在 ℃,恒容下,向平衡体系中再充入少量
℃,恒容下,向平衡体系中再充入少量 ,反应
,反应 的平衡将
的平衡将_______ (填“正向移动”“逆向移动”或“不移动”)。
(2)若在温度和体积相同的两个密闭容器中,按不同方式投入反应物,只发生反应 ,测得平衡时有关数据如下表:
,测得平衡时有关数据如下表:
α=_______ ,写出该反应的热化学方程式_______ ( 用含
用含 或
或 的表达式表示)。
的表达式表示)。
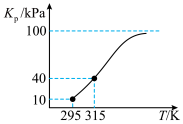
(3)将一定量 气体充入压强为100kPa的恒压容器中,发生反应
气体充入压强为100kPa的恒压容器中,发生反应
 ,测得平衡常数
,测得平衡常数 (用各物质的平衡分压代替平衡浓度计算)随温度的变化如图所示。
(用各物质的平衡分压代替平衡浓度计算)随温度的变化如图所示。
①
_______ 0(填“>”“=”或“<”)。
②向体积相等的丙、丁两个密闭容器中分别加入等量的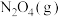 ,发生反应并达到平衡。保持丙容器恒容、丁容器恒压,将两体系的温度均从295K升至315K,则
,发生反应并达到平衡。保持丙容器恒容、丁容器恒压,将两体系的温度均从295K升至315K,则_______ (填“丙”或“丁”)容器中的平衡移动程度更大,原因是_______ 。
 )是造成灰霾、光化学烟雾的重要原因,对氮氧化物的研究具有重要意义。回答下列问题:
)是造成灰霾、光化学烟雾的重要原因,对氮氧化物的研究具有重要意义。回答下列问题:(1)已知在催化条件下
 与CO发生反应:
与CO发生反应: 。
。①在
 ℃,将
℃,将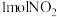 和1molCO加入容积为0.5L的密闭容器中发生上述反应,2min末,测得CO为0.8mol。在0~2min内,用
和1molCO加入容积为0.5L的密闭容器中发生上述反应,2min末,测得CO为0.8mol。在0~2min内,用 浓度变化表示的化学反应速率为
浓度变化表示的化学反应速率为②研究表明,在
 ℃,
℃, 与CO还会发生副反应
与CO还会发生副反应 。若在
。若在 ℃,恒容下,向平衡体系中再充入少量
℃,恒容下,向平衡体系中再充入少量 ,反应
,反应 的平衡将
的平衡将(2)若在温度和体积相同的两个密闭容器中,按不同方式投入反应物,只发生反应
 ,测得平衡时有关数据如下表:
,测得平衡时有关数据如下表:| 容器 | 甲 | 乙 |
| 反应物投入量 | 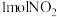 、 、 | 2molNO、 |
| CO或NO的转化率 | 40% | α |
| 能量变化 | 放出 | 吸收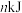 |
 用含
用含 或
或 的表达式表示)。
的表达式表示)。(3)将一定量
 气体充入压强为100kPa的恒压容器中,发生反应
气体充入压强为100kPa的恒压容器中,发生反应
 ,测得平衡常数
,测得平衡常数 (用各物质的平衡分压代替平衡浓度计算)随温度的变化如图所示。
(用各物质的平衡分压代替平衡浓度计算)随温度的变化如图所示。
①

②向体积相等的丙、丁两个密闭容器中分别加入等量的
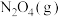 ,发生反应并达到平衡。保持丙容器恒容、丁容器恒压,将两体系的温度均从295K升至315K,则
,发生反应并达到平衡。保持丙容器恒容、丁容器恒压,将两体系的温度均从295K升至315K,则
您最近一年使用:0次
名校
3 . 异丙醇(C3H8O)可由生物质转化得到,催化异丙醇脱水制取高值化学品丙烯(C3H6)的工业化技术已引起人们的关注,其主要反应如下:
Ⅰ、C3H8O (g) C3H6 (g)+H2O(g) ΔH1=+52kJ·mol-1
C3H6 (g)+H2O(g) ΔH1=+52kJ·mol-1
Ⅱ、2C3H6(g) C6H12(g) ΔH2=-97kJ·mol-1
C6H12(g) ΔH2=-97kJ·mol-1
回答下列问题:
(1)已知2C3H8O(g)+9O2(g)=6CO2 (g)+8H2O(g) ΔH=-3750kJ·mol-1,则C3H6(g)燃烧生成CO2(g)和H2O(g)的热化学方程式为_____ 。
(2)在1350℃下,刚性密闭容器中的反应体系内水蒸气浓度与反应时间关系如下表:
4~8μs内,v(C3H8O)=_____ ppm·μs一1;
②t_____ 16(填“>”“<”或“=”)。
(3)在恒温刚性密闭容器中,反应Ⅰ、Ⅱ均达到平衡的判据是_____ (填标号)。
a.H2O(g)的分压不变
b.混合气体密度不变
c.n(C3H6)=2n(C6H12)
d.v正(H2O)=v逆(C3H8O)
(4)下图为反应Ⅰ、Ⅱ达到平衡时lgQp与温度的关系曲线。

(已知:对于可逆反应aA(g)+bB(g) cC(g)+dD(g),任意时刻Qp=
cC(g)+dD(g),任意时刻Qp= ,式中p(X))表示物质×的分压)
,式中p(X))表示物质×的分压)
①在350℃恒压平衡体系中充入少量水蒸气时,反应Ⅰ的的状态最有可能对应图中的_____ 点(填“甲”“乙”或“丙”),判断依据是_____ 。
②350℃时,在密闭容器中加入一定量的C3H8O,体系达到平衡后,测得C6H12的分压为xMPa,则水蒸气的分压为_____ MPa(用含x的代数式表示)。
Ⅰ、C3H8O (g)
 C3H6 (g)+H2O(g) ΔH1=+52kJ·mol-1
C3H6 (g)+H2O(g) ΔH1=+52kJ·mol-1Ⅱ、2C3H6(g)
 C6H12(g) ΔH2=-97kJ·mol-1
C6H12(g) ΔH2=-97kJ·mol-1回答下列问题:
(1)已知2C3H8O(g)+9O2(g)=6CO2 (g)+8H2O(g) ΔH=-3750kJ·mol-1,则C3H6(g)燃烧生成CO2(g)和H2O(g)的热化学方程式为
(2)在1350℃下,刚性密闭容器中的反应体系内水蒸气浓度与反应时间关系如下表:
| 反应时间/μs | 0 | 4 | 8 | 12 | t | 20 |
| H2O浓度/ppm | 0 | 2440 | 3200 | 3600 | 4000 | 4100 |
②t
(3)在恒温刚性密闭容器中,反应Ⅰ、Ⅱ均达到平衡的判据是
a.H2O(g)的分压不变
b.混合气体密度不变
c.n(C3H6)=2n(C6H12)
d.v正(H2O)=v逆(C3H8O)
(4)下图为反应Ⅰ、Ⅱ达到平衡时lgQp与温度的关系曲线。

(已知:对于可逆反应aA(g)+bB(g)
 cC(g)+dD(g),任意时刻Qp=
cC(g)+dD(g),任意时刻Qp= ,式中p(X))表示物质×的分压)
,式中p(X))表示物质×的分压) ①在350℃恒压平衡体系中充入少量水蒸气时,反应Ⅰ的的状态最有可能对应图中的
②350℃时,在密闭容器中加入一定量的C3H8O,体系达到平衡后,测得C6H12的分压为xMPa,则水蒸气的分压为
您最近一年使用:0次
名校
4 . 甲醇、乙醇来源丰富、价格低廉、运输贮存方便,都是重要的化工原料,有着重要的用途和应用前景,可以用多种方法合成。用 生产甲醇、乙醇。
生产甲醇、乙醇。
(1)已知: 的燃烧热为
的燃烧热为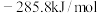 ,
, 的燃烧热为
的燃烧热为 ,
,
 ,则
,则

_______ kJ/mol。
(2)为探究用 生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入
生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入 和
和 在一定条件下发生反应,测得
在一定条件下发生反应,测得 、
、 和
和 的物质的量(n)随时间的变化如图所示:
的物质的量(n)随时间的变化如图所示:

①从反应开始到平衡,氢气的平均反应速率
_______ 。
②下列措施能使 的平衡转化率增大的是
的平衡转化率增大的是_______ (填序号)。
A.在原容器中再充入
B.在原容器中再充入
C.在原容器中充入1mol氦气
D.使用更有效的催化剂
E.缩小容器的容积
(3) 也可通过催化加氢合成乙醇,其反应原理为
也可通过催化加氢合成乙醇,其反应原理为
 。设m为起始时的投料比,即
。设m为起始时的投料比,即 。通过实验得到如图所示图象:
。通过实验得到如图所示图象:

①图甲中投料比相同,温度从高到低的顺序为_______ 。
②图乙中 、
、 、
、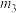 从大到小的顺序为
从大到小的顺序为_______ 。
③图丙表示在总压为5MPa的恒压条件下,且 时,平衡状态时各物质的物质的量分数与温度的关系,
时,平衡状态时各物质的物质的量分数与温度的关系, 温度时,该反应压强平衡常数
温度时,该反应压强平衡常数 的计算表达式为
的计算表达式为_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,代入数据,不用计算)。
 生产甲醇、乙醇。
生产甲醇、乙醇。(1)已知:
 的燃烧热为
的燃烧热为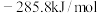 ,
, 的燃烧热为
的燃烧热为 ,
,
 ,则
,则

(2)为探究用
 生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入
生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入 和
和 在一定条件下发生反应,测得
在一定条件下发生反应,测得 、
、 和
和 的物质的量(n)随时间的变化如图所示:
的物质的量(n)随时间的变化如图所示:
①从反应开始到平衡,氢气的平均反应速率

②下列措施能使
 的平衡转化率增大的是
的平衡转化率增大的是A.在原容器中再充入

B.在原容器中再充入

C.在原容器中充入1mol氦气
D.使用更有效的催化剂
E.缩小容器的容积
(3)
 也可通过催化加氢合成乙醇,其反应原理为
也可通过催化加氢合成乙醇,其反应原理为
 。设m为起始时的投料比,即
。设m为起始时的投料比,即 。通过实验得到如图所示图象:
。通过实验得到如图所示图象:
①图甲中投料比相同,温度从高到低的顺序为
②图乙中
 、
、 、
、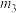 从大到小的顺序为
从大到小的顺序为③图丙表示在总压为5MPa的恒压条件下,且
 时,平衡状态时各物质的物质的量分数与温度的关系,
时,平衡状态时各物质的物质的量分数与温度的关系, 温度时,该反应压强平衡常数
温度时,该反应压强平衡常数 的计算表达式为
的计算表达式为
您最近一年使用:0次
名校
解题方法
5 . 室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v1=k1c2(M),反应②的速率可表示为v2=k2c2(M)(k1、k2为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法正确的是
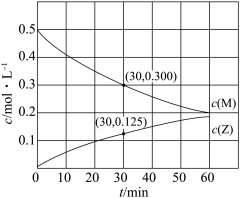

| A.0~30min时间段内,Y的平均反应速率为6.67×10-3mol•L-1•min-1 |
| B.反应开始后,体系中Y和Z的浓度之比保持不变 |
| C.如果反应能进行到底,反应结束时37.5%的M转化为Z |
| D.反应①的活化能比反应②的活化能小 |
您最近一年使用:0次
2023-11-11更新
|
73次组卷
|
2卷引用: 四川省成都市石室中学2023~2024学年高二上学期10月月考化学试题
名校
6 . 环戊二烯(C5H6)是一种重要的有机化工原料。
Ⅰ.环戊二烯容易反应生成双环戊二烯(C10H12):2C5H6(g) C10H12(g),不同温度下,溶液中环戊二烯(C5H6)浓度(初始浓度为1.5 mol·L-1 )与反应时间的关系如图所示:
C10H12(g),不同温度下,溶液中环戊二烯(C5H6)浓度(初始浓度为1.5 mol·L-1 )与反应时间的关系如图所示:
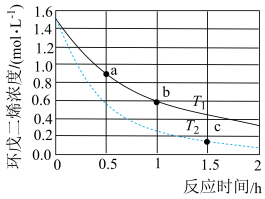
(1)反应开始至b点时,用环戊二烯(C5H6)表示的平均速率为___________ 。
(2)T1_______ T2,a点的逆反应速率___________ b点的正反应速率(两空均选填“>”、“<”或“=”)。
(3)一定量的环戊二烯气体在恒温恒压的密闭容器中发生上述反应,可说明一定达化学平衡状态的是___________ (填字母)。
a.v(C5H6)=2v(C10H12)
b.容器内气体压强不再变化
c.容器内混合气体的密度不再变化
d.容器内混合气体的平均相对分子质量不再变化
Ⅱ.可用环戊烯(C5H8)制备环戊二烯(C5H6),有如下反应:
反应i:C5H8(g) C5H6(g) + H2 (g) ∆H1 K1
C5H6(g) + H2 (g) ∆H1 K1
反应ii:2HI(g) H2 (g) + I2(g) ∆H2 = +11.0 kJ·mol-1 K2
H2 (g) + I2(g) ∆H2 = +11.0 kJ·mol-1 K2
反应iii:C5H8(g) + I2(g) C5H6(g) + 2HI(g) ∆H3 = + 89.3 kJ·mol-1 K3
C5H6(g) + 2HI(g) ∆H3 = + 89.3 kJ·mol-1 K3
(4)反应i的焓变∆H1=___________ ,反应iii的平衡常数K3为___________ (用K1,K2表示)。
(5)某温度时在恒容密闭容器中充入等物质的量的碘和环戊烯发生反应iii,起始总压为P0,平衡时总压为1.2P0。
①平衡时HI的体积分数为___________ %
②用平衡分压(分压=总压×物质的量分数)代替平衡浓度计算压强平衡常数Kp =___________ (要求用最简整数比,含p0的代数式表示)。
③达到平衡后,欲增加环戊烯(C5H8)的平衡转化率,同时加快反应速率可采取的措施有___________ (仅写一条)。
Ⅰ.环戊二烯容易反应生成双环戊二烯(C10H12):2C5H6(g)
 C10H12(g),不同温度下,溶液中环戊二烯(C5H6)浓度(初始浓度为1.5 mol·L-1 )与反应时间的关系如图所示:
C10H12(g),不同温度下,溶液中环戊二烯(C5H6)浓度(初始浓度为1.5 mol·L-1 )与反应时间的关系如图所示:
(1)反应开始至b点时,用环戊二烯(C5H6)表示的平均速率为
(2)T1
(3)一定量的环戊二烯气体在恒温恒压的密闭容器中发生上述反应,可说明一定达化学平衡状态的是
a.v(C5H6)=2v(C10H12)
b.容器内气体压强不再变化
c.容器内混合气体的密度不再变化
d.容器内混合气体的平均相对分子质量不再变化
Ⅱ.可用环戊烯(C5H8)制备环戊二烯(C5H6),有如下反应:
反应i:C5H8(g)
 C5H6(g) + H2 (g) ∆H1 K1
C5H6(g) + H2 (g) ∆H1 K1反应ii:2HI(g)
 H2 (g) + I2(g) ∆H2 = +11.0 kJ·mol-1 K2
H2 (g) + I2(g) ∆H2 = +11.0 kJ·mol-1 K2反应iii:C5H8(g) + I2(g)
 C5H6(g) + 2HI(g) ∆H3 = + 89.3 kJ·mol-1 K3
C5H6(g) + 2HI(g) ∆H3 = + 89.3 kJ·mol-1 K3(4)反应i的焓变∆H1=
(5)某温度时在恒容密闭容器中充入等物质的量的碘和环戊烯发生反应iii,起始总压为P0,平衡时总压为1.2P0。
①平衡时HI的体积分数为
②用平衡分压(分压=总压×物质的量分数)代替平衡浓度计算压强平衡常数Kp =
③达到平衡后,欲增加环戊烯(C5H8)的平衡转化率,同时加快反应速率可采取的措施有
您最近一年使用:0次
7 . I.查阅资料:NaNO2溶液和NH4Cl溶液在50℃左右微热可反应生成N2。
(1)实验小组用不同浓度的NaNO2溶液、NH4Cl溶液及少量醋酸溶液(作催化剂)反应,其速率方程为v=kcm(NaNO2)•cn(NH4Cl)•c(H+),k为反应速率常数,以此计算反应的瞬时速率。反应物浓度与反应的瞬时速率如表所示:
①由表实验数据计算得m=________ 。
②该反应的速率常数k=________ L3•mol-3•min-1。
Ⅱ.由CO2与H2制备甲醇是当今研究的热点之一。
(2)在一定条件下,向0.5L恒容密闭容器中充入xmolCO2和ymolH2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH3=-50kJ•mol-1
CH3OH(g)+H2O(g) ΔH3=-50kJ•mol-1
①若x=1、y=3,测得在相同时间内,不同温度下H2的转化率如图1所示,点a_________ 填“已”或“未”)达到平衡。T2时,若起始压强为10atm,Kp=________ atm-2(结果保留一位小数,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。

②已知速率方程v正=k正c(CO2)·c3(H2),v逆=k逆c(CH3OH)·c(H2O),k正、k逆是速率常数,只受温度影响,图2表示速率常数k正、k逆的对数lgk与温度的倒数 之间的关系,A、B、D、E分别代表图1中a点、c点的速率常数,其中点
之间的关系,A、B、D、E分别代表图1中a点、c点的速率常数,其中点________ (填A或B或D或E)表示c点的lgk逆。

Ⅲ.回答下列问题:
(3)甲醇和CO2可直接合成碳酸二甲酯(CH3OCOOCH3,简称DMC):2CH3OH(g)+CO2(g) CH3OCOOCH3(g)+H2O(g) ΔH<0。一定条件下分别向甲、乙、丙三个恒容密闭容器中加入一定量的初始物质发生该反应,各容器中温度、反应物的起始量如表,反应过程中DMC的物质的量浓度随时间变化如图3所示:
CH3OCOOCH3(g)+H2O(g) ΔH<0。一定条件下分别向甲、乙、丙三个恒容密闭容器中加入一定量的初始物质发生该反应,各容器中温度、反应物的起始量如表,反应过程中DMC的物质的量浓度随时间变化如图3所示:

乙容器中,若平衡时n(CO2)=0.2mol,则T1________ T2(填“>”“<"或”=”)。甲、丙两容器的反应达平衡时CO2的转化率:甲________ 丙(填“>”“<"或”=”)。
(1)实验小组用不同浓度的NaNO2溶液、NH4Cl溶液及少量醋酸溶液(作催化剂)反应,其速率方程为v=kcm(NaNO2)•cn(NH4Cl)•c(H+),k为反应速率常数,以此计算反应的瞬时速率。反应物浓度与反应的瞬时速率如表所示:
| 实验编号 | NaNO2溶液/mol•L-1 | NH4Cl溶液/mol•L-1 | H+/mol•L-1 | V/mol•L-1•min-1 |
| 1 | 0.100 | 0.100 | 0.001 | 2.0×10-8 |
| 2 | 0.200 | 0.100 | 0.001 | 8.0×10-8 |
| 3 | 0.100 | 0.200 | 0.001 | 4.0×10-8 |
②该反应的速率常数k=
Ⅱ.由CO2与H2制备甲醇是当今研究的热点之一。
(2)在一定条件下,向0.5L恒容密闭容器中充入xmolCO2和ymolH2,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH3=-50kJ•mol-1
CH3OH(g)+H2O(g) ΔH3=-50kJ•mol-1①若x=1、y=3,测得在相同时间内,不同温度下H2的转化率如图1所示,点a

②已知速率方程v正=k正c(CO2)·c3(H2),v逆=k逆c(CH3OH)·c(H2O),k正、k逆是速率常数,只受温度影响,图2表示速率常数k正、k逆的对数lgk与温度的倒数
 之间的关系,A、B、D、E分别代表图1中a点、c点的速率常数,其中点
之间的关系,A、B、D、E分别代表图1中a点、c点的速率常数,其中点
Ⅲ.回答下列问题:
(3)甲醇和CO2可直接合成碳酸二甲酯(CH3OCOOCH3,简称DMC):2CH3OH(g)+CO2(g)
 CH3OCOOCH3(g)+H2O(g) ΔH<0。一定条件下分别向甲、乙、丙三个恒容密闭容器中加入一定量的初始物质发生该反应,各容器中温度、反应物的起始量如表,反应过程中DMC的物质的量浓度随时间变化如图3所示:
CH3OCOOCH3(g)+H2O(g) ΔH<0。一定条件下分别向甲、乙、丙三个恒容密闭容器中加入一定量的初始物质发生该反应,各容器中温度、反应物的起始量如表,反应过程中DMC的物质的量浓度随时间变化如图3所示:
| 容器 | 甲 | 乙 | 丙 |
| 容积(L) | 0.5 | 0.5 | V |
| 温度(℃) | T1 | T2 | T1 |
| 起始量 | 1molCO2(g)、2molCH3OH(g) | 1molDMC(g)、1molH2O(g) | 2molCO2(g)、2molCH3OH(g) |
您最近一年使用:0次
名校
解题方法
8 . 在人们高度重视环境和保护环境的今天,消除和利用硫氧化物、氮氧化物、碳氧化物对改善大气质量具有重要的意义。
(1)在绝热的某刚性容器中置入 和
和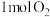 ,发生反应:
,发生反应:
 。下列说法中能够判断该反应一定处于平衡状态的有
。下列说法中能够判断该反应一定处于平衡状态的有___________ (填数字序号)。
①容器中 、
、 、
、 共存 ②单位时间内生成
共存 ②单位时间内生成 的同时消耗
的同时消耗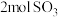
③反应容器中压强不随时间变化 ④容器中温度恒定不变
⑤容器中 、
、 、
、 的物质的量之比为2∶1∶2
的物质的量之比为2∶1∶2
(2)氮氧化物是造成光化学污染的罪魁祸首,用一氧化碳还原氮氧化物,可防止氮氧化物污染,如反应:
 =
= 。
。
①已知该反应在不同条件下的化学反应速率如下:
a.v(CO)=1.5 mol·L-1·min-1 b.v(NO)=0.03 mol·L-1·s-1
c.v(N2)=0.6 mol·L-1·min-1 d.v(CO2)=1.6 mol·L-1·min-1
上述4种情况反应速率最快的是___________ (填字母)。
②实验测得反应2CO(g)+2NO(g) 2CO2(g)+N2 (g)
2CO2(g)+N2 (g)  =
= ,v正=k正•c2(NO)•c2(CO),v逆=k逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。在一定温度下达到平衡时v正 = v逆,则
,v正=k正•c2(NO)•c2(CO),v逆=k逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。在一定温度下达到平衡时v正 = v逆,则
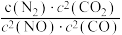 ,达到平衡后,仅升高温度,平衡向
,达到平衡后,仅升高温度,平衡向___________ 移动(填“正反应方向”“逆反应方向”或“不”)。k正增大的倍数___________ (填“>”、“<”或“=”)k逆增大的倍数。
(3)已知:
 。将1mol CO和
。将1mol CO和 充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
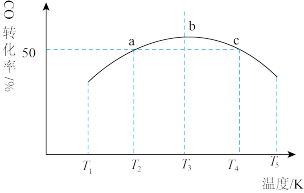
①
___________ 0(填“>”或“<”)。
②由图可知,T3前反应中CO的转化率随温度升高而增大,原因是___________ 。
③已知c点时容器内的压强为p,在 温度下该反应的压强平衡常数
温度下该反应的压强平衡常数 为
为___________ (用含p的关系式表示)。( 为以分压表示的平衡常数,分压=总压×物质的量分数)
为以分压表示的平衡常数,分压=总压×物质的量分数)
(1)在绝热的某刚性容器中置入
 和
和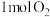 ,发生反应:
,发生反应:
 。下列说法中能够判断该反应一定处于平衡状态的有
。下列说法中能够判断该反应一定处于平衡状态的有①容器中
 、
、 、
、 共存 ②单位时间内生成
共存 ②单位时间内生成 的同时消耗
的同时消耗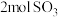
③反应容器中压强不随时间变化 ④容器中温度恒定不变
⑤容器中
 、
、 、
、 的物质的量之比为2∶1∶2
的物质的量之比为2∶1∶2(2)氮氧化物是造成光化学污染的罪魁祸首,用一氧化碳还原氮氧化物,可防止氮氧化物污染,如反应:

 =
= 。
。①已知该反应在不同条件下的化学反应速率如下:
a.v(CO)=1.5 mol·L-1·min-1 b.v(NO)=0.03 mol·L-1·s-1
c.v(N2)=0.6 mol·L-1·min-1 d.v(CO2)=1.6 mol·L-1·min-1
上述4种情况反应速率最快的是
②实验测得反应2CO(g)+2NO(g)
 2CO2(g)+N2 (g)
2CO2(g)+N2 (g)  =
= ,v正=k正•c2(NO)•c2(CO),v逆=k逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。在一定温度下达到平衡时v正 = v逆,则
,v正=k正•c2(NO)•c2(CO),v逆=k逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。在一定温度下达到平衡时v正 = v逆,则
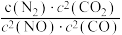 ,达到平衡后,仅升高温度,平衡向
,达到平衡后,仅升高温度,平衡向(3)已知:

 。将1mol CO和
。将1mol CO和 充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
①

②由图可知,T3前反应中CO的转化率随温度升高而增大,原因是
③已知c点时容器内的压强为p,在
 温度下该反应的压强平衡常数
温度下该反应的压强平衡常数 为
为 为以分压表示的平衡常数,分压=总压×物质的量分数)
为以分压表示的平衡常数,分压=总压×物质的量分数)
您最近一年使用:0次
名校
解题方法
9 . 完成下列小题
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和 )。
)。 与
与 通入聚集太阳能反应器,发生反应
通入聚集太阳能反应器,发生反应
 。
。
已知:Ⅰ. 、
、 、CO的燃烧热(
、CO的燃烧热( )分别为
)分别为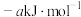 、
、 、
、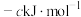 ;
;
Ⅱ.
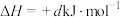 。
。
则
_____  (用含字母a、b、c、d的代数式表示)。
(用含字母a、b、c、d的代数式表示)。
(2)用合成气生成甲醇的反应为
 ,在10L恒容密闭容器中按物质的量之比1:2充入CO和
,在10L恒容密闭容器中按物质的量之比1:2充入CO和 ,200℃时
,200℃时 随时间的变化如表所示:
随时间的变化如表所示:
①0~3min内用 表示的反应速率
表示的反应速率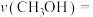
_____ 。
②200℃时,该反应的平衡常数
_____ 。向上述200℃达到平衡的恒容密闭容器中再加入5molCO、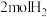 、
、 ,保持温度不变,则反应
,保持温度不变,则反应_____ (填“正向”“逆向”或“不”)进行。
③上述反应如果在绝热恒容的密闭环境下进行,下列各项可作为该反应达到平衡状态的标志的是_____ (填字母)。
A.混合气体密度不再变化
B.容器内的温度保持不变
C.CO和 的物质的量之比保持不变
的物质的量之比保持不变
D.CO的消耗速率与 的生成速率之比为1:1
的生成速率之比为1:1
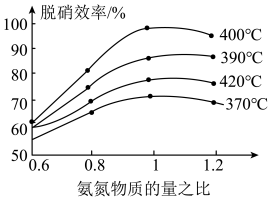
(3)汽车尾气是雾霾形成的原因之一、研究氮氧化物的处理方法可有效减少雾霾的形成,可采用在催化剂作用下氧化还原法脱硝: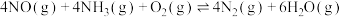
 。根据图示判断提高脱硝效率的最佳条件是
。根据图示判断提高脱硝效率的最佳条件是_____ ;氨氮物质的量之比一定时,在400℃时,脱硝效率最大,其可能的原因是_____ 。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和
 )。
)。 与
与 通入聚集太阳能反应器,发生反应
通入聚集太阳能反应器,发生反应
 。
。已知:Ⅰ.
 、
、 、CO的燃烧热(
、CO的燃烧热( )分别为
)分别为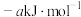 、
、 、
、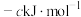 ;
;Ⅱ.

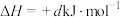 。
。则

 (用含字母a、b、c、d的代数式表示)。
(用含字母a、b、c、d的代数式表示)。(2)用合成气生成甲醇的反应为

 ,在10L恒容密闭容器中按物质的量之比1:2充入CO和
,在10L恒容密闭容器中按物质的量之比1:2充入CO和 ,200℃时
,200℃时 随时间的变化如表所示:
随时间的变化如表所示:| t/min | 0 | 1 | 3 | 5 |
 /mol /mol | 8.0 | 5.4 | 4.0 | 4.0 |
 表示的反应速率
表示的反应速率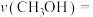
②200℃时,该反应的平衡常数

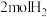 、
、 ,保持温度不变,则反应
,保持温度不变,则反应③上述反应如果在绝热恒容的密闭环境下进行,下列各项可作为该反应达到平衡状态的标志的是
A.混合气体密度不再变化
B.容器内的温度保持不变
C.CO和
 的物质的量之比保持不变
的物质的量之比保持不变D.CO的消耗速率与
 的生成速率之比为1:1
的生成速率之比为1:1(3)汽车尾气是雾霾形成的原因之一、研究氮氧化物的处理方法可有效减少雾霾的形成,可采用在催化剂作用下氧化还原法脱硝:
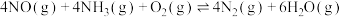
 。根据图示判断提高脱硝效率的最佳条件是
。根据图示判断提高脱硝效率的最佳条件是
您最近一年使用:0次
2023-09-21更新
|
124次组卷
|
2卷引用:四川省绵阳南山中学2023-2024学年高三上学期第二次综合演练理综化学试题
名校
10 . 研究氮的相关化合物在化工生产中有重要意义。
(1)在2L的恒温恒容密闭容器中,发生反应 ,通入等物质的量的NO和
,通入等物质的量的NO和 气体,
气体,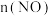 随时间的变化如下表:
随时间的变化如下表:
①0~4s内,
___________  。
。
②在第5s时, 的转化率为
的转化率为___________ 。
③由数据推测,反应在第4s时恰好达到平衡状态。该推测___________ (填“正确”或“错误”)。
(2)用一氧化碳或活性炭还原氮氧化物,减少大气污染。一定条件下,用CO与NO反应生成 和
和 ,反应的化学方程式为
,反应的化学方程式为 。为提高该反应的速率,下列措施可行的是___________(填标号)。
。为提高该反应的速率,下列措施可行的是___________(填标号)。
(3)废气脱碳制甲醇:向2L密闭容器中充入2mol 和6mol
和6mol  ,在恒容绝热的条件下发生反应:
,在恒容绝热的条件下发生反应:
 。下列叙述中,能说明此反应达到平衡状态的是___________(填标号)。
。下列叙述中,能说明此反应达到平衡状态的是___________(填标号)。
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①氢氧燃料电池的在导线中电子的方向为由___________ (用a、b表示)。
②溶液中OH- 移向___________ 电极(填“A”或“B”)。
③该原电池的B极发生___________ (填“氧化”或“还原”)反应,该电极的反应式为___________ 。
(1)在2L的恒温恒容密闭容器中,发生反应
 ,通入等物质的量的NO和
,通入等物质的量的NO和 气体,
气体,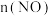 随时间的变化如下表:
随时间的变化如下表:| t/s | 0 | 1 | 2 | 3 | 4 | 5 |
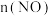 /mol /mol | 0.020 | 0.012 | 0.008 | 0.005 | 0.004 | 0.004 |

 。
。②在第5s时,
 的转化率为
的转化率为③由数据推测,反应在第4s时恰好达到平衡状态。该推测
(2)用一氧化碳或活性炭还原氮氧化物,减少大气污染。一定条件下,用CO与NO反应生成
 和
和 ,反应的化学方程式为
,反应的化学方程式为 。为提高该反应的速率,下列措施可行的是___________(填标号)。
。为提高该反应的速率,下列措施可行的是___________(填标号)。| A.压缩容器体积 |
| B.适当降温 |
| C.使用合适催化剂 |
| D.恒温恒压下,充入稀有气体 |
(3)废气脱碳制甲醇:向2L密闭容器中充入2mol
 和6mol
和6mol  ,在恒容绝热的条件下发生反应:
,在恒容绝热的条件下发生反应:
 。下列叙述中,能说明此反应达到平衡状态的是___________(填标号)。
。下列叙述中,能说明此反应达到平衡状态的是___________(填标号)。| A.单位时间内断裂3mol H-H键的同时断裂2mol O-H键 |
B. 和 和 的浓度比为1∶3 的浓度比为1∶3 |
| C.容器内温度不再变化 |
| D.混合气体的平均相对分子质量不再变化 |
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①氢氧燃料电池的在导线中电子的方向为由
②溶液中OH- 移向
③该原电池的B极发生
您最近一年使用:0次
2023-07-14更新
|
418次组卷
|
2卷引用:四川省什邡中学2023-2024学年高二上学期10月月考化学试题



