名校
1 . 对于反应 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.该反应的 |
B.反应的平衡常数可表示为 |
| C.使用高效催化剂能降低反应的焓变 |
D.其他条件相同,增大 的转化率下降 的转化率下降 |
您最近一年使用:0次
2024-02-29更新
|
42次组卷
|
2卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题
名校
解题方法
2 . “肼合成酶”以其中的Fe2+配合物为催化中心,可将NH2OH与NH3转化为肼(NH2NH2)其反应历程如下所示。下列说法错误的是


| A.反应历程涉及有N-H,N-O键断裂,还有N一N键的生成 |
| B.NH2NH2是非极性分子,其中N原子均为sp2杂化 |
| C.催化中心的Fe2+被氧化为Fe3+,又被还原为Fe2+ |
| D.将NH2OH替换为ND2OD,反应可得ND2NH2 |
您最近一年使用:0次
名校
解题方法
3 . 以甲醇为原料,采用钴碘催化法循环制醋酸,过程如图所示。下列说法正确的是
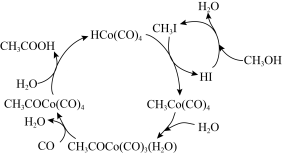

A.总反应的原子利用率为 |
B. 和 和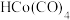 可降低该反应的活化能及反应热 可降低该反应的活化能及反应热 |
C. 的VSEPR模型为 的VSEPR模型为 形 形 |
D.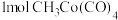 中 中 键数目 键数目 |
您最近一年使用:0次
2024-02-25更新
|
306次组卷
|
3卷引用:河北省石家庄市第二中学2023-2024学年高二下学期3月月考化学试题
4 . 下列说法错误的是
| A.发生碰撞的分子具有足够能量和适当取向时;才能发生化学反应 |
| B.增大反应物浓度,可增大活化分子百分数,使有效碰撞次数增多 |
| C.升高温度,可增大活化分子百分数,也可增加反应物分子间的有效碰撞几率 |
| D.使用催化剂,可以降低反应活化能,增大活化分子百分数,使有效碰撞次数增多 |
您最近一年使用:0次
名校
解题方法
5 . 氮肥是保证粮食安全的重要物资,一种利用电化学制备 的历程如图所示。下列说法错误的是
的历程如图所示。下列说法错误的是
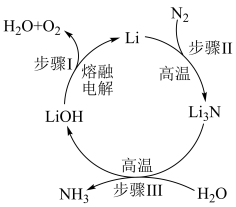
 的历程如图所示。下列说法错误的是
的历程如图所示。下列说法错误的是
A.步骤Ⅰ中阳极反应式为 |
| B.步骤Ⅱ中的反应属于氮的固定 |
C. 、LiOH为该历程中的催化剂 、LiOH为该历程中的催化剂 |
D.该历程总反应为 |
您最近一年使用:0次
名校
解题方法
6 . 氮的氧化物是造成大气污染的主要物质,以乙烯(C2H4)作为还原剂的脱硝(NO)机理如图所示,下列说法正确的是
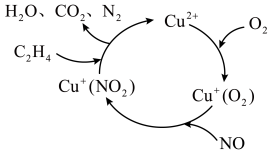

A.H2CO3的电离方程式为H2CO3 2H+ + 2H+ + |
| B.该机理图中,Cu2+、Cu+ (O2)和Cu+(NO2)均为催化剂 |
C.Cu2+与水反应的离子方程式为Cu2++2H2O Cu(OH)2↓+2H+ Cu(OH)2↓+2H+ |
| D.该反应的化学方程式可能为C2H4+2NO+2O2=2H2O+2CO2+N2 |
您最近一年使用:0次
2024-01-14更新
|
97次组卷
|
3卷引用:河北省石家庄市河北师范大学附属中学2023-2024学年高二上学期12月月考化学试题
名校
7 . 合成氨工业中,原料气( 、
、 及少量CO、
及少量CO、 的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。以下说法错误的是
。以下说法错误的是
 、
、 及少量CO、
及少量CO、 的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。以下说法错误的是
。以下说法错误的是A.原料气中 的体积分数越大,平衡混合物中氨的体积分数也越大 的体积分数越大,平衡混合物中氨的体积分数也越大 |
| B.杂质有可能引发催化剂中毒 |
| C.使用催化剂可降低反应的活化能,大大提高生产效率 |
| D.铜氨液再生的适宜条件是高温低压 |
您最近一年使用:0次
名校
8 . 我国学者结合实验与计算机模拟结果,研究了CO2与H2在TiO2/Cu催化剂表面生成CH3OH和H2O的部分反应历程(包含反应①~⑤,共5个基元反应)如图所示,其中吸附在催化剂表面的物种用*标注.

下列说法错误的是

下列说法错误的是
| A.反应①为放热反应 | B.反应②的活化能Ea=0.68eV |
| C.反应④可表示为HO*+H*=H2O* | D.反应⑤为H2O从催化剂表面脱附的过程 |
您最近一年使用:0次
2023-11-10更新
|
405次组卷
|
4卷引用:河北省石家庄市第四十二中学2023-2024学年高二上学期期中考试化学试题
河北省石家庄市第四十二中学2023-2024学年高二上学期期中考试化学试题河北省定州市2023-2024学年高二上学期11月期中考试化学试题新疆乌鲁木齐市第九中学2023-2024学年高三上学期11月月考化学试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
名校
解题方法
9 . 甲醛有毒,被世界卫生组织列为一类致癌物。但甲醛是重要的工业原料,在化工、纺织、医疗等领域有广泛应用。
I.回收利用CO2是一种减弱温室效应的有效途径。科学家研究发现可利用回收的CO2与H2反应制备甲醛。
已知:①甲醛的燃烧热为524kJ•mol-1
②H2的燃烧热为285.8 kJ•mol-1
③H2O(g)=H2O(l) △H=-44kJ•mol-1
(1)CO2与H2制备甲醛的反应:CO2(g)+2H2(g)=HCHO(g)+H2O(g) △H=______ 。
(2)在2L恒容密闭容器中通入0.2molCO2和0.4molH2,在三种不同条件下发生(1)中反应,测得CO2的转化率与时间的关系如图所示,曲线X对应温度下反应的平衡常数K=_______ ,由曲线Y到曲线X采取的措施可能是____ 由细线Z到曲线X采取的措施可能是_______ 。
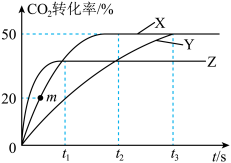
(3)反应速率v(正)=k(正)c(CO2)c2(H2),v(逆)=k(逆)c(CH2O)c(H2O),k(正)、k(逆)分别为正、逆向反应速率常数,计算m点 =
=______ 。
II.甲醇直接脱氢是工业上合成甲醛的一种新方法,该法得到无水甲醛的同时有到副产品氢气。
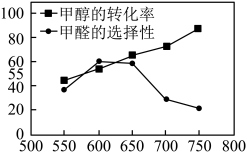
(4)在一个2L恒容密闭容器中投入1molCH3OH(g),在催化剂作用下发生反应:CH3OH(g)=HCHO(g)+H2(g) △H>0,同时存在副反应:CH3OH(g)=CO(g)+2H2(g) △H>0。20min后,测得甲醇的转化率与甲醛的选择性分别与温度的关系如图所示。温度高于650℃,甲醇的转化率升高,甲醛的产率_____ ,原因可能是________ 。
I.回收利用CO2是一种减弱温室效应的有效途径。科学家研究发现可利用回收的CO2与H2反应制备甲醛。
已知:①甲醛的燃烧热为524kJ•mol-1
②H2的燃烧热为285.8 kJ•mol-1
③H2O(g)=H2O(l) △H=-44kJ•mol-1
(1)CO2与H2制备甲醛的反应:CO2(g)+2H2(g)=HCHO(g)+H2O(g) △H=
(2)在2L恒容密闭容器中通入0.2molCO2和0.4molH2,在三种不同条件下发生(1)中反应,测得CO2的转化率与时间的关系如图所示,曲线X对应温度下反应的平衡常数K=

(3)反应速率v(正)=k(正)c(CO2)c2(H2),v(逆)=k(逆)c(CH2O)c(H2O),k(正)、k(逆)分别为正、逆向反应速率常数,计算m点
 =
=II.甲醇直接脱氢是工业上合成甲醛的一种新方法,该法得到无水甲醛的同时有到副产品氢气。
(4)在一个2L恒容密闭容器中投入1molCH3OH(g),在催化剂作用下发生反应:CH3OH(g)=HCHO(g)+H2(g) △H>0,同时存在副反应:CH3OH(g)=CO(g)+2H2(g) △H>0。20min后,测得甲醇的转化率与甲醛的选择性分别与温度的关系如图所示。温度高于650℃,甲醇的转化率升高,甲醛的产率

您最近一年使用:0次
名校
10 . 通过2NO(g)+2CO(g) 2CO2(g)+N2(g) △H=-746.5kJ•mol-1催化还原的方法,可将汽车尾气中有害气体转化为无害气体。下列说法正确的是
2CO2(g)+N2(g) △H=-746.5kJ•mol-1催化还原的方法,可将汽车尾气中有害气体转化为无害气体。下列说法正确的是
 2CO2(g)+N2(g) △H=-746.5kJ•mol-1催化还原的方法,可将汽车尾气中有害气体转化为无害气体。下列说法正确的是
2CO2(g)+N2(g) △H=-746.5kJ•mol-1催化还原的方法,可将汽车尾气中有害气体转化为无害气体。下列说法正确的是| A.该反应在任何条件下都能自发进行 |
B.反应的平衡常数可表示为K=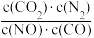 |
C.其它条件不变,增大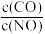 的值,NO的转化率下降 的值,NO的转化率下降 |
| D.使用高效的催化剂可以降低反应的焓变 |
您最近一年使用:0次



