22-23高一下·上海·期末
1 . 工业合成氨
(1)合成氨的适宜条件探究:N2(g)+3H2(g) 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)
∴合成氨的合理生产条件:① 使用___________ 为催化剂 ②一定程度的加压 ③温度控制在催化剂的活性温度(500℃) ④及时分离___________
(1)合成氨的适宜条件探究:N2(g)+3H2(g)
 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)| 反应条件 | 对化学反应速率的影响 | 对平衡混合物中NH3含量的影响 | 化学反应速率与化学平衡综合考虑 |
| 增大压强 | 影响一致,应 | ||
| 升高温度 | 影响 | ||
| 使用催化剂 | 用合适催化剂有利于加快反应速率 | ||
| 增加反应物浓度 | 平衡向 | 影响一致应 |
您最近一年使用:0次
2023·天津河东·一模
解题方法
2 . 光催化固氮合成氨的机理如图所示,下列说法不正确的是
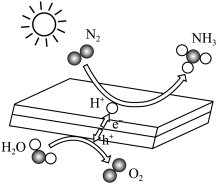

| A.NH3分子是极性分子 |
| B.此反应中氮气做氧化剂 |
| C.无论使用哪种催化剂,同一个反应的活化能是不变的 |
D.此反应的化学反应方程式是:2N2+6H2O 4NH3+3O2 4NH3+3O2 |
您最近一年使用:0次
21-22高一下·湖南长沙·阶段练习
名校
解题方法
3 . 纳米级Fe3O4可用于以太阳能为热源分解水制H2,过程如图所示。下列说法中,不正确的是
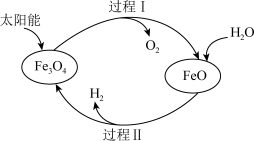

| A.Fe3O4中Fe元素的化合价为+2、+3 | B.过程Ⅱ的反应:2H2O=2H2↑+O2↑ |
| C.整个过程实现了太阳能向化学能的转化 | D.Fe3O4为整个过程的催化剂 |
您最近一年使用:0次
2022-09-07更新
|
208次组卷
|
3卷引用:专题03 化学反应速率与化学平衡(知识串讲+专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)
(已下线)专题03 化学反应速率与化学平衡(知识串讲+专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)湖南省长沙市A佳教育联盟2021-2022学年高一下学期3月联考化学试题上海市敬业中学2022-2023学年高二上学期10月月考(等级考)化学试题
名校
解题方法
4 . 某化学课外小组的同学准备通过实验探究,加深对化学反应速率和化学反应限度的认识。
实验一:探究温度和浓度对反应速率的影响
实验原理及方案:在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生反应生成碘,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。
(1)上述表格中:V1=____ mL,V2=____ mL。
实验二:探究KI和FeCl3混合时生成KCl、I2和FeCl2的反应存在一定的限度。
实验步骤:
i.向5mL,0.01mol/LKI溶液中滴加5~6滴0.01mol/LFeCl3溶液,充分反应后,将所得溶液分成甲、乙两等份;
ii.向甲中滴加CCl4,充分振荡;
iii.向乙中滴加KSCN。
请回答下列问题:
(2)KI和FeCl3在溶液中反应的离子方程式为:2I-+2Fe3+ I2(溶液)+2Fe2+,写出该反应的平衡常数K的表达式
I2(溶液)+2Fe2+,写出该反应的平衡常数K的表达式___ 。
(3)步骤和iii中的实验现象说明KI和FeCl3混合时生成KCl、I2和FeCl2的反应存在一定的限度,则步骤ii中的实验现象是____ ,且步骤iii中的实验现象是____ 。
实验三:对铝片与相同H+浓度的盐酸和硫酸在同温同压下反应时,铝和盐酸反应速率更快的原因探究。填写下列空白:
①该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因I:Cl-对反应具有促进作用,而SO 对反应没有影响;
对反应没有影响;
原因II:Cl-对反应没有影响,而SO 对反应具有阻碍作用;
对反应具有阻碍作用;
(4)原因III:____ ;
原因IV:Cl-、SO 均对反应具有促进作用,但Cl-影响更大;
均对反应具有促进作用,但Cl-影响更大;
(5)原因V:_____ 。
②该同学设计并进行了两组实验,即得出了正确结论。他取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
a.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
(6)若原因I是正确的,则应观察到的现象是:实验a中____ ,实验b中____ 。
实验一:探究温度和浓度对反应速率的影响
实验原理及方案:在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生反应生成碘,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。
| 实验序号 | 0.01mol/LKIO3酸性溶液(含淀粉)的体积/mL | 0.01mol/LNa2SO3溶液的体积/mL | 水的体积/mL | 实验温度/℃ | 出现蓝色的时间/s |
| ① | 5 | 5 | V1 | 0 | |
| ② | 5 | 5 | 40 | 25 | |
| ③ | 5 | V2 | 35 | 25 |
实验二:探究KI和FeCl3混合时生成KCl、I2和FeCl2的反应存在一定的限度。
实验步骤:
i.向5mL,0.01mol/LKI溶液中滴加5~6滴0.01mol/LFeCl3溶液,充分反应后,将所得溶液分成甲、乙两等份;
ii.向甲中滴加CCl4,充分振荡;
iii.向乙中滴加KSCN。
请回答下列问题:
(2)KI和FeCl3在溶液中反应的离子方程式为:2I-+2Fe3+
 I2(溶液)+2Fe2+,写出该反应的平衡常数K的表达式
I2(溶液)+2Fe2+,写出该反应的平衡常数K的表达式(3)步骤和iii中的实验现象说明KI和FeCl3混合时生成KCl、I2和FeCl2的反应存在一定的限度,则步骤ii中的实验现象是
实验三:对铝片与相同H+浓度的盐酸和硫酸在同温同压下反应时,铝和盐酸反应速率更快的原因探究。填写下列空白:
①该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因I:Cl-对反应具有促进作用,而SO
 对反应没有影响;
对反应没有影响;原因II:Cl-对反应没有影响,而SO
 对反应具有阻碍作用;
对反应具有阻碍作用;(4)原因III:
原因IV:Cl-、SO
 均对反应具有促进作用,但Cl-影响更大;
均对反应具有促进作用,但Cl-影响更大;(5)原因V:
②该同学设计并进行了两组实验,即得出了正确结论。他取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
a.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
(6)若原因I是正确的,则应观察到的现象是:实验a中
您最近一年使用:0次
名校
5 . 肼(N2H4)是一种应用广泛的化工原料。工业上先合成氨气,再进一步制备肼。完成下列填空:
(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同):

则生产中适宜选择的催化剂是_______ (填“A”或“B”或“C”)。
(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”):
(3)在一体积为10L的密闭容器中充入了280gN2,100gH2,反应半小时后,测得有34gNH3生成,则用H2表示该反应的速率为_______ mol·L-1·min-1,此时,氮气的转化率为_______ 。
(4)下列判断可以作为该反应达到平衡的标志的是_______。
(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同):

则生产中适宜选择的催化剂是
(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”):
| 反应速率 | 平衡常数K | 氨的体积分数 | |
| 变化情况 |
(3)在一体积为10L的密闭容器中充入了280gN2,100gH2,反应半小时后,测得有34gNH3生成,则用H2表示该反应的速率为
(4)下列判断可以作为该反应达到平衡的标志的是_______。
| A.单位时间内每消耗1摩尔氮气的同时消耗3摩尔氢气 |
| B.混合气体的平均分子量不再发生变化 |
| C.混合气体的密度保持不变 |
| D.体系的温度不再变化 |
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
6 . “漂尘”是物质燃烧时产生的粒状漂浮物,颗粒很小(直径小于10-7m),不易沉降(可漂浮数小时甚至数年),它与空气中的SO2接触,SO2会部分被氧化成SO3,“漂尘”所起的主要作用是
| A.催化剂 | B.还原剂 | C.吸附剂 | D.氧化剂 |
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
7 . 对于反应2SO2(g)+O2(g)  2SO3(g)(放热反应)已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是(O~t1:v正=v逆;t1时改变条件,t2时重新建立平衡)
2SO3(g)(放热反应)已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是(O~t1:v正=v逆;t1时改变条件,t2时重新建立平衡)
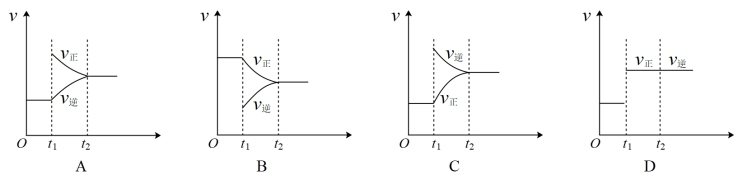
 2SO3(g)(放热反应)已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是(O~t1:v正=v逆;t1时改变条件,t2时重新建立平衡)
2SO3(g)(放热反应)已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是(O~t1:v正=v逆;t1时改变条件,t2时重新建立平衡)
| A.图A是增加氧气的浓度 | B.图B是减小SO3浓度 |
| C.图C是升高温度 | D.图D是加入催化剂 |
您最近一年使用:0次
名校
8 . 2NO(g)+O2(g)⇌2NO2(g)体系中能使该反应的反应速率增大,且平衡向正反应方向移动的是
| A.及时分离出NO2气体 | B.扩大容器体积 |
| C.增大O2的浓度 | D.选择高效催化剂 |
您最近一年使用:0次
2022-04-15更新
|
581次组卷
|
4卷引用:上海市光明中学2021-2022学年高一下学期期中化学试题
名校
9 . 如图为二氧化硫与氧气反应的速率(ν)与时间(t)的关系,判断在t1时刻曲线发生变化的原因是


| A.增大O2的浓度 | B.扩大容器体积 | C.升高温度 | D.加入催化剂 |
您最近一年使用:0次
2022-04-14更新
|
100次组卷
|
2卷引用:上海市南洋模范中学2021-2022学年高一下学期3月考化学试题
2022高一·上海·专题练习
10 . 为探究催化剂对过氧化氢分解反应速率的影响,某兴趣小组设计如图装置。实验时,通过胶头滴管向容器中各滴入5滴溶液后,每隔10 s观测注射器中气体体积并进行比较。

请回答:
(1)仪器A的名称是___________ 。
(2)若甲装置在相同时间内收集到气体体积大于乙装置,能否推测Fe3+对H2O2分解的催化效果比Cu2+的好?___________ (填“能”或“不能”),请说明理由___________ 。

请回答:
(1)仪器A的名称是
(2)若甲装置在相同时间内收集到气体体积大于乙装置,能否推测Fe3+对H2O2分解的催化效果比Cu2+的好?
您最近一年使用:0次



