名校
1 . 金表面发生分解反应: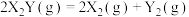 ,其速率方程为
,其速率方程为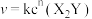 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
下列叙述不正确的是
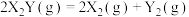 ,其速率方程为
,其速率方程为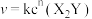 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:t/min c/(mol·L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
| X2Y | 0.100 | 0.040 | 0.020 | 0 | ||
| X2 | 0 | 0.020 | ||||
| Y2 | 0 | 0.020 |
| A.提高反应物浓度,反应速率不变 |
B. |
C.其他条件不变,若 起始浓度为 起始浓度为 ,则反应物浓度减半所需时间为 ,则反应物浓度减半所需时间为 |
D.当升高温度,反应 时 时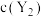 可能小于 可能小于 |
您最近一年使用:0次
名校
解题方法
2 . 液相催化还原法可去除水体中的 ,其分步催化还原机理如图1所示。其他条件相同,不同
,其分步催化还原机理如图1所示。其他条件相同,不同 时,反应1小时后
时,反应1小时后 化率和不同产物在总还原产物中所占的物质的量的百分比如图2所示。
化率和不同产物在总还原产物中所占的物质的量的百分比如图2所示。_____________ ,还原剂是_____________ 。
(2)反应ⅰ的离子方程式是_____________________________________ 。
(3)研究表明, 在
在 表面与
表面与 竞争吸附,会降低
竞争吸附,会降低 吸附
吸附 的能力,但对
的能力,但对 吸附
吸附 的能力影响不大。
的能力影响不大。
①随 增大,
增大, 和氨态氮在还原产物中的百分比均减小,原因是
和氨态氮在还原产物中的百分比均减小,原因是_________________________ ,导致反应ⅱ的化学反应速率降低。
②随 减小,还原产物中
减小,还原产物中 的变化趋势是
的变化趋势是_____________________________ ,说明 表面吸附的
表面吸附的 和
和 的个数比变大,对反应
的个数比变大,对反应_________________________ (用离子方程式表示)更有利。
(4)分析图2,使用该催化剂,通过调节溶液 ,可将
,可将 可能多地转化为
可能多地转化为 。其具体方法是
。其具体方法是_____________ 。
 ,其分步催化还原机理如图1所示。其他条件相同,不同
,其分步催化还原机理如图1所示。其他条件相同,不同 时,反应1小时后
时,反应1小时后 化率和不同产物在总还原产物中所占的物质的量的百分比如图2所示。
化率和不同产物在总还原产物中所占的物质的量的百分比如图2所示。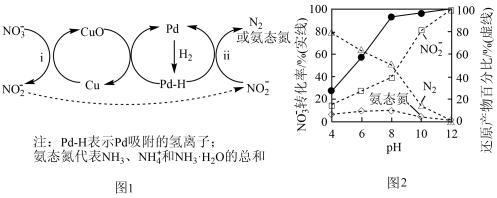
(2)反应ⅰ的离子方程式是
(3)研究表明,
 在
在 表面与
表面与 竞争吸附,会降低
竞争吸附,会降低 吸附
吸附 的能力,但对
的能力,但对 吸附
吸附 的能力影响不大。
的能力影响不大。①随
 增大,
增大, 和氨态氮在还原产物中的百分比均减小,原因是
和氨态氮在还原产物中的百分比均减小,原因是②随
 减小,还原产物中
减小,还原产物中 的变化趋势是
的变化趋势是 表面吸附的
表面吸附的 和
和 的个数比变大,对反应
的个数比变大,对反应(4)分析图2,使用该催化剂,通过调节溶液
 ,可将
,可将 可能多地转化为
可能多地转化为 。其具体方法是
。其具体方法是
您最近一年使用:0次
名校
3 . 天然气中含有少量 等气体,开采应用受限。T.F菌在酸性
等气体,开采应用受限。T.F菌在酸性 溶液中可实现天然气的催化脱硫,其原理如图所示,总反应方程式为
溶液中可实现天然气的催化脱硫,其原理如图所示,总反应方程式为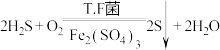 。下列说法错误的是
。下列说法错误的是
 等气体,开采应用受限。T.F菌在酸性
等气体,开采应用受限。T.F菌在酸性 溶液中可实现天然气的催化脱硫,其原理如图所示,总反应方程式为
溶液中可实现天然气的催化脱硫,其原理如图所示,总反应方程式为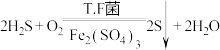 。下列说法错误的是
。下列说法错误的是
| A.大量开采天然气会加剧温室效应 |
| B.脱硫过程的总反应属于置换反应 |
C.脱硫过程中 的质量和化学性质不变 的质量和化学性质不变 |
| D.该反应原理可以应用于高温条件下脱硫 |
您最近一年使用:0次
2023-11-16更新
|
208次组卷
|
3卷引用:湖北省宜昌市协作体2023-2024学年高一上学期期中考试化学试题
名校
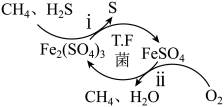
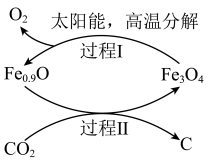
4 . 利用缺铁氧化物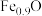 可实现
可实现 的综合利用,构建低碳环保社会,下列说法错误的是
的综合利用,构建低碳环保社会,下列说法错误的是
 可实现
可实现 的综合利用,构建低碳环保社会,下列说法错误的是
的综合利用,构建低碳环保社会,下列说法错误的是
A.过程Ⅰ发生反应的化学方程式为 |
B.过程Ⅱ中 是氧化产物 是氧化产物 |
| C.在整个过程中Fe0.9O是催化剂 |
D.整个过程的总反应为 |
您最近一年使用:0次
2023-10-26更新
|
195次组卷
|
2卷引用:湖北省襄阳市第六中学2023-2024学年高一上学期10月月考化学试题
名校
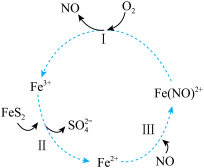
5 . 在酸性条件下,黄铁矿( )催化氧化的反应方程式为
)催化氧化的反应方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是
 )催化氧化的反应方程式为
)催化氧化的反应方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是
| A.在酸性条件下,黄铁矿催化氧化中NO作催化剂 |
| B.整个反应中,被氧化与被还原的元素的质量之比为7∶4 |
C.反应I的离子方程式为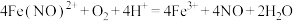 |
D.反应II的离子方程式为14Fe3++FeS2+8H2O=2 +15Fe2++16H+ +15Fe2++16H+ |
您最近一年使用:0次
解题方法
6 . 据文献显示: 催化合成DMC的一种反应机理如图所示。下列叙述正确的是
催化合成DMC的一种反应机理如图所示。下列叙述正确的是

 催化合成DMC的一种反应机理如图所示。下列叙述正确的是
催化合成DMC的一种反应机理如图所示。下列叙述正确的是
| A.①②的反应类型不同 |
B. 能提高反应物的平衡转化率 能提高反应物的平衡转化率 |
| C.DMC是乙酸的同系物 |
| D.上述合成DMC的反应属于真正的“绿色化学”,实现了原子利用率100% |
您最近一年使用:0次
名校
解题方法
7 . 过氧化氢(H2O2)是常用的绿色氧化剂。某化学兴趣小组查阅了H2O2的相关信息,并针对它的某些性质进行了探究,具体如下:H2O2可以通过H2和O2在某催化剂表面直接反应合成,具体原理如下图所示:

(1)采用同位素示踪法研究催化剂中H+的作用:将H2用D2(2H2)代替再进行实验。催化剂中氢离子参与反应的证据是生成的产物中有H2O2或_______ 粒子(填化学式)。
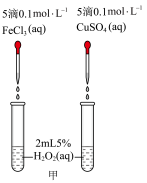
II.H2O2不稳定,在Fe3+、Cu2+等粒子的催化下会很快分解并放出热量。为了比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如下实验。
(2)定性分析:通过观察甲装置两支试管中_______ 的现象,得出关于FeCl3和CuSO4催化效果的结论。某同学认为此方案还需要进一步控制变量,提出可将试剂CuSO4更换为_______ (填化学式)。
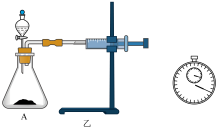
(3)定量测定:用乙装置进行定量实验。实验时组装好装置乙,关闭分液漏斗的活塞,将注射器活塞向外拉出一段距离后松开,观察活塞是否回到原来的位置。该操作的实验目的是_______ 。若反应30s后注射器中收集到气体的体积为VmL(标准状况),则锥形瓶A中实际产生气体的体积_______ VmL(填“>”、“<”或“=”)。
III.H2O2既有氧化性,又有还原性。
(4)H2O2可以氧化废水中的CN—,Cu2+可催化该反应。已知H2O2与CN—反应会生成参与大气循环的无毒气体。氰化氢(HCN)是一种易挥发的弱酸,有剧毒,对环境危害很大。
①H2O2与CN-的反应不能在酸性溶液中进行,原因是_______ ,反应生成气体的化学式为_______ 。
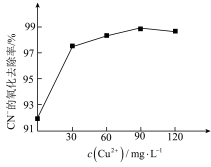
②一定条件下,测得CN-的氧化去除率随溶液中c(Cu2+)的变化如下图所示。c(Cu2+)过多时,CN-的氧化去除率有所下降,原因是_______ 。
(5)取少量84消毒液(有效成分为NaClO)于试管中,滴加H2O2溶液,产生大量无色气体。写出发生反应的化学方程式_______ 。

(1)采用同位素示踪法研究催化剂中H+的作用:将H2用D2(2H2)代替再进行实验。催化剂中氢离子参与反应的证据是生成的产物中有H2O2或
II.H2O2不稳定,在Fe3+、Cu2+等粒子的催化下会很快分解并放出热量。为了比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如下实验。
(2)定性分析:通过观察甲装置两支试管中

(3)定量测定:用乙装置进行定量实验。实验时组装好装置乙,关闭分液漏斗的活塞,将注射器活塞向外拉出一段距离后松开,观察活塞是否回到原来的位置。该操作的实验目的是

III.H2O2既有氧化性,又有还原性。
(4)H2O2可以氧化废水中的CN—,Cu2+可催化该反应。已知H2O2与CN—反应会生成参与大气循环的无毒气体。氰化氢(HCN)是一种易挥发的弱酸,有剧毒,对环境危害很大。
①H2O2与CN-的反应不能在酸性溶液中进行,原因是
②一定条件下,测得CN-的氧化去除率随溶液中c(Cu2+)的变化如下图所示。c(Cu2+)过多时,CN-的氧化去除率有所下降,原因是

(5)取少量84消毒液(有效成分为NaClO)于试管中,滴加H2O2溶液,产生大量无色气体。写出发生反应的化学方程式
您最近一年使用:0次
名校
8 . 根据要求回答问题:
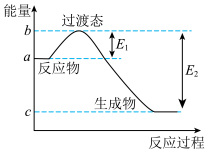
(1)如图是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,活化能E1的变化是_____ (填“增大”“减小”或“不变”,下同),ΔH的变化是_____ 。图中最稳定的是_____ (填“反应物”“过渡态”或“生成物”)。
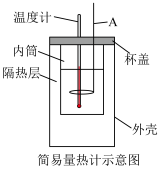
(2)50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热(设溶液的密度均为1g•cm-3,反应后溶液的比热容c=4.18J•g-1•℃-1)。回答下列问题:
从实验装置上看,图中仪器A的名称是_____ ,隔热层的作用是_____ 。根据表中数据,结合题干信息,请写出生成1molH2O的热化学方程式_____ (保留3位有效数字)。
(3)生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的1.2~2.0万倍,在大气中的寿命可长达740年之久,表中是几种化学键的键能:
写出N2(g)与F2(g)反应合成NF3(g)的热化学方程式_____ 。
(4)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。这两步反应的能量变化如图:
。这两步反应的能量变化如图:
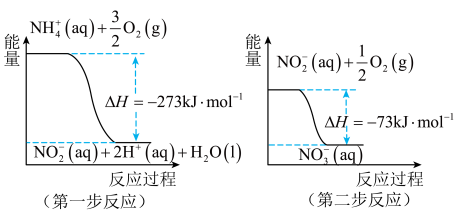
第二步反应是_____ (填“放热”或“吸热”)反应。1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_____ 。
(1)如图是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,活化能E1的变化是

(2)50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热(设溶液的密度均为1g•cm-3,反应后溶液的比热容c=4.18J•g-1•℃-1)。回答下列问题:
 | 实验次数 | 反应物的温度/℃ | 反应前体系的温度 | 反应后体系的温度 | 温度差 | |
| 盐酸 | NaOH溶液 | t1/℃ | t2/℃ | (t2-t1)/℃ | ||
| 1 | 25.0 | 25.2 | 25.1 | 28.5 | 3.4 | |
| 2 | 24.9 | 25.1 | 25.0 | 28.3 | 3.3 | |
| 3 | 25.6 | 25.4 | 25.5 | 29.0 | 3.5 | |
(3)生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的1.2~2.0万倍,在大气中的寿命可长达740年之久,表中是几种化学键的键能:
| 化学键 | N≡N | F-F | N-F |
| 键能/kJ•mol-1 | 941.7 | 154.8 | 283.0 |
(4)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。这两步反应的能量变化如图:
。这两步反应的能量变化如图:
第二步反应是
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是
您最近一年使用:0次
名校
解题方法
9 . 已知H2O2(aq)分解为H2O(l)和O2(g)的能量变化如图曲线A所示,若在H2O2溶液中加入少量KI,则H2O2的分解过程可表示为:①H2O2+I-=H2O+IO-,②H2O2+IO-=H2O+O2+I-,其能量变化如图曲线B所示。下列有关说法不正确 的是
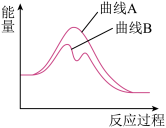
| A.上述反应①为吸热反应,反应②为放热反应 |
| B.2molH2O2(aq)具有的能量大于2molH2O(l)和1molO2(g)具有的总能量 |
| C.I-在H2O2分解过程中起到催化剂作用 |
| D.从曲线B可以看出,加入KI减少了H2O2(aq)分解为H2O(l)和O2(g)的能量变化 |
您最近一年使用:0次
2023-04-21更新
|
498次组卷
|
6卷引用:湖北省沙市中学2022-2023学年高一下学期5月月考化学试题
湖北省沙市中学2022-2023学年高一下学期5月月考化学试题浙江省9+1高中联盟2022-2023学年高一下学期4月期中化学试题(已下线)【2023】【高一下】【期中考】【9+1】【高中化学】【霍钰涵收集】(已下线)【2023】【高一下】【期中考】【西子实验】【高中化学】【张太顺收集】贵州省遵义市仁怀市高中教育联盟2022-2023学年高一下学期5月期中考试化学试题浙江省宁波市北仑中学2023-2024学年高一下学期期中考试化学试题
10 . 化学反应速率的调控在工农业生产和日常生活中有重要作用,下列说法正确的是
| A.在化学工业中,使用催化剂一定能增大化学产率 |
| B.月饼等包装中加入铁粉,能延长月饼的保质期 |
| C.将肉类等食品进行低温冷藏,能使其永远不会腐败变质 |
| D.在室外,夏天面粉发酵速度与冬天面粉发酵速度相差不大 |
您最近一年使用:0次



