名校
解题方法
1 . 在相同条件下通入一定量X,研究催化剂对反应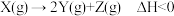 的影响,各物质浓度c随反应时间t的部分变化曲线如图。下列说法正确的是
的影响,各物质浓度c随反应时间t的部分变化曲线如图。下列说法正确的是
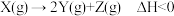 的影响,各物质浓度c随反应时间t的部分变化曲线如图。下列说法正确的是
的影响,各物质浓度c随反应时间t的部分变化曲线如图。下列说法正确的是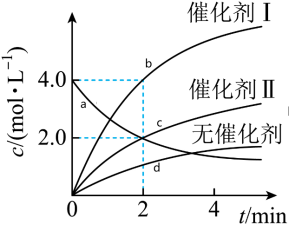
| A.无催化剂时,反应不能进行 |
| B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低 |
C.使用催化剂Ⅰ, 时, 时,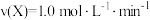 |
| D.c曲线可表示使用催化剂I时Z的浓度随t的变化 |
您最近一年使用:0次
2024-03-31更新
|
543次组卷
|
3卷引用:广东省深圳市高级中学2023-2024学年高一下学期4月期中考试化学试题
广东省深圳市高级中学2023-2024学年高一下学期4月期中考试化学试题广东省广州市天河区普通高中2023-2024学年高三毕业班综合测试(二)化学试题(已下线)化学(广东卷03)-2024年高考押题预测卷
名校
2 . 在处理汽车尾气的三元催化剂中,Rh的主要作用是消除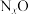 ,Pd的主要作用是消除CO,部分催化机理及能量变化如图所示。下列说法不正确的是
,Pd的主要作用是消除CO,部分催化机理及能量变化如图所示。下列说法不正确的是
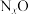 ,Pd的主要作用是消除CO,部分催化机理及能量变化如图所示。下列说法不正确的是
,Pd的主要作用是消除CO,部分催化机理及能量变化如图所示。下列说法不正确的是
| A.在NO和CO的整个反应过程中步骤Ⅲ是决速步骤 |
| B.反应进行的三步分别是放热反应、放热反应和吸热反应 |
C.第一步反应: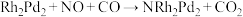 |
D.CO能促进NO转化成 |
您最近一年使用:0次
2024-03-21更新
|
395次组卷
|
2卷引用:广东省茂名市高州中学2023-2024学年高一下学期期中考试化学试题
3 .  是一种常见试剂,在实验室、工业生产上有广泛用途。
是一种常见试剂,在实验室、工业生产上有广泛用途。
I. 不稳定、易分解,
不稳定、易分解, 等对其分解起催化作用,为比较
等对其分解起催化作用,为比较 和
和 对
对 分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
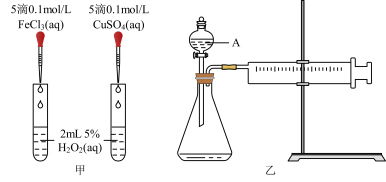
(1)若利用图甲装置,可通过观察___________ 现象,从而定性比较得出结论。
(2)有同学提出将 改为
改为___________  更为合理,其理由是
更为合理,其理由是___________ 。
(3)若利用乙实验可进行定量分析,实验时均以生成 气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是___________ 。
(4)如图为某小组研究的酸、碱对 分解的影响。该小组提出可以用
分解的影响。该小组提出可以用 固体与
固体与 溶液反应制
溶液反应制 ,反应的化学方程式为
,反应的化学方程式为___________ ,支持这一方案的理由是___________ 。
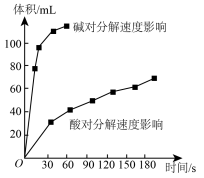
Ⅱ.实验室用 快速制氧气,其分解速率受多种因素影响。实验测得
快速制氧气,其分解速率受多种因素影响。实验测得 时不同条件下
时不同条件下 浓度随时间的变化如甲、乙、丙、丁四图所示:
浓度随时间的变化如甲、乙、丙、丁四图所示:
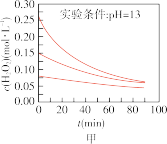
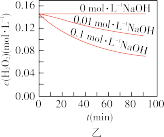

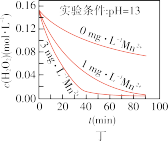
(5)下列说法正确的是:___________(填字母序号)
(6)催化剂 在反应中,改变了
在反应中,改变了___________ (填字母序号)
A.反应速率 B.反应限度 C.反应焓变 D.反应路径 E.反应活化能 F.活化分子百分数
 是一种常见试剂,在实验室、工业生产上有广泛用途。
是一种常见试剂,在实验室、工业生产上有广泛用途。I.
 不稳定、易分解,
不稳定、易分解, 等对其分解起催化作用,为比较
等对其分解起催化作用,为比较 和
和 对
对 分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
(1)若利用图甲装置,可通过观察
(2)有同学提出将
 改为
改为 更为合理,其理由是
更为合理,其理由是(3)若利用乙实验可进行定量分析,实验时均以生成
 气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是(4)如图为某小组研究的酸、碱对
 分解的影响。该小组提出可以用
分解的影响。该小组提出可以用 固体与
固体与 溶液反应制
溶液反应制 ,反应的化学方程式为
,反应的化学方程式为
Ⅱ.实验室用
 快速制氧气,其分解速率受多种因素影响。实验测得
快速制氧气,其分解速率受多种因素影响。实验测得 时不同条件下
时不同条件下 浓度随时间的变化如甲、乙、丙、丁四图所示:
浓度随时间的变化如甲、乙、丙、丁四图所示:



(5)下列说法正确的是:___________(填字母序号)
A.图甲表明,其他条件相同时, 浓度越小,其分解越慢 浓度越小,其分解越慢 |
B.图乙表明,其他条件相同时,溶液碱性越弱, 分解越快 分解越快 |
C.图丙表明,少量 存在时,溶液碱性越强, 存在时,溶液碱性越强, 分解越快 分解越快 |
D.图丁表明,碱性溶液中, 浓度越大,对 浓度越大,对 分解速率的影响越大 分解速率的影响越大 |
 在反应中,改变了
在反应中,改变了A.反应速率 B.反应限度 C.反应焓变 D.反应路径 E.反应活化能 F.活化分子百分数
您最近一年使用:0次
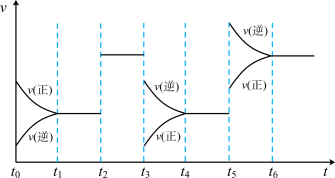
4 . 某密闭容器中发生如下反应: 。如图表示该反应的速率(v)随时间(t)变化的关系,
。如图表示该反应的速率(v)随时间(t)变化的关系,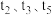 时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
 。如图表示该反应的速率(v)随时间(t)变化的关系,
。如图表示该反应的速率(v)随时间(t)变化的关系,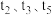 时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
A. 时加入催化剂 时加入催化剂 | B. 时降低了温度 时降低了温度 |
C. 时增大了压强 时增大了压强 | D. 时间内转化率一定最低 时间内转化率一定最低 |
您最近一年使用:0次
名校
5 . 研究气体的制备和性质有重要意义。某兴趣小组分别对 和
和 的制备进行研究,回答下列问题。
的制备进行研究,回答下列问题。
Ⅰ.氨气的制备

(1)盛装碱石灰的仪器的名称_______ 。
(2)实验室用加热 和
和 固体混合物制备氨气,化学方程式为
固体混合物制备氨气,化学方程式为_______ 。
(3)收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:
_______  尾气处理(按气流方向表示)。
尾气处理(按气流方向表示)。
(4)检验集气瓶已收集满氨的方法:用_______ ,靠近集气瓶口,若出现_______ ,则说明收集满。
Ⅱ. 分解制备
分解制备
(5)探究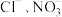 对
对 分解的影响
分解的影响
设计如图实验装置,在试管中分别添加了如下表的试剂和用量,再分别注入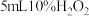 溶液,实验设计如下:
溶液,实验设计如下:

①实验结果显示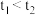 ,可得出的结论是:
,可得出的结论是:_______ (填化学式)更有利于 分解。
分解。
②甲同学查阅资料得知: 能加速
能加速 分解,
分解, 对
对 分解无影响。为排除
分解无影响。为排除 干扰,该同学再进行实验:向两份
干扰,该同学再进行实验:向两份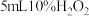 溶液中分别加入
溶液中分别加入 浓度均为
浓度均为_______  的
的_______ (填化学式)溶液和_______ (填化学式)溶液。 内,发现
内,发现 均几乎不分解。甲同学认为:在无
均几乎不分解。甲同学认为:在无 存在的情况下,
存在的情况下,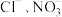 对
对 催化分解无影响。
催化分解无影响。
 和
和 的制备进行研究,回答下列问题。
的制备进行研究,回答下列问题。Ⅰ.氨气的制备

(1)盛装碱石灰的仪器的名称
(2)实验室用加热
 和
和 固体混合物制备氨气,化学方程式为
固体混合物制备氨气,化学方程式为(3)收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:

 尾气处理(按气流方向表示)。
尾气处理(按气流方向表示)。(4)检验集气瓶已收集满氨的方法:用
Ⅱ.
 分解制备
分解制备
(5)探究
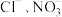 对
对 分解的影响
分解的影响设计如图实验装置,在试管中分别添加了如下表的试剂和用量,再分别注入
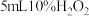 溶液,实验设计如下:
溶液,实验设计如下:
| 实验 | 添加试剂及用量 |  完全分解所需时间 完全分解所需时间 |
| 1 | 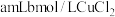 溶液 溶液 |  |
| 2 | 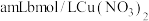 溶液 溶液 |  |
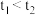 ,可得出的结论是:
,可得出的结论是: 分解。
分解。②甲同学查阅资料得知:
 能加速
能加速 分解,
分解, 对
对 分解无影响。为排除
分解无影响。为排除 干扰,该同学再进行实验:向两份
干扰,该同学再进行实验:向两份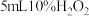 溶液中分别加入
溶液中分别加入 浓度均为
浓度均为 的
的 内,发现
内,发现 均几乎不分解。甲同学认为:在无
均几乎不分解。甲同学认为:在无 存在的情况下,
存在的情况下,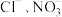 对
对 催化分解无影响。
催化分解无影响。
您最近一年使用:0次
2023-07-12更新
|
214次组卷
|
4卷引用:广东省中山市2022-2023学年高一下学期期末统一考试化学试题
6 . 下列措施能减慢化学反应速率的是
| A.用煤粉代替煤块燃烧 | B.把食物存放在冰箱里 |
| C.用柴火做饭时对灶膛鼓风 | D. 分解制 分解制 时,加少量 时,加少量 |
您最近一年使用:0次
7 . 厦门大学设计的具有高催化活性的Pt3FeCo-C纳米催化剂,可用于氨的二聚成肼反应:2NH3=N2H4+H2。下列说法错误的是
| A.Pt、Fe、Co均为过渡金属元素 |
| B.Pt3FeCo-C纳米催化剂可以加快该反应的反应速率 |
| C.每2molNH3完全反应时形成3mol非极性共价键 |
| D.液氨汽化为吸热过程,液氨可用作制冷剂 |
您最近一年使用:0次
2023-07-11更新
|
137次组卷
|
2卷引用:广东省清远市2022-2023学年高一下学期期末质量检测化学试题
名校
8 . 某学习小组对硝酸工业活性炭脱硝工艺进行探究。回答下列问题:
Ⅰ.硝酸工业产生的烟气中含有大量 ,工艺如图所示:
,工艺如图所示:
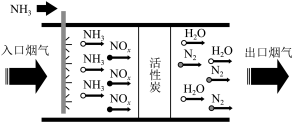
(1)该流程中活性炭是催化剂,加入催化剂的目的是___________ 。
(2)若要使 和
和 恰好充分反应。则反应混合物中
恰好充分反应。则反应混合物中 与
与 的体积比为
的体积比为___________ (用含x的式子表示)。
Ⅱ.某同学为了探究干燥条件下 与
与 的反应,设计如图所示实验装置进行实验。
的反应,设计如图所示实验装置进行实验。

(3)装置A为氨气的发生装置,应选用___________ (填“X”或“Y”)为此实验制备氨气的装置,相关反应的化学方程式为___________ 。
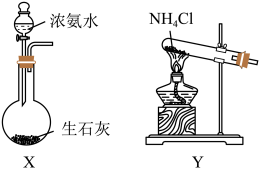
(4)该实验设计中存在缺陷,请写出解决方案:___________ 。
(5)装置D用于制备 气体。
气体。
①有同学推测反应过程中有可能产生NO,该同学做此推测的理由为___________ 。
②装置D中发生反应的实验现象为___________ 。
③ 能与碱液反应,故在拆装置之前,应该怎么操作
能与碱液反应,故在拆装置之前,应该怎么操作___________ 。
Ⅰ.硝酸工业产生的烟气中含有大量
 ,工艺如图所示:
,工艺如图所示:
(1)该流程中活性炭是催化剂,加入催化剂的目的是
(2)若要使
 和
和 恰好充分反应。则反应混合物中
恰好充分反应。则反应混合物中 与
与 的体积比为
的体积比为Ⅱ.某同学为了探究干燥条件下
 与
与 的反应,设计如图所示实验装置进行实验。
的反应,设计如图所示实验装置进行实验。
(3)装置A为氨气的发生装置,应选用

(4)该实验设计中存在缺陷,请写出解决方案:
(5)装置D用于制备
 气体。
气体。①有同学推测反应过程中有可能产生NO,该同学做此推测的理由为
②装置D中发生反应的实验现象为
③
 能与碱液反应,故在拆装置之前,应该怎么操作
能与碱液反应,故在拆装置之前,应该怎么操作
您最近一年使用:0次
解题方法
9 . Ⅰ. 已知某反应:A(g)+ 3B(g)  C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
(1)t1 h时,c(D) ___________ mol/L。
(2)0-t2 h内,以A的浓度变化表示反应的平均速率:v(A)___________ mol·L-1·h-1。
(3)下列能说明该反应达到平衡状态的是___________(填标号)。
Ⅱ.
(4)合成氨反应中,温度越低,氨的产率越高,但在生产中选定的反应温度为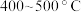 ,原因是
,原因是_________________________ 。
(5)合成氨反应可能的微观历程如图所示:
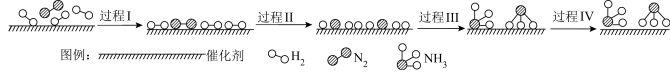
吸附在催化剂表面的物质用*标注。已知过程Ⅱ可以表示为 ,则过程Ⅲ可以表示为
,则过程Ⅲ可以表示为___________ 。
 C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。浓度/( ) ) | c(A) | c(B) | c(D) |
| 0 | 1.0 | 3.0 | 0 |
 h h | 0.8 | ||
 h h | 2.1 |
(2)0-t2 h内,以A的浓度变化表示反应的平均速率:v(A)
(3)下列能说明该反应达到平衡状态的是___________(填标号)。
| A.容器中的压强不随时间变化 | B.气体密度不再变化 |
| C.B和D的浓度之比为3:4 | D.消耗0.3 mol B的同时生成0.4 mol D |
Ⅱ.
(4)合成氨反应中,温度越低,氨的产率越高,但在生产中选定的反应温度为
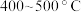 ,原因是
,原因是(5)合成氨反应可能的微观历程如图所示:

吸附在催化剂表面的物质用*标注。已知过程Ⅱ可以表示为
 ,则过程Ⅲ可以表示为
,则过程Ⅲ可以表示为
您最近一年使用:0次
名校
10 . Ⅰ.H2O2被称为绿色氧化剂,对其性质进行研究极其重要。某同学以H2O2分解为例,进行了以下实验:
(1)问题一:设计实验②和③的目的是:_______ 。
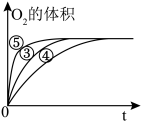
(2)问题二:实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出什么实验结论______ 。
Ⅱ.氮氧化物是主要的大气污染物之一,可用一氧化碳或活性炭还原氮氧化物,减少大气污染。
(3)一定条件下,用CO与NO反应生成CO2和N2,反应的化学方程式:2CO(g)+2NO(g) N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是
N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是______ (填标号)。
(4)两个10L的密闭容器中分别都加入活性炭(足量)和1.0molNO,发生反应:C(s)+2NO(g)  N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
①T1时,0~5min内,反应速率v(CO2)=______ mol•L-1•min-1。
②T2时,按表中数据,反应一定达到化学平衡状态的时间段是______ min~10min,此时,容器中CO2的物质的量浓度是______ mo/L。
③两容器中温度关系为T1______ T2(填“>”“<”或“=”)。
| 编号 | 反应物 | 催化剂 | 温度 |
| ① | 20mL2%H2O2溶液+2mLH2O | 无 | 20℃ |
| ② | 20mL5%H2O2溶液+2mLH2O | 无 | 20℃ |
| ③ | 20mL5%H2O2溶液+2mLH2O | 1g粉末状MnO2 | 20℃ |
| ④ | 20mL5%H2O2溶液+2mL1mol/LHCl溶液 | 1g粉末状MnO2 | 20℃ |
| ⑤ | 20mL5%H2O2溶液+2mLH2O | 1g粉末状MnO2 | 40℃ |
(2)问题二:实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出什么实验结论

Ⅱ.氮氧化物是主要的大气污染物之一,可用一氧化碳或活性炭还原氮氧化物,减少大气污染。
(3)一定条件下,用CO与NO反应生成CO2和N2,反应的化学方程式:2CO(g)+2NO(g)
 N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是
N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是| A.压缩容器体积 | B.降低温度 |
| C.使用合适催化剂 | D.恒温恒容充入稀有气体 |
 N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:| 物质的量/mol | 容器1(T1℃) | 容器2(T2℃) | |||||||
| 0 | 5min | 9min | 10min | 12min | 0 | 5min | 9min | 10min | |
| NO | 1.0 | 0.58 | 0.42 | 0.40 | 0.40 | 1.0 | 0.50 | 0.34 | 0.34 |
| N2 | 0 | 0.21 | 0.29 | 0.30 | 0.30 | 0 | 0.25 | 0.33 | 0.33 |
②T2时,按表中数据,反应一定达到化学平衡状态的时间段是
③两容器中温度关系为T1
您最近一年使用:0次
2023-05-23更新
|
180次组卷
|
4卷引用:广东省湛江市第二十一中学2022-2023学年高一下学期期中考试(选考)化学试题



