名校
解题方法
1 . 化学反应过程伴随有热量的变化。
(1)下列反应中属于放热反应的有___________ 。
①燃烧木炭取暖 ②C与H2O(g)反应制取水煤气 ③煅烧石灰石(主要成分是CaCO3)制生石灰 ④氯化铵晶体和Ba(OH)2·8H2O混合搅拌 ⑤食物因氧化而腐败 ⑥盐酸与NaOH溶液反应 ⑦镁与稀硫酸溶液反应
(2)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
①已知2CH4(g)=C2H4(g)+2H2(g),其中1mol C2H4中存在1mol C=C和4mol C-H键,已知每生成1 mol H2反应吸收83.5 kJ热量,则a=___________ 。
②已知5SO2(g)+2 (aq)+2H2O(l)=2Mn2+(aq)+5
(aq)+2H2O(l)=2Mn2+(aq)+5 (aq)+4H+(aq),每1 mol SO2参加反应放出热量m kJ,那么当放出的热量为n kJ时,该反应转移的电子数为
(aq)+4H+(aq),每1 mol SO2参加反应放出热量m kJ,那么当放出的热量为n kJ时,该反应转移的电子数为___________ 。(用含m、n的代数式表示,NA为阿伏加德罗常数的值。)
(3)反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:

①该反应为___________ (填“吸热”或“放热”)反应。
②若要使该反应的反应速率增大,下列措施可行的是___________ (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度 D.使用催化剂
(4)若将上述反应设计成原电池,则化学反应速率会___________ (填“变大”或“变小”)
铜为原电池某一极材料,则铜为:___________ (填“正”或“负”)极,该极上发生的电极反应为:___________ 。
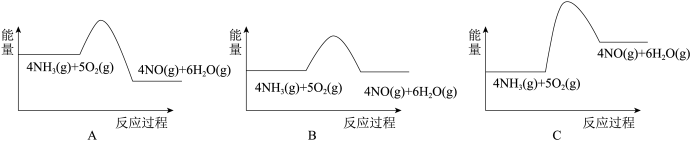
(5)关于氨气的催化氧化反应,先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达700 ℃以上。下列图示中,能够正确表示该反应过程中能量变化的是___________ (填序号),说明断键吸收的能量___________ (填“大于”“小于”或“等于”)成键放出的能量。
(1)下列反应中属于放热反应的有
①燃烧木炭取暖 ②C与H2O(g)反应制取水煤气 ③煅烧石灰石(主要成分是CaCO3)制生石灰 ④氯化铵晶体和Ba(OH)2·8H2O混合搅拌 ⑤食物因氧化而腐败 ⑥盐酸与NaOH溶液反应 ⑦镁与稀硫酸溶液反应
(2)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
②已知5SO2(g)+2
 (aq)+2H2O(l)=2Mn2+(aq)+5
(aq)+2H2O(l)=2Mn2+(aq)+5 (aq)+4H+(aq),每1 mol SO2参加反应放出热量m kJ,那么当放出的热量为n kJ时,该反应转移的电子数为
(aq)+4H+(aq),每1 mol SO2参加反应放出热量m kJ,那么当放出的热量为n kJ时,该反应转移的电子数为(3)反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:

①该反应为
②若要使该反应的反应速率增大,下列措施可行的是
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度 D.使用催化剂
(4)若将上述反应设计成原电池,则化学反应速率会
铜为原电池某一极材料,则铜为:
(5)关于氨气的催化氧化反应,先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达700 ℃以上。下列图示中,能够正确表示该反应过程中能量变化的是

您最近一年使用:0次
名校
解题方法
2 . 下列措施中,不能加快化学反应速率的是
| A.锌与稀硫酸反应,加入蒸馏水 |
| B.铝在氧气中燃烧,铝片换成铝粉 |
| C.大理石与盐酸反应,适当升高温度 |
| D.氯酸钾分解制氧气,添加少量二氧化锰 |
您最近一年使用:0次
2023-07-19更新
|
175次组卷
|
3卷引用:黑龙江省大庆铁人中学2022-2023学年高一下学期期末化学试题
名校
解题方法
3 .  捕获和转化可减少
捕获和转化可减少 排放,是人类助力自然界实现“碳循环”,其原理如图1所示。以
排放,是人类助力自然界实现“碳循环”,其原理如图1所示。以 为载气,将
为载气,将 以恒定流速通入反应器,单位时间内流出气体中各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
以恒定流速通入反应器,单位时间内流出气体中各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上检测到有积炭。
,在催化剂上检测到有积炭。
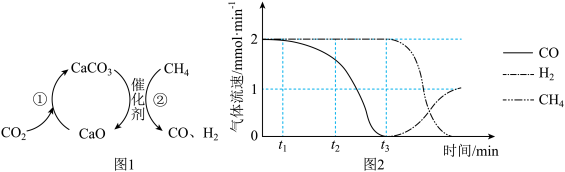
下列说法错误的是
 捕获和转化可减少
捕获和转化可减少 排放,是人类助力自然界实现“碳循环”,其原理如图1所示。以
排放,是人类助力自然界实现“碳循环”,其原理如图1所示。以 为载气,将
为载气,将 以恒定流速通入反应器,单位时间内流出气体中各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
以恒定流速通入反应器,单位时间内流出气体中各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上检测到有积炭。
,在催化剂上检测到有积炭。
下列说法错误的是
A.反应①为化合反应,CaO、 可循环利用 可循环利用 |
B.催化剂表面的积炭,有利于 捕获与转化 捕获与转化 |
C.0- 时段, 时段, ,推测该条件下发生反应②: ,推测该条件下发生反应②: |
D. 之后, 之后, 比 比 多,且检测到积炭,推测有副反应: 多,且检测到积炭,推测有副反应: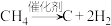 发生 发生 |
您最近一年使用:0次
4 . 回答下列问题:
(1)断开 键、
键、 键、
键、 键分别需要吸收的能量为436kJ、391kJ、946kJ,合成氨工业中生成
键分别需要吸收的能量为436kJ、391kJ、946kJ,合成氨工业中生成 时理论上能
时理论上能_______ (填“吸收”或“放出”)能量_______ kJ。
(2)我国科研人员研究发现合成氨的反应历程有多种,其中有一种反应历程如图所示(吸附在催化剂表面的物质用*表示)。下列说法错误的是_______ 。

a. 生成
生成 是通过多步还原反应生成的
是通过多步还原反应生成的
b.过程Ⅰ和Ⅲ中能量的变化相同
c.大量氨分子吸附在催化剂表面,将降低反应速率
(1)断开
 键、
键、 键、
键、 键分别需要吸收的能量为436kJ、391kJ、946kJ,合成氨工业中生成
键分别需要吸收的能量为436kJ、391kJ、946kJ,合成氨工业中生成 时理论上能
时理论上能(2)我国科研人员研究发现合成氨的反应历程有多种,其中有一种反应历程如图所示(吸附在催化剂表面的物质用*表示)。下列说法错误的是

a.
 生成
生成 是通过多步还原反应生成的
是通过多步还原反应生成的b.过程Ⅰ和Ⅲ中能量的变化相同
c.大量氨分子吸附在催化剂表面,将降低反应速率
您最近一年使用:0次
名校
5 . Ⅰ.H2O2被称为绿色氧化剂,对其性质进行研究极其重要。某同学以H2O2分解为例,进行了以下实验:
(1)问题一:设计实验②和③的目的是:_______ 。
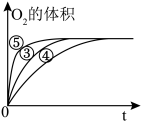
(2)问题二:实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出什么实验结论______ 。
Ⅱ.氮氧化物是主要的大气污染物之一,可用一氧化碳或活性炭还原氮氧化物,减少大气污染。
(3)一定条件下,用CO与NO反应生成CO2和N2,反应的化学方程式:2CO(g)+2NO(g) N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是
N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是______ (填标号)。
(4)两个10L的密闭容器中分别都加入活性炭(足量)和1.0molNO,发生反应:C(s)+2NO(g)  N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
①T1时,0~5min内,反应速率v(CO2)=______ mol•L-1•min-1。
②T2时,按表中数据,反应一定达到化学平衡状态的时间段是______ min~10min,此时,容器中CO2的物质的量浓度是______ mo/L。
③两容器中温度关系为T1______ T2(填“>”“<”或“=”)。
| 编号 | 反应物 | 催化剂 | 温度 |
| ① | 20mL2%H2O2溶液+2mLH2O | 无 | 20℃ |
| ② | 20mL5%H2O2溶液+2mLH2O | 无 | 20℃ |
| ③ | 20mL5%H2O2溶液+2mLH2O | 1g粉末状MnO2 | 20℃ |
| ④ | 20mL5%H2O2溶液+2mL1mol/LHCl溶液 | 1g粉末状MnO2 | 20℃ |
| ⑤ | 20mL5%H2O2溶液+2mLH2O | 1g粉末状MnO2 | 40℃ |
(2)问题二:实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出什么实验结论

Ⅱ.氮氧化物是主要的大气污染物之一,可用一氧化碳或活性炭还原氮氧化物,减少大气污染。
(3)一定条件下,用CO与NO反应生成CO2和N2,反应的化学方程式:2CO(g)+2NO(g)
 N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是
N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是| A.压缩容器体积 | B.降低温度 |
| C.使用合适催化剂 | D.恒温恒容充入稀有气体 |
 N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:| 物质的量/mol | 容器1(T1℃) | 容器2(T2℃) | |||||||
| 0 | 5min | 9min | 10min | 12min | 0 | 5min | 9min | 10min | |
| NO | 1.0 | 0.58 | 0.42 | 0.40 | 0.40 | 1.0 | 0.50 | 0.34 | 0.34 |
| N2 | 0 | 0.21 | 0.29 | 0.30 | 0.30 | 0 | 0.25 | 0.33 | 0.33 |
②T2时,按表中数据,反应一定达到化学平衡状态的时间段是
③两容器中温度关系为T1
您最近一年使用:0次
2023-05-23更新
|
180次组卷
|
4卷引用:黑龙江省大庆市大庆中学2022-2023学年高一下学期7月期末考试化学试题
名校
6 . 某研究性学习小组利用草酸( )溶液和酸性高锰酸钾溶液的氧化还原反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
)溶液和酸性高锰酸钾溶液的氧化还原反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
已知: 可以加快草酸与酸性高锰酸钾反应的速率。
可以加快草酸与酸性高锰酸钾反应的速率。
(1)请写出该反应的氧化产物___________ ,该反应中参加反应的 和
和 物质的量之比为
物质的量之比为___________ 。
(2)实验②中 的体积
的体积
___________ mL。
(3)根据表中实验①②的数据,可以得到的结论是___________ 。
(4)探究温度对反应速率的影响,应选择实验(填编号)________ 。
(5)该实验过程中 随时间变化的趋势应如图所示。
随时间变化的趋势应如图所示。

在 、
、 、
、 三个相同的时间段里,
三个相同的时间段里,
___________  (填“>”、“<”或“=”),可能原因是
(填“>”、“<”或“=”),可能原因是___________ 。
 )溶液和酸性高锰酸钾溶液的氧化还原反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
)溶液和酸性高锰酸钾溶液的氧化还原反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:| 实验编号 | 实验温度/℃ | 试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
0.6mol/L 溶液 溶液 |  | 3mol/L稀 溶液 溶液 | 0.05mol/L 溶液 溶液 | |||
| ① | 25 | 5.0 | 3.0 | 2.0 | 5.0 | 1.4 |
| ② | 25 | 4.0 | V | 2.0 | 5.0 | 2.6 |
| ③ | 50 | 5.0 | 3.0 | 2.0 | 5.0 | 0.9 |
 可以加快草酸与酸性高锰酸钾反应的速率。
可以加快草酸与酸性高锰酸钾反应的速率。(1)请写出该反应的氧化产物
 和
和 物质的量之比为
物质的量之比为(2)实验②中
 的体积
的体积
(3)根据表中实验①②的数据,可以得到的结论是
(4)探究温度对反应速率的影响,应选择实验(填编号)
(5)该实验过程中
 随时间变化的趋势应如图所示。
随时间变化的趋势应如图所示。
在
 、
、 、
、 三个相同的时间段里,
三个相同的时间段里,
 (填“>”、“<”或“=”),可能原因是
(填“>”、“<”或“=”),可能原因是
您最近一年使用:0次
名校
7 . 我国科学家研究了活性炭催化条件下煤气中H2S和Hg的协同脱除,部分反应机理如图所示(吸附在催化剂表面的物种用*标注)。下列说法正确的是
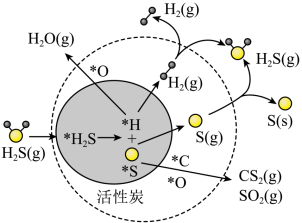
| A.图示反应过程中有极性共价键的断裂,没有非极性共价键的生成 |
| B.H2S活性炭分解生成H2(g)和S(s)的过程释放能量 |
| C.整个脱硫过程中硫元素既表现出氧化性又表现出还原性 |
| D.该机理由于活性炭的参与降低了H2S分解的热效应,使反应更易进行 |
您最近一年使用:0次
2023-04-29更新
|
244次组卷
|
5卷引用:黑龙江省牡丹江市第一高级中学2023-2024学年高一下学期5月期中考试化学试题
名校
8 . 同学们已经学习了同位素、同系物、同素异形体、同分异构体,你能区别这些概念吗?请将下面列出了几组物质进行分类。
①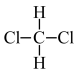 和
和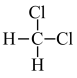 ②C(CH3)4和CH3CH(CH3)CH2CH3③CH4和C4H10④金刚石与石墨 ⑤氕、氘与氚 ⑥16O、17O和18O ⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3) ⑧氧气与臭氧 ⑨CH3Cl和CH3CH2Cl
②C(CH3)4和CH3CH(CH3)CH2CH3③CH4和C4H10④金刚石与石墨 ⑤氕、氘与氚 ⑥16O、17O和18O ⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3) ⑧氧气与臭氧 ⑨CH3Cl和CH3CH2Cl
(1)属于同位素的是_______ 。
(2)属于同系物的是_______ 。
(3)属于同素异形体的是_______ 。
(4)属于同分异构体的是_______ (以上填空均填写序号)。
(5)C4H10的一氯代物有_______ 种;CH3CH(CH3)CH2CH3的一氯代物有_______ 种。
(6)甲烷既是一种清洁能源,也是一种重要的化工原料。用TiO2/Cu2Al2O4为催化剂可以将CO2和CH4直接转化成乙酸(CH3COOH)。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。

①250~300℃时,温度升高而乙酸的生成速率降低的原因是_______ 。
②当温度的取值范围在_______ 时,温度是影响乙酸的生成速率的主要因素。
①
 和
和 ②C(CH3)4和CH3CH(CH3)CH2CH3③CH4和C4H10④金刚石与石墨 ⑤氕、氘与氚 ⑥16O、17O和18O ⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3) ⑧氧气与臭氧 ⑨CH3Cl和CH3CH2Cl
②C(CH3)4和CH3CH(CH3)CH2CH3③CH4和C4H10④金刚石与石墨 ⑤氕、氘与氚 ⑥16O、17O和18O ⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3) ⑧氧气与臭氧 ⑨CH3Cl和CH3CH2Cl(1)属于同位素的是
(2)属于同系物的是
(3)属于同素异形体的是
(4)属于同分异构体的是
(5)C4H10的一氯代物有
(6)甲烷既是一种清洁能源,也是一种重要的化工原料。用TiO2/Cu2Al2O4为催化剂可以将CO2和CH4直接转化成乙酸(CH3COOH)。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。

①250~300℃时,温度升高而乙酸的生成速率降低的原因是
②当温度的取值范围在
您最近一年使用:0次
9 . 下列所加的物质属于催化剂的是
| A.电解水制氢气时,加入少量的Na2SO4 |
| B.纯锌与硫酸反应制氢气时,滴入少量硫酸铜 |
| C.实验室用浓盐酸制氯气时,需加入MnO2固体 |
| D.利用H2O2水溶液制氧气时,加入少量的MnO2固体 |
您最近一年使用:0次
名校
10 . 三效催化剂能有效实现汽车尾气中CO、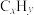 、
、 三种成分的净化,其催化剂BaO表面物质转化的关系如图。下列说法错误的是
三种成分的净化,其催化剂BaO表面物质转化的关系如图。下列说法错误的是

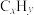 、
、 三种成分的净化,其催化剂BaO表面物质转化的关系如图。下列说法错误的是
三种成分的净化,其催化剂BaO表面物质转化的关系如图。下列说法错误的是
| A.在转化过程中,氮元素均被还原 |
| B.催化剂BaO先参加反应后又再生成,最终质量不变 |
C.储存时发生反应: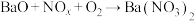 , , 的系数为2x-5 的系数为2x-5 |
D.还原时若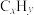 为 为 且与CO的数目相同,则生成的 且与CO的数目相同,则生成的 和 和 的数目相等 的数目相等 |
您最近一年使用:0次
2022-10-09更新
|
187次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学校2022一2023学年高一上学期9月份考试化学试题



