名校
解题方法
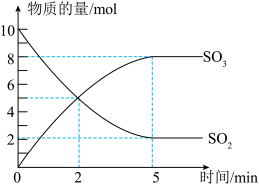
1 . 工业制硫酸的一步重要反应是SO2的催化氧化。在2L密闭容器中,充入SO2和足量O2,在催化剂、500℃的条件下发生反应。SO2、SO3的物质的量随时间的变化如图。下列说法不正确 的是
| A.在上述条件下,SO2不可能100%地转化为SO3 |
| B.反应到2min时,正逆反应速率相等 |
| C.反应开始至5min末,以SO2浓度的变化表示该反应的平均反应速率是0.8mol/(L·min) |
| D.使用催化剂是为了加快反应速率,提高生产效率 |
您最近一年使用:0次
2024-05-04更新
|
306次组卷
|
2卷引用:北京市陈经纶中学2023-2024学年高一下学期期中诊断化学试卷
名校
2 .  和
和 在催化剂表面合成氨的微观历程及能量变化的示意图如下,用
在催化剂表面合成氨的微观历程及能量变化的示意图如下,用 、
、 、
、 分别表示
分别表示 、
、 、
、 ,已知:
,已知: ,反应释放热量,下列说法正确的是
,反应释放热量,下列说法正确的是

| A.合成氨反应中,反应物断键吸收能量小于生成物形成新键释放的能量 |
B.②→③过程,是吸热过程且只有 键的断裂 键的断裂 |
C.③→④过程,N原子和H原子形成了含有非极性键的 |
D.使用催化剂,对生成 的速率没有影响 的速率没有影响 |
您最近一年使用:0次
名校
解题方法
3 . 我国是世界上最早冶炼锌的国家之一,有独立的炼锌发展史。现代炼锌主要采取湿法工艺,以闪锌矿(主要成分为 ,还含铁等元素)、软锰矿(主要成分为
,还含铁等元素)、软锰矿(主要成分为 )为原料联合生产锌和高纯度二氧化锰的一种流程如下:
)为原料联合生产锌和高纯度二氧化锰的一种流程如下:
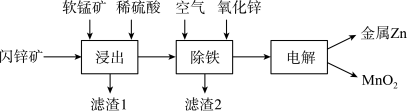
(1)浸出:加入 能促进
能促进 的溶解,提高锌的浸出率,同时生成硫单质。
的溶解,提高锌的浸出率,同时生成硫单质。 的作用类似催化剂,“催化”过程可表示为:
的作用类似催化剂,“催化”过程可表示为:
ⅰ:
ⅱ:……
①写出ⅱ的离子方程式:_______ 。
②下列实验方案可证实上述“催化”过程。将实验方案补充完整。
a.向酸化的 溶液中加入
溶液中加入 溶液,溶液几乎无色,再加入少量
溶液,溶液几乎无色,再加入少量 ,溶液变红。
,溶液变红。
b._______ 。
(2)除铁:已知①进入除铁工艺的溶液的pH约为3;②控制溶液pH为2.5~3.5,使铁主要以 沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量
沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量 的理由是
的理由是_______ 。
(3)电解:总反应(未配平): 。若不考虑副反应,为了使溶液中的
。若不考虑副反应,为了使溶液中的 、
、 均恰好完全反应,理论上需要再添加哪种离子?
均恰好完全反应,理论上需要再添加哪种离子?_______ (填“ ”、“
”、“ ”或“都不需要”)。
”或“都不需要”)。
 ,还含铁等元素)、软锰矿(主要成分为
,还含铁等元素)、软锰矿(主要成分为 )为原料联合生产锌和高纯度二氧化锰的一种流程如下:
)为原料联合生产锌和高纯度二氧化锰的一种流程如下:
(1)浸出:加入
 能促进
能促进 的溶解,提高锌的浸出率,同时生成硫单质。
的溶解,提高锌的浸出率,同时生成硫单质。 的作用类似催化剂,“催化”过程可表示为:
的作用类似催化剂,“催化”过程可表示为:ⅰ:

ⅱ:……
①写出ⅱ的离子方程式:
②下列实验方案可证实上述“催化”过程。将实验方案补充完整。
a.向酸化的
 溶液中加入
溶液中加入 溶液,溶液几乎无色,再加入少量
溶液,溶液几乎无色,再加入少量 ,溶液变红。
,溶液变红。b.
(2)除铁:已知①进入除铁工艺的溶液的pH约为3;②控制溶液pH为2.5~3.5,使铁主要以
 沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量
沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量 的理由是
的理由是(3)电解:总反应(未配平):
 。若不考虑副反应,为了使溶液中的
。若不考虑副反应,为了使溶液中的 、
、 均恰好完全反应,理论上需要再添加哪种离子?
均恰好完全反应,理论上需要再添加哪种离子? ”、“
”、“ ”或“都不需要”)。
”或“都不需要”)。
您最近一年使用:0次
名校
解题方法
4 . 空气质量评价的主要污染物为  等,一般来自于燃煤、工业废气、汽车尾气,会导致雾霾、酸雨的形成,危害环境。烟气中的
等,一般来自于燃煤、工业废气、汽车尾气,会导致雾霾、酸雨的形成,危害环境。烟气中的  可以用以下工艺除去。下列说法
可以用以下工艺除去。下列说法不正确 的是
 等,一般来自于燃煤、工业废气、汽车尾气,会导致雾霾、酸雨的形成,危害环境。烟气中的
等,一般来自于燃煤、工业废气、汽车尾气,会导致雾霾、酸雨的形成,危害环境。烟气中的  可以用以下工艺除去。下列说法
可以用以下工艺除去。下列说法
A.过程Ⅰ中, 和 和  均为反应物 均为反应物 |
B.过程Ⅱ中,发生反应:  |
C. 最终转化为 最终转化为  |
D. 在反应中作催化剂 在反应中作催化剂 |
您最近一年使用:0次
2024-02-19更新
|
347次组卷
|
2卷引用:北京市房山区2023-2024学年高一上学期期末检测化学试题
名校
5 . NO2的储存和还原技术能有效降低柴油发动机在空气过量时排放的NO2,原理如图1所示。用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,如图2所示。
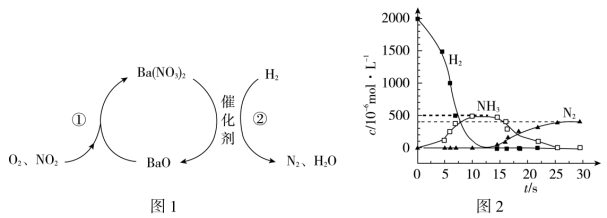
下列说法不正确的是

下列说法不正确的是
A.反应①为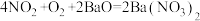 |
| B.储存和还原技术也能降低尾气排放的NO |
| C.0~12.5s内,氢气的消耗速率为v(H2)=1.6×10-4mol/(L·s) |
| D.反应②分两步进行,第二步Ba(NO3)2消耗的速率大于第一步的 |
您最近一年使用:0次
2023-07-13更新
|
279次组卷
|
4卷引用:北京朝阳区2022-2023学年高一下学期7月期末考试化学试题
名校
6 . 下列做法能减缓化学反应速率的是
| A.把食物放在冰箱里冷藏 |
| B.用H2O2溶液制O2时,通常加入少量的MnO2 |
| C.利用乙醇和乙酸制备乙酸乙酯,加入浓硫酸并加热 |
| D.用浓度较大的盐酸溶解石灰石 |
您最近一年使用:0次
2023-07-13更新
|
138次组卷
|
2卷引用:北京朝阳区2022-2023学年高一下学期7月期末考试化学试题
名校
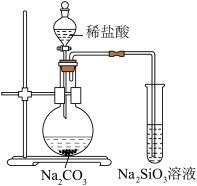
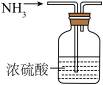
7 . 下列实验方案中能达到相应实验目的的是
| 选项 | A | B |
| 方案 |
|
|
| 目的 | 验证 对 对 分解有催化作用 分解有催化作用 | 比较C、Si和Cl的非金属性 |
| 选项 | C | D |
| 方案 |
 球浸泡在冷水和热水中 球浸泡在冷水和热水中 |
|
| 目的 | 探究温度对化学平衡的影响 | 干燥氨气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-11更新
|
308次组卷
|
2卷引用:北京市第一○一中学2022-2023学年高一下学期期末考试化学试题
名校
8 . 汽车尾气中含有CO、NOx等有害气体。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:___________ 。
(2)汽车尾气中NO生成过程的能量变化示意图如下:
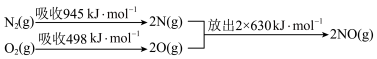
该条件下,N2和O2完全反应生成2molNO时需要_______ (吸收或释放)________ kJ的能量。
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

①NiO电极上发生的是___________ 反应(填“氧化”或“还原”)。
②外电路中,电子的流动方向是从___________ 电极流出(填NiO或Pt);Pt电极上的电极反应式为___________ 。
(4)一种新型催化剂能使NO和CO发生反应:2NO+2CO⇌2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
①请将表中数据补充完整:A___________ ;B___________ 。
②能验证温度对化学反应速率影响规律的实验是___________ (填实验编号)。
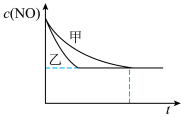
③实验Ⅰ和实验Ⅱ中,c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的曲线是___________ (填“甲”或“乙”)。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
(2)汽车尾气中NO生成过程的能量变化示意图如下:

该条件下,N2和O2完全反应生成2molNO时需要
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

①NiO电极上发生的是
②外电路中,电子的流动方向是从
(4)一种新型催化剂能使NO和CO发生反应:2NO+2CO⇌2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
| 实验 编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.20×10-3 | B | 124 |
| Ⅲ | 350 | A | 5.80×10-3 | 82 |
②能验证温度对化学反应速率影响规律的实验是
③实验Ⅰ和实验Ⅱ中,c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的曲线是

您最近一年使用:0次
名校
9 . 下列实验操作和现象与结论关系不正确 的是
| 操作和现象 | 结论 | |
| A | 将铝片放入盐酸中,产生气泡的速率开始时较慢,随后加快,后来又逐渐减慢 | H+的浓度是影响反应速率的唯一因素 |
| B | 将大小相同的K和Na放入等体积的水中,钾比钠反应剧烈 | 钾元素的金属性比钠元素强 |
| C | 漂白粉与浓HCl混合产生的气体能使湿润蓝色石蕊试纸先变红后褪色 | 漂白粉和浓HCl反应生成Cl2 |
| D | 向盛有H2O2溶液的试管中,加入少量FeCl3溶液,产生气泡的速率比不加FeCl3溶液的快 | FeCl3可以加快H2O2分解的速率,起了催化作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 合成氨是工业上的重要反应:N2(g)+3H2(g) 2NH3(g),下列说法
2NH3(g),下列说法不正确 的是
 2NH3(g),下列说法
2NH3(g),下列说法| A.增大压强既加快反应速率,又有利于平衡向合成氨方向移动 |
| B.反应达平衡状态后,单位时间内生成1molN2的同时消耗3molH2 |
| C.将氨分离出来,有利于平衡向合成氨方向移动 |
| D.铁作催化剂既加快反应速率,又有利于平衡向合成氨方向移动 |
您最近一年使用:0次