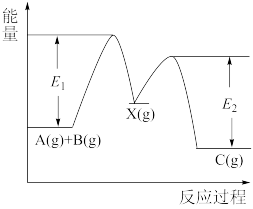
| A.△H1=△H-△H2 >0 | B.X是反应A(g)+B(g)→C(g)的催化剂 |
| C.E2是反应②的活化能 | D.△H = E1-E2 |
【实验原理】2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液 颜色褪至无色 所需时间/min | |||
| 0.6 mol · L-1 H2C2O4溶液 | H2O | 0.2 mol · L-1 KMnO4溶液 | 3 mol · L-1 稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
(1)根据上表中的实验数据,可以得到的结论是
(2)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率v(KMnO4)=
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图甲所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图乙所示。该小组同学根据图乙所示信息提出了新的假设,并继续进行实验探究。
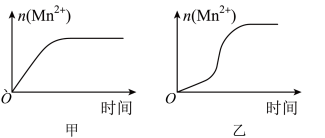
②请你帮助该小组同学完成实验方案,并填写表中空白。
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6mol/LH2C2O4溶液 | H2O | 0.2mol/LKMnO4溶液 | 3mol/L稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | t | |
③若该小组同学提出的假设成立,应观察到的现象是
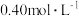 的
的 溶液中加入少量
溶液中加入少量 溶液(忽略整个过程中溶液体积的变化),不同时刻测得生成
溶液(忽略整个过程中溶液体积的变化),不同时刻测得生成 的体积(已折算为标准状况下)如表所示:
的体积(已折算为标准状况下)如表所示: | 0 | 2 | 4 | 6 |
 | 0 | 9.9 | 17.5 | 22.4 |
资料显示,反应分两步进行:①
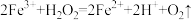 ;②
;②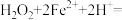
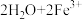 。反应过程中能量变化如图所示。下列说法正确( )
。反应过程中能量变化如图所示。下列说法正确( )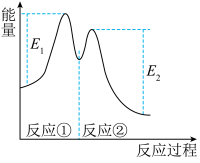
A. 的作用是增大过氧化氢的分解速率 的作用是增大过氧化氢的分解速率 |
| B.反应①、②均是放热反应 |
C.反应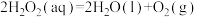 是吸热反应 是吸热反应 |
D.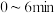 内的平均反应速率 内的平均反应速率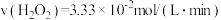 |
| 选项 | 事实 | 解释 |
| A | 夏天,常用冰箱保存食品和新鲜蔬菜 | 降低温度,食品和蔬菜腐烂速率减慢 |
| B | 植物油要密封保存 | 减小 的浓度,减慢植物油被氧化的速率 的浓度,减慢植物油被氧化的速率 |
| C | 烧锅炉时,常常将煤块粉碎 | 减小 和 和 气体的排放量 气体的排放量 |
| D | 酿造米酒时,在熟米饭中掺一些酒曲 | 酒曲作催化剂,加快淀粉转化成米酒 |
| A.A | B.B | C.C | D.D |
 2NH3,下列关于该反应的说法正确的是
2NH3,下列关于该反应的说法正确的是| A.升高温度可以减慢反应速率 |
| B.减小N2的浓度可以加快反应速率 |
| C.使用恰当的催化剂能加快反应速率 |
| D.达到化学平衡时,N2转化率为100% |
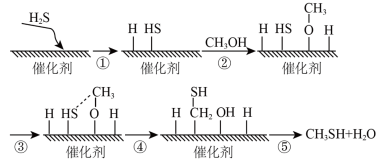
| A.CH3SH中碳元素化合价为-2价 |
| B.过程⑤中,形成了O—H键和C—H键 |
| C.该催化剂可有效提高生成物的产量 |
D.硫化氢与甲醇合成甲硫醇的总反应方程式为:H2S + CH3OH CH3SH+ H2O CH3SH+ H2O |
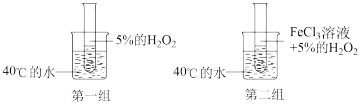
| A.浓度 | B.压强 | C.温度 | D.催化剂 |

| A.HAP能提高HCHO与O2的反应速率 |
| B.HCHO在反应过程中,有C—H键发生断裂 |
| C.根据图示信息,CO2分子中的氧原子全部来自O2 |
D.该反应可表示为:HCHO+O2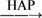 CO2+H2O CO2+H2O |
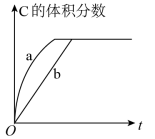
①增大A的浓度 ②增大B的浓度 ③升高温度 ④加入合适的催化剂
| A.③④ | B.①③ | C.④ | D.①② |
10 . 合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3⇌[Cu(NH3)3CO]Ac。完成下空:
(1)如果要提高上述反应的反应速率,可以采取的措施是
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
(2)铜液中的足量的氨可吸收二氧化碳,写出该反应的化学方程式
(3)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为
(4)已知与CO2与CS2分子结构相似,熔点CS2高于CO2,其原因是
(5)某研究性学习组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
实验序号 | 实验温度 | KMnO4溶液 | H2C2O4溶液 | H2O | 溶液褪色时间 | ||
V(mL) | c(mol/L) | V(mL) | c(mol/L) | V(mL) | t(s) | ||
A | 293K | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313K | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
①其中V1=
②反应一段时间后该反应速率会加快,造成此种变化的原因可能是



