解题方法
1 . I.某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
(1)已知反应后H2C2O4转化为CO2逸出,KMnO4溶液转化为MnSO4,每消耗1molH2C2O4转移___ mol电子。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4)∶n(KMnO4)≥___ 。
(2)探究温度对化学反应速率影响的实验编号是___ (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是____ 。
II.水煤气变换CO(g) + H2O(g)⇌CO2(g) + H2(g)是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。已知T(大于100)℃时,将2molCO(g)和3molH2O(g)通入一容积固定为2L的密闭容器中,回答下列问题:
(1)反应进行到1min时测得CO的物质的量为1.8mol,则H2的平均反应速率为___ ,此时改变某一条件,能使H2的平均反应速率加快的是___ 。
A.恒容时充入氖气 B.升高温度 C.将体积缩小一半 D.恒温恒容,移走CO2
(2)已知在T℃时H2(g)+CoO(s) ⇌Co(s)+H2O(g) K1=1,CO(g)+CoO(s) ⇌Co(s)+CO2(g) K2=4,求T℃时,CO(g)+H2O(g) ⇌ CO2(g)+H2(g)的平衡常数为___ 。
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(2)探究温度对化学反应速率影响的实验编号是
II.水煤气变换CO(g) + H2O(g)⇌CO2(g) + H2(g)是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。已知T(大于100)℃时,将2molCO(g)和3molH2O(g)通入一容积固定为2L的密闭容器中,回答下列问题:
(1)反应进行到1min时测得CO的物质的量为1.8mol,则H2的平均反应速率为
A.恒容时充入氖气 B.升高温度 C.将体积缩小一半 D.恒温恒容,移走CO2
(2)已知在T℃时H2(g)+CoO(s) ⇌Co(s)+H2O(g) K1=1,CO(g)+CoO(s) ⇌Co(s)+CO2(g) K2=4,求T℃时,CO(g)+H2O(g) ⇌ CO2(g)+H2(g)的平衡常数为
您最近一年使用:0次
2 . 研究化学反应时,既要考虑物质变化与能量变化,也要关注反应的快慢与限度。回答下列问题:
(1)某温度时,在2 L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:(A、B均为气体)
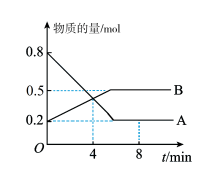
①该反应的化学方程式为____________________ ;
②反应开始至4 min时,B的平均反应速率为________ ;
③4 min时,反应是否达到平衡状态?________ (填“是”或“否”),8 min时,v(正)________ v(逆)(填“>”、“<”或“=”)。
(2)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
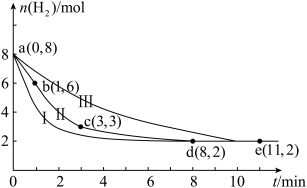
①a—b,b—c,c—d,d—e四段中,平均反应速率最大的时间段是___________ ,该时间段内CO2的平均反应速率是________ 。
②若在反应中加入了催化剂,则反应过程将变为图中的曲线_____ (填“Ⅰ”或“Ⅱ”或“Ⅲ”)。
③平衡时CO2的转化率是_________ ;反应前后容器内的压强比是__________ 。
(1)某温度时,在2 L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:(A、B均为气体)

①该反应的化学方程式为
②反应开始至4 min时,B的平均反应速率为
③4 min时,反应是否达到平衡状态?
(2)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图曲线Ⅱ所示。a,b,c,d,e括号内数据表示坐标.
①a—b,b—c,c—d,d—e四段中,平均反应速率最大的时间段是
②若在反应中加入了催化剂,则反应过程将变为图中的曲线
③平衡时CO2的转化率是
您最近一年使用:0次
2019-05-14更新
|
448次组卷
|
4卷引用:贵州省黔西南州赛文高级中学 2021-2022学年高二上学期期中考试化学试题
2013·河南郑州·一模
名校
3 . 某化学反应的能量变化如下图所示。下列有关叙述正确的是
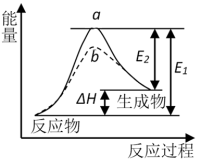

| A.该反应的焓变ΔH=E2-E1 |
| B.a、b分别对应有催化剂和无催化剂的能量变化 |
| C.催化剂能改变反应的焓变 |
| D.催化剂能降低反应的活化能 |
您最近一年使用:0次
2019-03-03更新
|
307次组卷
|
12卷引用:2015-2016学年贵州遵义航天中学高二上第三次月考化学卷
2015-2016学年贵州遵义航天中学高二上第三次月考化学卷湖北省宜昌市葛洲坝中学2017-2018学年高二上学期期中考试化学试题新疆维吾尔自治区伊宁市生产建设兵团四师一中2018-2019学年高二上学期期中考试化学试题山东省菏泽市第一中学老校区2018-2019学年高二上学期期末模拟化学试题云南省曲靖市沾益区四中2018-2019学年高二上学期期末考试化学试题【全国百强校】山东省潍坊第一中学2018-2019学年高二下学期开学(2月)考试化学试题广东省揭阳市惠来县第一中学2019-2020学年高二上学期期中考试化学试题海南省农垦中学2023-2024学年高二上学期期末考试化学试题(B卷)(已下线)2013届河南省郑州市高三第一次模拟考试化学试卷(已下线)2015届浙江省柯桥中学高三月考(10月)化学试卷2015届北京市第66中学高三上学期期中考试化学试卷河南省安阳市第一中学2023届高三第四次全真模拟化学试题
名校
4 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸的反应,记录以下实验数据:
(1)请写出该反应的离子方程式__________________________________________ ,当该反应以表中数据反应完全时转移电子数为_______________ NA
(2)V1______
(3)根据上表中的实验①、②数据,可以得到的结论是_____ 。
(4)探究温度对化学反应速率的影响,应选择_____ (填实验编号)
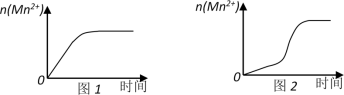
(5)该小组同学根据经验绘制了 n (Mn 2+ )随时间变化的趋势如图 1 所示,但有同学查阅已有的实验资料发现,该实验过程中 n (Mn 2+ ) 随时间变化的实际趋势如图 2 所示。
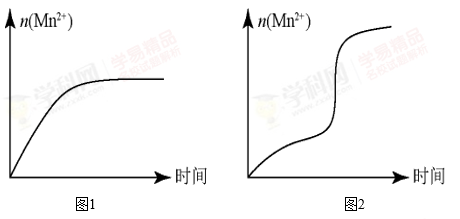
该小组同学根据图 2 所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
①该小组同学提出的假设是_____ 。
②若该小组同学提出的假设成立,应观察到_________________________________ 现象。
实验编号 | 实验温度 | 试管中所加试剂及其用量 / mL | 溶液褪至无色所需时间/ min | |||
0.6mol/L H2C2O4 溶液 | H2O | 3mol/L H2SO4 稀溶液 | 0.05mol/L KMnO4溶液 | |||
① | 25 | 3.0 | V1 | 2.0 | 3.0 | 1.5 |
② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
③ | 50 | 2.0 | V2 | 2.0 | 3.0 | 1.0 |
(1)请写出该反应的离子方程式
(2)V1
(3)根据上表中的实验①、②数据,可以得到的结论是
(4)探究温度对化学反应速率的影响,应选择
(5)该小组同学根据经验绘制了 n (Mn 2+ )随时间变化的趋势如图 1 所示,但有同学查阅已有的实验资料发现,该实验过程中 n (Mn 2+ ) 随时间变化的实际趋势如图 2 所示。

该小组同学根据图 2 所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
实验编号 | 实验温度/℃ | 试管中所加试剂及其用量 | 再加入某种固体 | 溶液褪至无色所需时间 / min | |||
| ④ | 25 | 0.6mol/L H2C2O4 溶液 | H2O | 3mol/L H2SO4 稀溶液 | 0.05mol/L KMnO4 溶液 | ||
2.0 | 3.0 | 2.0 | 3.0 | MnSO4 | t | ||
①该小组同学提出的假设是
②若该小组同学提出的假设成立,应观察到
您最近一年使用:0次
2018-12-10更新
|
151次组卷
|
2卷引用:【全国百强校】贵州省遵义市第四中学2018-2019学年高二上学期第一次月考化学试题1
名校
5 . 下列生产或实验事实引出的相应结论不正确的是
| 选项 | 事实 | 结论 |
| A | 工业制硫酸中,在矿石处理阶段,将矿石粉碎再煅烧 | 增大反应物的接触面积,加快化学反应速率 |
| B | A、B两支试管中分别加入等体积5%的H2O2,在B试管中加入MnO2,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| C | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间变短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
| D | 一定条件下:H2(g)+I2(g)  2HI(g)达到反应平衡,缩小体积颜色加深 2HI(g)达到反应平衡,缩小体积颜色加深 | c(I2)增大,I2物质的量增多 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-12-10更新
|
247次组卷
|
5卷引用:【全国百强校】贵州省遵义市第四中学2018-2019学年高二上学期第一次月考化学试题1
名校
6 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验内容及记录】
请回答:
(1)写出以上反应的化学方程式:______________________________________________
(2)根据上表中的实验数据,可以得到的结论是______________________________________________ 。
(3)利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4) =___________ 。
(4)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①该小组同学提出的假设是____________________________________________________ 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
③若该小组同学提出的假设成立,应观察到的现象是_____________________ 。
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量 / mL | 室温下溶液颜色褪至无色所需时间 / min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05mol/L KMnO4溶液 | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| 3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
(1)写出以上反应的化学方程式:
(2)根据上表中的实验数据,可以得到的结论是
(3)利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4) =
(4)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该小组同学提出的假设是
②请你帮助该小组同学完成实验方案,并填写表中空白。
| 实验编号 | 室温下,试管中所加试剂及其用量 / mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 / min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05 mol/L KMnO4溶液 | |||
| 4 | 3.0 | 2.0 | 2.0 | 3.0 | | t |
您最近一年使用:0次
2018-12-09更新
|
344次组卷
|
3卷引用:贵州省毕节市金沙县第一中学2021-2022学年高二上学期期中考试化学试题
名校
7 . 合成气(CO和H2)是目前化工常用的原料,下面是用甲烷制备合成气的两种方法:①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
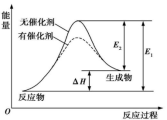
 CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
| A.E1表示2CH4(g)+O2(g)=2CO(g)+4H2(g)的活化能 |
B.E2表示CH4(g)+H2O(g) CO(g)+3H2(g)的活化能 CO(g)+3H2(g)的活化能 |
| C.该图示为反应②的反应过程与能量变化示意图 |
| D.一般情况下,加入催化剂,既能降低E1,也能降低E2,但不能改变E1与E2的差值 |
您最近一年使用:0次
2018-01-20更新
|
459次组卷
|
6卷引用:贵州省安顺市平坝第一高级中学2019-2020学年高二上学期期中考试化学试题
名校
8 . 影响化学反应速率的因素有:浓度、压强、温度、催化剂等。下列有关说法不正确的是
| A.改变压强不一定能改变有气体参与反应的速率 |
| B.增大浓度能加快化学反应速率,原因是增大浓度增加了反应体系中活化分子的百分数 |
| C.温度升高使化学反应速率加快的主要原因是增加了单位体积内活化分子总数 |
| D.催化剂能加快化学反应速率主要原因是降低反应活化能 |
您最近一年使用:0次
2017-11-24更新
|
219次组卷
|
2卷引用:【全国百强校】贵州省铜仁市思南中学2018-2019学年高二上学期第一次月考化学试题
名校
9 . 反应H2(g) + I2(g) 2HI(g)的逆反应速率随时间变化的曲线如下图所示,t1时刻反应达到平衡,维持其他条件不变,t1时刻只改变一种条件,该条件可能是
2HI(g)的逆反应速率随时间变化的曲线如下图所示,t1时刻反应达到平衡,维持其他条件不变,t1时刻只改变一种条件,该条件可能是
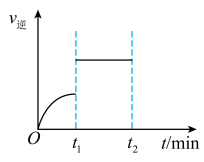
①增大H2浓度 ②缩小容器体积 ③恒容时充入Ar气 ④使用催化剂
 2HI(g)的逆反应速率随时间变化的曲线如下图所示,t1时刻反应达到平衡,维持其他条件不变,t1时刻只改变一种条件,该条件可能是
2HI(g)的逆反应速率随时间变化的曲线如下图所示,t1时刻反应达到平衡,维持其他条件不变,t1时刻只改变一种条件,该条件可能是 
①增大H2浓度 ②缩小容器体积 ③恒容时充入Ar气 ④使用催化剂
| A.①② | B.③④ | C.②④ | D.①④ |
您最近一年使用:0次
2017-11-11更新
|
708次组卷
|
16卷引用:贵州省北京师范大学遵义附属学校2019-2020学年高二下学期第二次月考化学试题
贵州省北京师范大学遵义附属学校2019-2020学年高二下学期第二次月考化学试题甘肃省会宁县第一中学2017-2018学年高二上学期期中考试(理)化学试题湖南省衡阳市26中2017-2018学年高二上学期期中考试化学试题湖南省衡阳二十六中2017-2018学年高二上学期期中考试化学试题甘肃省甘谷第一中学2019-2020学年高二上学期第一次月考化学试题江苏省苏州市相城区陆慕高级中学2019-2020高二下学期4月质量检测化学试题山东省新泰一中北校2020-2021学年高二上学期第二次阶段性考试化学试题(已下线)综合复习与测试(1)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)河北省唐山十县一中联盟2022-2023学年高二上学期期中考试化学试题福建省南靖县第一中学、兰水中学2022-2023学年高二上学期期中联考化学试题福建省德化一中、永安一中、漳平一中三校协作2022-2023学年高二上学期12月联考化学试题云南昆明市昆明行知中学2021-2022学年高二上学期期中考试化学试题河南省潢川第一中学2022-2023学年高二上学期期末考试化学试题河北定州中学2023-2024学年高二上学期12月月考化学试题山西省朔州市怀仁市大地学校高中部2023-2024学年高二上学期12月月考化学试题陕西师范大学附属中学2022-2023学年高一下学期6月期末考试化学试题
名校
解题方法
10 . 某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色先慢后快,即反应速率由小变大。小组成员为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种,并为此设计实验进行探究验证。
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等。
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容。
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为______________
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是_______________
(3)猜想Ⅱ可是:___________________
要设计实验验证猜想Ⅱ,进行该实验还要补充一种试剂及一种仪器,分别是_______________
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容_____________ 。
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等。
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容。
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是
(3)猜想Ⅱ可是:
要设计实验验证猜想Ⅱ,进行该实验还要补充一种试剂及一种仪器,分别是
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容
| 试管A | 试管B | |
| 加入试剂 | ||
| 实验现象(褪色时间) | ||
| 结论 | 猜想Ⅱ正确 | |
您最近一年使用:0次
2016-12-09更新
|
298次组卷
|
4卷引用:贵州省贵阳市第三实验中学2019-2020学年高二上学期第一次月考化学试题



