解题方法
1 . 化学创造美好生活,下列物质用途与所述的化学知识没有关联的是
| 选项 | 物质用途 | 化学知识 |
| A | 二氧化硫用作红酒防腐剂 |  溶于水显弱酸性 溶于水显弱酸性 |
| B | 乙炔用于金属切割与焊接 |  燃烧放出大量热 燃烧放出大量热 |
| C | 碳酸氢钠用作面团膨松剂 |  受热分解会产生 受热分解会产生 |
| D | 铁触媒用作合成氨的催化剂 | 催化剂可以提高反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 有研究认为,强碱性环境下反应:I-+ClO- IO-+Cl-可能分如下三步进行:
IO-+Cl-可能分如下三步进行:
第一步:ClO-+H2O HClO+OH- K1=3.3×10-10
HClO+OH- K1=3.3×10-10
第二步:…… K2=……
第三步:HIO+OH- IO-+H2O K3=2.3×103
IO-+H2O K3=2.3×103
下列说法正确的是
 IO-+Cl-可能分如下三步进行:
IO-+Cl-可能分如下三步进行:第一步:ClO-+H2O
 HClO+OH- K1=3.3×10-10
HClO+OH- K1=3.3×10-10第二步:…… K2=……
第三步:HIO+OH-
 IO-+H2O K3=2.3×103
IO-+H2O K3=2.3×103下列说法正确的是
A.第二步反应的平衡常数表达式为K2= |
| B.由K值大小可以判断第三步反应比第一步快 |
| C.升高温度会使K1变小、K3变大 |
| D.OH-是该反应的催化剂 |
您最近一年使用:0次
2022-05-29更新
|
436次组卷
|
4卷引用:上海市虹口区2022届高三下学期第二次模拟考试化学试题
上海市虹口区2022届高三下学期第二次模拟考试化学试题(已下线)第22讲 化学平衡常数及转化率的计算(讲)-2023年高考化学一轮复习讲练测(全国通用)河南省郑州市实验中学2023-2024学年高三上学期期中考试化学试题河南省濮阳市油田第一中学2023-2024学年高三上学期培优测试理科综合化学试题
3 . 用下列仪器或装置(图中夹持略)进行相应实验,能达到实验目的的是
| A | B | C | D |
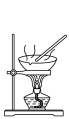 | 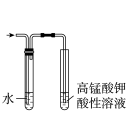 | 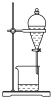 | 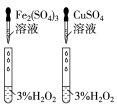 |
蒸发结晶制备 晶体 晶体 | 检验溴乙烷消去产物 | 分离苯和溴苯 | 探究不同催化剂 对  分解速率的影响 分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-18更新
|
661次组卷
|
6卷引用:复旦大学附属中学2022届高三下学期 教学质量检测(二模)化学等级试卷
4 . CO2和CH4都是温室气体。一定条件下,CH4和CO2以镍合金为催化剂,发生反应:CO2(g)+CH4(g) 2CO(g)+2H2(g)。完成下列填空。
2CO(g)+2H2(g)。完成下列填空。
(1)甲烷分子的空间构型是_______ ,干冰的晶体类型是_______ 。
(2)该反应的化学平衡常数表达式为K=_______ 。不同温度下,K的数值如下:
该反应的逆反应是_______ 反应(填“吸热”或“放热”)。
(3)T1°C时,科研人员探究等质量的三种催化剂(图中用I、II、III表示)在相同条件下的催化效果。在1L恒容容器中,分别充入1molCO2和2molCH4,测得H2物质的量随时间变化如图所示。
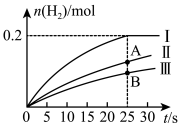
①使用催化剂I时,0~25秒间CO2的平均反应速率v(CO2)=_______ mol·L-1·s-1;CH4的平衡浓度是_______ mol·L-1。
②如果不考虑催化剂价格,则使用催化剂_______ (填“I”、“I”或“III”)的效果最好。状态A与B生成H2的速率大小关系是v(A)_______ v(B)(填“>”、“<”或“=”)。
③有利于提高CO2转化率的措施是_______ (填字母)。
a.使用更高效的催化剂
b.升高温度
c.增大压强
d.增大CH4与CO2的投料比
 2CO(g)+2H2(g)。完成下列填空。
2CO(g)+2H2(g)。完成下列填空。(1)甲烷分子的空间构型是
(2)该反应的化学平衡常数表达式为K=
| 温度 | 200°C | 250°C | 300°C |
| K | 56 | 64 | 80 |
(3)T1°C时,科研人员探究等质量的三种催化剂(图中用I、II、III表示)在相同条件下的催化效果。在1L恒容容器中,分别充入1molCO2和2molCH4,测得H2物质的量随时间变化如图所示。

①使用催化剂I时,0~25秒间CO2的平均反应速率v(CO2)=
②如果不考虑催化剂价格,则使用催化剂
③有利于提高CO2转化率的措施是
a.使用更高效的催化剂
b.升高温度
c.增大压强
d.增大CH4与CO2的投料比
您最近一年使用:0次
5 . 合成氨反应过程中的能量变化如图所示,下列说法正确的是


| A.反应体系中加入催化剂,会改变反应的热效应 |
| B.反应物的总能量低于生产物的总量 |
C.该反应的热化学方程式为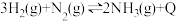 (Q>0) (Q>0) |
| D.该反应是吸热反应 |
您最近一年使用:0次
名校
解题方法
6 . 下列实验不能达到目的的是
| 选项 | 目的 | 实验 |
| A | 比较水与乙醇中氢的活泼性 | 分别将少量钠投入到盛有水和乙醇的烧杯中 |
| B | 加快氧气的生成速率 | 在过氧化氢溶液中加入少量 |
| C | 除去乙酸乙酯中的少量乙酸 | 加入饱和碳酸钠溶液洗涤、分液 |
| D | 配制浓度为 的 的 溶液 溶液 | 称取 固体4.0g,放入100 固体4.0g,放入100 容量瓶中,加水溶解并稀释至刻度 容量瓶中,加水溶解并稀释至刻度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-08-08更新
|
621次组卷
|
8卷引用:上海市宝山区2022届高三模拟考试化学试题
解题方法
7 . 在汽车尾气处理过程中存在反应: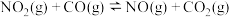 ,该反应过程及能量变化如图所示。下列说法正确的是
,该反应过程及能量变化如图所示。下列说法正确的是

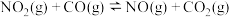 ,该反应过程及能量变化如图所示。下列说法正确的是
,该反应过程及能量变化如图所示。下列说法正确的是
| A.升高温度,平衡正向移动 | B.改变压强,反应速率不变 |
| C.反应过程中吸收的热量小于放出的热量 | D.使用催化剂可以有效提高反应物的平衡转化率 |
您最近一年使用:0次
2020-12-26更新
|
369次组卷
|
3卷引用:上海市松江区2021届高三一模化学试卷
2012·上海徐汇·二模
8 . 正丁醛可由丙烯通过下列反应制取:
CH3CH=CH2 + CO + H2 CH3CH2CH2CHO(正丁醛)反应①
CH3CH2CH2CHO(正丁醛)反应①
同时发生副反应:CH3CH=CH2 +CO + H2 (CH3)2CHCHO(异丁醛)反应②
(CH3)2CHCHO(异丁醛)反应②
CH3CH=CH2 + H2 CH3CH2CH3反应③
CH3CH2CH3反应③
三个反应在不同温度时的平衡常数见下表。回答问题:
(1)423K时,如果反应在恒容密闭容器中发生,当反应达到平衡时,下列说法错误的是_____ (填序号)。
a.c(CO):c( H2)一定等于1:1
b.反应混合物的密度保持不变
c.丙烯转化率达到最大值
d.单位时间内,n(CO)消耗= n(正丁醛)生成
(2)当反应达到平衡后,若将反应体系的温度从298 K提高到423 K,再次达到平衡后,在生成物中,__________ (填物质名称)的摩尔百分含量降低。
(3)若反应在298K进行,根据平衡常数作出的推测正确的是______ 。
a.反应③的反应速率最大 b.达到平衡后生成物中丙烷的体积百分含量最高
c.反应②达到平衡所需时间最长 d.298K时只有反应③向正反应方向进行
(4)使用催化剂后,单位时间里正丁醛的产量大大提高,反应体系产物中正/异醛比增大。导致这种情况出现的原因是____________________________ 。
CH3CH=CH2 + CO + H2
 CH3CH2CH2CHO(正丁醛)反应①
CH3CH2CH2CHO(正丁醛)反应①同时发生副反应:CH3CH=CH2 +CO + H2
 (CH3)2CHCHO(异丁醛)反应②
(CH3)2CHCHO(异丁醛)反应②CH3CH=CH2 + H2
 CH3CH2CH3反应③
CH3CH2CH3反应③三个反应在不同温度时的平衡常数见下表。回答问题:
| 温度/K | 反应① | 反应② | 反应③ |
| 298 | 2.96×109 | 2.53×109 | 1.32×1015 |
| 423 | 1.05×102 | 5.40×102 | 2.52×102 |
(1)423K时,如果反应在恒容密闭容器中发生,当反应达到平衡时,下列说法错误的是
a.c(CO):c( H2)一定等于1:1
b.反应混合物的密度保持不变
c.丙烯转化率达到最大值
d.单位时间内,n(CO)消耗= n(正丁醛)生成
(2)当反应达到平衡后,若将反应体系的温度从298 K提高到423 K,再次达到平衡后,在生成物中,
(3)若反应在298K进行,根据平衡常数作出的推测正确的是
a.反应③的反应速率最大 b.达到平衡后生成物中丙烷的体积百分含量最高
c.反应②达到平衡所需时间最长 d.298K时只有反应③向正反应方向进行
(4)使用催化剂后,单位时间里正丁醛的产量大大提高,反应体系产物中正/异醛比增大。导致这种情况出现的原因是
您最近一年使用:0次
解题方法
9 . 乙二酸俗称草酸(结构简式为HOOC—COOH,可简写为H2C2O4),它是一种重要的化工原料。(常温下0.01 mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示。)填空:
(1)写出H2C2O4的电离方程式________________ 。
(2)KHC2O4溶液显酸性的原因是_________________ ;向0.1 mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是______ 。
a.c(K+)=c(HC2O4-)+c(H2C2O4)+c(C2O42-) b.c(Na+)=c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-) d.c(K+)>c(Na+)
(3)H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫色消失。写出反应的离子方程式____________________ ;又知该反应开始时速率较慢,随后大大加快,可能的原因是______________________ 。
| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
(1)写出H2C2O4的电离方程式
(2)KHC2O4溶液显酸性的原因是
a.c(K+)=c(HC2O4-)+c(H2C2O4)+c(C2O42-) b.c(Na+)=c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-) d.c(K+)>c(Na+)
(3)H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫色消失。写出反应的离子方程式
您最近一年使用:0次
解题方法
10 . 如图是某条件时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )


| A.该反应的热化学方程式为:2NH3⇌N2+3H2 △H=﹣92kJ·mol﹣1 |
| B.生成物的能量之和比反应物的能量之和高 92 kJ |
| C.a曲线是未加入催化剂时的能量变化曲线 |
| D.加入催化剂可增加正反应速率,减小逆反应速率 |
您最近一年使用:0次



