1 . 下表中"方法导引”与“示例"对应关系不正确的是
| 选项 | 方法导引 | 示例 |
| A | 分类 | 实验室中制取气体装置的连接顺序一般为:发生装置 除杂装置 除杂装置 收集装置 收集装置 尾气处理装置 尾气处理装置 |
| B | 预测 | 钠、钾能与水反应,铷与钠、钾都属于IA族元素,则可预测铷也能与水反应 |
| C | 变量控制 | 探究催化剂对化学反应速率的影响时,需要控制温度、浓度和他影响因素保持不变 |
| D | 认识有机化合物的一般思路 | 先分析有机物的碳骨架和官能团,再认识它的类别、性质和用途 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 尿素(分子式 )水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
)水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
 )水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
)水溶液热解产生的NH3可去除尾气中的NOx,流程如下: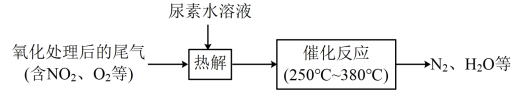
| A.尿素中氮元素的化合价为-3 |
B.“催化反应”过程中NH3还原NO2的化学方程式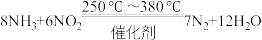 |
| C.若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。硫酸盐的产生是因为SO2被O2、H2O还原成H2SO4,再与NH3反应而得 |
D.“催化反应”过程中需控制温度在 之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低 之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低 |
您最近一年使用:0次
3 . 我国丙烷储量丰富,将丙烷转化为具有高附加值的产品是提高丙烷利用效率.实现碳基能源高效利用的关键技术之一。传统利用丙烷:燃烧供能;理想利用丙烷:丙烷脱氢(PDH)制丙烯。下列叙述错误的是
| A.丙烷的燃烧反应一定是放热反应 |
B.丙烷的一氯代物 有2种结构 有2种结构 |
| C.丙烷与溴水在光照条件下容易发生取代反应 |
| D.工业选择合适的催化剂能提高PDH反应的生产效率 |
您最近一年使用:0次
名校
解题方法
4 . 工业合成氨是最重要的人工固氮途径,发生反应: 。请回答:
。请回答:
(1)已知断开1mol的某化学键所需能量如表所示。若固氮反应中有2mol 生成时,
生成时,______ (填 “吸收”或“放出”)热量______ kJ。
(2)恒温恒压条件下,向密闭容器中投入等物质的量的 和
和 发生反应,下列描述能说明反应已达到化学平衡状态的是______。
发生反应,下列描述能说明反应已达到化学平衡状态的是______。
(3)利用 可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的
可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的______ 极(填“正”或“负”),其电极方程式为______ 。______ (填“a”、“b”或“c”)______
 。请回答:
。请回答:(1)已知断开1mol的某化学键所需能量如表所示。若固氮反应中有2mol
 生成时,
生成时,化学键 |
|
|
|
能量(kJ) | 436 | 391 | 946 |
(2)恒温恒压条件下,向密闭容器中投入等物质的量的
 和
和 发生反应,下列描述能说明反应已达到化学平衡状态的是______。
发生反应,下列描述能说明反应已达到化学平衡状态的是______。A.反应速率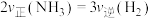 | B.混合气体的密度不再变化 |
| C.混合气体的平均摩尔质量不再变化 | D. 的体积分数不再变化 的体积分数不再变化 |
(3)利用
 可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的
可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的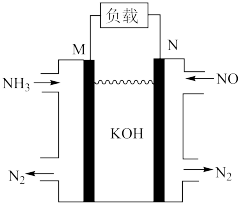


您最近一年使用:0次
名校
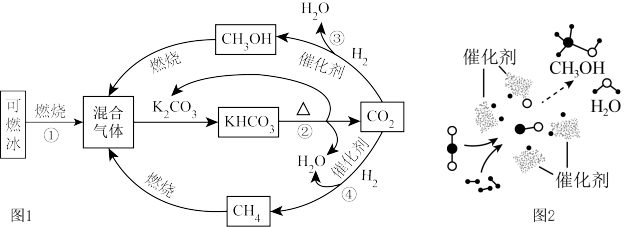
5 . 为解决能源与环境问题,有学者提出如图1所示的含碳物质转化的技术路线。 )完全燃烧的化学方程式为
)完全燃烧的化学方程式为______ 。
(2)反应②属于______ 反应(填基本反应类型)。
(3)我国学者开发促进反应③的一种新型催化剂,催化过程如图2所示。该过程的中间产物______ (填化学式)、氧和氢进一步作用生成甲醇( )和水。
)和水。
(4)反应④的化学方程式为______ 。
(5)该技术路线有利用于实现______ (填字母)。
A.碳循环利用 B.减少碳排放 C.减少白色污染
 )完全燃烧的化学方程式为
)完全燃烧的化学方程式为(2)反应②属于
(3)我国学者开发促进反应③的一种新型催化剂,催化过程如图2所示。该过程的中间产物
 )和水。
)和水。(4)反应④的化学方程式为
(5)该技术路线有利用于实现
A.碳循环利用 B.减少碳排放 C.减少白色污染
您最近一年使用:0次
名校
6 . 含氨污染物治理及其回收利用是重要课题。
(1)用碱液脱硝是目前研究的课题之一。将 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料 。该工艺需控制
。该工艺需控制 和
和 物质的量之比接近
物质的量之比接近 。若
。若 ,则会导致
,则会导致___________ 。若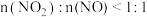 ,则会导致
,则会导致___________ 。
(2)用尿素 (N元素为
(N元素为 价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与
价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与 反应转化成无毒气体,该反应的化学方程式:
反应转化成无毒气体,该反应的化学方程式:___________ 。
(3)工业上在催化剂作用下用 还原工业废气中所含少量
还原工业废气中所含少量 生成
生成 和
和 达到脱除目的,但当温度高于
达到脱除目的,但当温度高于 时,
时, 脱除率下降,原因可能是
脱除率下降,原因可能是___________ 。
(4)用纳米铁粉处理废水中的 :
:
①酸性条件下,纳米铁粉与废水中 反应生成
反应生成 与
与 ,其反应的离子方程式是
,其反应的离子方程式是___________ 。
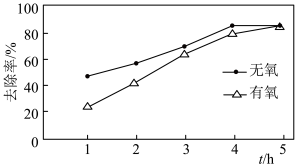
②研究发现,废水中溶解氧会对 的去除产生一定影响。在初始
的去除产生一定影响。在初始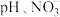 初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下
初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下 的去除率随反应时间的变化如图所示。
的去除率随反应时间的变化如图所示。 时,有氧条件下
时,有氧条件下 去除率低于无氧条件下,其可能的原因是
去除率低于无氧条件下,其可能的原因是___________ 。
(5)将 铜与
铜与 一定浓度的硝酸反应,铜完全溶解,产生的气体为
一定浓度的硝酸反应,铜完全溶解,产生的气体为 和
和 混合气体,其在标准状况下的体积为
混合气体,其在标准状况下的体积为 ,则混合气体中
,则混合气体中 的体积为
的体积为___________ 。(写出计算过程)
(1)用碱液脱硝是目前研究的课题之一。将
 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料 。该工艺需控制
。该工艺需控制 和
和 物质的量之比接近
物质的量之比接近 。若
。若 ,则会导致
,则会导致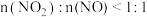 ,则会导致
,则会导致(2)用尿素
 (N元素为
(N元素为 价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与
价)吸收氮氧化物是一种可行的方法。尿素在高温条存下与 反应转化成无毒气体,该反应的化学方程式:
反应转化成无毒气体,该反应的化学方程式:(3)工业上在催化剂作用下用
 还原工业废气中所含少量
还原工业废气中所含少量 生成
生成 和
和 达到脱除目的,但当温度高于
达到脱除目的,但当温度高于 时,
时, 脱除率下降,原因可能是
脱除率下降,原因可能是(4)用纳米铁粉处理废水中的
 :
:①酸性条件下,纳米铁粉与废水中
 反应生成
反应生成 与
与 ,其反应的离子方程式是
,其反应的离子方程式是②研究发现,废水中溶解氧会对
 的去除产生一定影响。在初始
的去除产生一定影响。在初始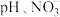 初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下
初始浓度、纳米铁粉与硝酸盐质量比均一定的条件下,有氧与无氧条作下 的去除率随反应时间的变化如图所示。
的去除率随反应时间的变化如图所示。 时,有氧条件下
时,有氧条件下 去除率低于无氧条件下,其可能的原因是
去除率低于无氧条件下,其可能的原因是
(5)将
 铜与
铜与 一定浓度的硝酸反应,铜完全溶解,产生的气体为
一定浓度的硝酸反应,铜完全溶解,产生的气体为 和
和 混合气体,其在标准状况下的体积为
混合气体,其在标准状况下的体积为 ,则混合气体中
,则混合气体中 的体积为
的体积为
您最近一年使用:0次
名校
解题方法
7 . 氮的化合物研究是环境科学的热点课题之一。
金属与不同密度硝酸溶液反应时,还原产物百分比与硝酸密度的关系下图所示:
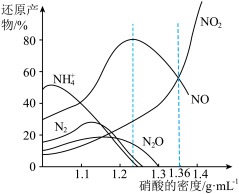
(1)当硝酸溶液的密度为1.36g.cm-3时,下列化学方程式中,能较准确表达Fe与过量硝酸反应的是(填序号)________________ 。
A.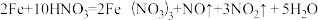
B.
C.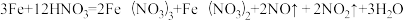
(2)现有一定量铝粉和铜粉的混合物与一定量很稀的硝酸溶液充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入5mo/L的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如下图所示:
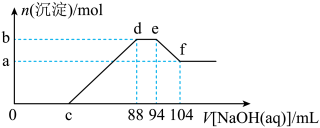
①c点对应NaOH溶液的体积为________________ mL;
②ef段发生反应的离子方程式为________________ 。
(3)研究表明硝酸与金属反应时,最容易生成亚硝酸(HNO2,弱酸),然后才转化成NO2,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的HNO2再氧化成HNO3,如图为金属在不同浓度的HNO3-H2O2混合溶液中的溶解速率和生成NOx的体积V的变化示意图:

①最佳溶解金属的混合溶液中HNO3的质量分数________________ 。
②H2O2与HNO2反应的化学方程式为________________ 。
(4)NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NOx的储存和还原在不同时段交替进行,如图1所示:若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。

①根据图1分析可以得出BaO的作用是________________ 。
②根据图2分析用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,第一步反应的化学方程为________________ 。
③还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有O2条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。请写出该反应的化学方程式________________ 。
金属与不同密度硝酸溶液反应时,还原产物百分比与硝酸密度的关系下图所示:

(1)当硝酸溶液的密度为1.36g.cm-3时,下列化学方程式中,能较准确表达Fe与过量硝酸反应的是(填序号)
A.
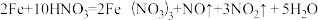
B.

C.
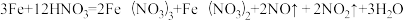
(2)现有一定量铝粉和铜粉的混合物与一定量很稀的硝酸溶液充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入5mo/L的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如下图所示:

①c点对应NaOH溶液的体积为
②ef段发生反应的离子方程式为
(3)研究表明硝酸与金属反应时,最容易生成亚硝酸(HNO2,弱酸),然后才转化成NO2,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的HNO2再氧化成HNO3,如图为金属在不同浓度的HNO3-H2O2混合溶液中的溶解速率和生成NOx的体积V的变化示意图:

①最佳溶解金属的混合溶液中HNO3的质量分数
②H2O2与HNO2反应的化学方程式为
(4)NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NOx的储存和还原在不同时段交替进行,如图1所示:若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。

①根据图1分析可以得出BaO的作用是
②根据图2分析用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,第一步反应的化学方程为
③还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有O2条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。请写出该反应的化学方程式
您最近一年使用:0次
8 . 为了深入探究某个化学问题,往往需要我们会依据一定的原理作出假设,并设计一定的化学实验方案。某化学兴趣小组的同学,对实验室制备氧气的若干问题进行如下探究:
[探究一]为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
(1)写出本实验中反应的化学方程式为___________ ;测量 体积的装置是
体积的装置是___________ (选填下图1中的装置编号)。
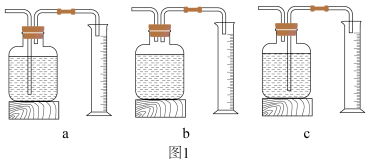
(2)由实验I、Ⅱ、Ⅲ可知:影响双氧水分解速率的因素是:___________
[探究二]B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。于是他们用天平称量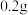 氧化铜,取5%过氧化氢溶液
氧化铜,取5%过氧化氢溶液 于试管中,进行如图2实验:
于试管中,进行如图2实验:
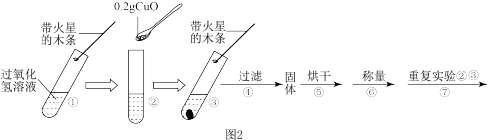
(3)填表:
(4)步骤①的目的是___________ 。
(5)步骤④需用到的玻璃仪器有铁架台(带铁圈)、烧杯、___________ 、___________ 。
(6)步骤⑦中应选用___________ 的过氧化氢溶液。
(7)过氧化氢能将二氧化硫氧化,请写出离子方程式为___________ 。
[探究一]为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
| 双氧水的质量 | 双氧水的浓度 |  的质量 的质量 | 相同时间内产生 的体积 的体积 | |
| I | 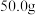 | 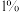 |  |  |
| Ⅱ | 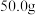 |  |  | 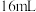 |
| Ⅲ | 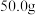 | 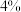 |  | 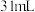 |
(1)写出本实验中反应的化学方程式为
 体积的装置是
体积的装置是
(2)由实验I、Ⅱ、Ⅲ可知:影响双氧水分解速率的因素是:
[探究二]B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。于是他们用天平称量
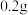 氧化铜,取5%过氧化氢溶液
氧化铜,取5%过氧化氢溶液 于试管中,进行如图2实验:
于试管中,进行如图2实验:
(3)填表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 称得氧化铜的质量为 | 将固体加入盛有过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象。 | 在过氧化氢溶液的分解实验中,氧化铜也能作催化剂。 |
(4)步骤①的目的是
(5)步骤④需用到的玻璃仪器有铁架台(带铁圈)、烧杯、
(6)步骤⑦中应选用
(7)过氧化氢能将二氧化硫氧化,请写出离子方程式为
您最近一年使用:0次
名校
9 . 下列叙述错误的是
| A.由正丁烷(g)→异丁烷(g) △H<0可知,异丁烷比正丁烷稳定 |
| B.常温下,用铁分别与浓、稀硫酸反应探究浓度对化学反应速率的影响 |
| C.冰在室温下自动熔化成水,这是熵增的过程 |
| D.合成氨工业生产中原料气需净化以防止催化剂“中毒” |
您最近一年使用:0次
2023-11-12更新
|
150次组卷
|
2卷引用:陕西省西安市蓝田县城关中学大学区联考2023-2024学年高一下学期3月月考化学试题
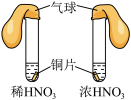
10 . 通过以下实验装置,不能达到实验目的的是
|
|
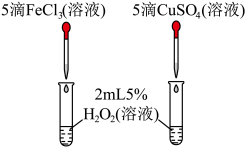
| A.通过气球膨胀速率比较浓硝酸和稀硝酸的氧化性强弱 | B.通过试管中气泡产生速率比较 和 和 的催化效率高低 的催化效率高低 |
|
|
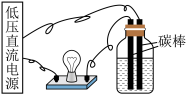
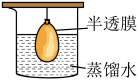
| C.通过小灯泡亮度判断不同浓度NaCl溶液的导电性强弱 | D.通过以上装置分离NaCl溶液和 胶体 胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次