名校
1 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
[实验原理]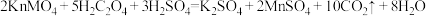
[实验内容及记录]
(1)请完成此实验设计,其中:
_______ ,
_______ 。
(2)实验①、②探究的是_______ 对化学反应速率的影响,根据表中的实验数据,可以得到的结论是_______ 。
(3)探究温度对化学反应速率的影响,应选择_______ (填实验编号)。
(4)该小组同学根据经验绘制了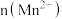 随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中
随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中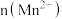 随时间变化的实际趋势如图乙所示。
随时间变化的实际趋势如图乙所示。

该小组同学根据图乙所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
①该小组同学提出的假设是_______ 。
②能佐证该假设成立的实验证据是_______ 。
[实验原理]
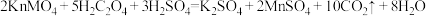
| 实验编号 | 实验温度/℃ | 试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
0.6mol/L 溶液 溶液 |  | 3mol/L稀 溶液 溶液 | 0.05mol/L 溶液 溶液 | |||
| ① | 25 | 3.0 |  | 2.0 | 3.0 | 1.5 |
| ② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| ③ | 50 | 2.0 |  | 2.0 | 3.0 | 1.7 |
(1)请完成此实验设计,其中:


(2)实验①、②探究的是
(3)探究温度对化学反应速率的影响,应选择
(4)该小组同学根据经验绘制了
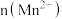 随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中
随时间变化的趋势如图甲所示,但有同学查阅已有的实验资料发现该实验过程中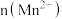 随时间变化的实际趋势如图乙所示。
随时间变化的实际趋势如图乙所示。
该小组同学根据图乙所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
| 实验编号 | 实验温度/℃ | 试管中所加试剂及其用量 | 再向试管中加入某种固体 | 溶液褪至无色所需时间/min | |||
0.6mol/L 溶液 溶液 |  | 3mol/L稀 溶液 溶液 | 0.05mol/L 溶液 溶液 | ||||
| ④ | 25 | 2.0 | 3.0 | 2.0 | 3.0 |  | t |
②能佐证该假设成立的实验证据是
您最近一年使用:0次
名校
解题方法
2 . “一锅法”用三氧化钉(RuCl3)催化硝基苯(PhNO2,Ph—表示苯基)与醇(RCH2OH)反应生成仲胺(RCH2NHPh)的反应过程如图所示,[Ru]表示催化剂。下列叙述错误的是
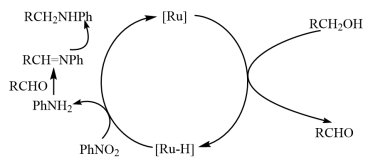

| A.RCHO是中间体,不是产物 |
| B.存在反应PhNH2+RCHO→RCH=NPh+H2O |
| C.还原反应的氢均来自RCH2OH |
| D.反应过程中Ru的成键数目有变化 |
您最近一年使用:0次
名校
解题方法
3 . 自然界中时刻存在着氮的转化。实现氮按照一定方向转化一直是科学领域研究的重要课题,如图为N2分子在催化剂的作用下发生的一系列转化示意图:
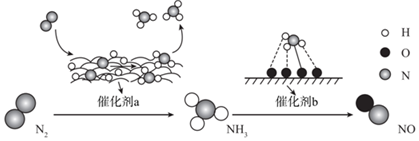
下列叙述正确的是

下列叙述正确的是
| A.N2→NH3,NH3→NO均属于氮的固定 |
| B.催化剂a作用下氮原子发生了氧化反应 |
| C.催化剂a、b表面均未发生共价键的断裂 |
| D.使用催化剂a、b均可以提高单位时间内生成物的产量 |
您最近一年使用:0次
2021-05-28更新
|
273次组卷
|
11卷引用:福建省福州市第三中学2021届高三上学期第四次质量检测化学试题
福建省福州市第三中学2021届高三上学期第四次质量检测化学试题广东省深圳、汕头、潮州、揭阳名校2021届高三12月联考化学试题山西省临汾市2020-2021学年高一下学期4月联考质量检测化学试题(已下线)【浙江新东方】高中化学20210513-042【2021】【高二下】浙江省杭州高级中学2021届高三上学期期中考试化学试题河南省焦作市博爱英才学校2021届高三开学考试化学试题(已下线)【浙江新东方】116(已下线)练习13 共价键-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)(已下线)专题03 化学键【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版必修2)安徽省亳州市第二中学2020-2021学年高一下学期期末考试化学试题江西省宁冈中学2020-2021学年高二上学期期中考试化学试题
名校
4 . 取50 mL过氧化氢水溶液,在少量I−存在下分解:2H2O2=2H2O+O2↑。在一定温度下,测得O2的放出量,转换成H2O2的物质的量浓度(c),如下表:
下列说法不正确 的是
| t/min | 0 | 20 | 40 | 60 | 80 |
| c/(mol·L−1) | 0.80 | a | 0.20 | 0.10 | 0.050 |
| A.反应20 min时,测得O2体积为224 mL(标准状况),则a=0.40 |
| B.第30 min时的瞬时速率大于第40 min时的瞬时速率 |
| C.60~80 min,H2O2分解的平均速率为0.0050 mol·(L·min)−1 |
| D.MnO2和FeCl3对H2O2的分解也有催化作用 |
您最近一年使用:0次
2021-04-13更新
|
380次组卷
|
2卷引用:福建省福州市闽侯县第一中学2023-2024学年高一下学期3月月考化学试题
名校
5 . 甲硫醇是一种重要的原料和化工试剂,硫化氢与甲醇合成甲硫醇的催化过程如下。下列说法中不正确 的是
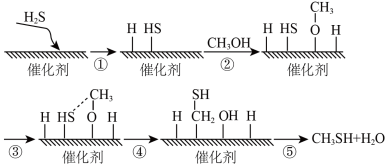

| A.过程①吸收能量 |
| B.过程④中,形成了O—H键和C—S键 |
| C.该催化剂可降低反应活化能从而有效提高反应物的平衡转化率 |
| D.硫化氢与甲醇合成甲硫醇的反应类型为取代反应 |
您最近一年使用:0次
2020-11-10更新
|
406次组卷
|
6卷引用:福建省平潭翰英中学2021-2022学年高三上学期第一次月考化学试题
福建省平潭翰英中学2021-2022学年高三上学期第一次月考化学试题江西省南昌市第二中学2021届高三上学期第四次考试化学试题(已下线)【南昌新东方】2. 2020 高三 南昌二中第三次考试 左佳鑫江西省上高二中2022届高三第二次月考化学试卷河北省张家口市宣化第一中学2021-2022学年高三上学期12月月考化学试题(已下线)小题必刷28 化学平衡及平衡移动——2021年高考化学一轮复习小题必刷(通用版本)
11-12高一·浙江温州·期中
名校
6 . 为了说明影响化学反应快慢的因素,某同学分别设计了如下A~D四个实验,你认为结论不正确的是( )
| A.将大小、形状相同的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大 |
| B.在相同条件下,等质量的大理石块和大理石粉与相同浓度的盐酸反应,大理石粉反应快 |
| C.将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解 |
| D.两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
您最近一年使用:0次
2020-06-23更新
|
524次组卷
|
17卷引用:福建省福州市福清市虞阳中学2022-2023学年下学期高一年第一次月考化学试卷
福建省福州市福清市虞阳中学2022-2023学年下学期高一年第一次月考化学试卷2015-2016学年河北省定州中学高一6月月考化学试卷辽宁省锦州市黑山县黑山中学2019-2020学年高一6月质量检测化学试题(已下线)2011-2012年浙江温州龙湾中学高一期中考试理科化学试卷(已下线)2013-2014安徽省安庆一中、合肥六中第二学期期末联考高一化学试卷2014-2015学年宁夏银川唐徕回民中学高一下期末化学试卷2015-2016学年湖南省邵阳市邵东三中高一下期中化学试卷【全国百强校】黑龙江省哈尔滨市第六中学2017-2018学年高一下学期期中(5月)考试化学试题2018-2019学年苏教版高中化学必修二:专题综合测评2 化学反应与能量转化人教版高中化学必修2模块综合测试题青海省西宁市大通回族土族自治县第一完全中学2019-2020学年高一下学期期中考试化学试题云南省昆明市禄劝彝族苗族自治县第一中学2019-2020学年高一下学期期中考试化学(理科)试题湖南省邵阳市隆回县2019-2020学年高一下学期期末考试化学试题(已下线)6.2.1 化学反应速率(练好题)(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)山东省淄博市沂源县第二中学2020-2021学年高一下学期期中考试化学试题江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高二下学期期中考试化学试题山西省侯马市第一中学校2021-2022年高二上学期期中测试化学试题
12-13高二上·江苏南通·阶段练习
名校
7 . 为探究Fe3+和Cu2+对H2O2分解反应的催化效果,某同学分别设计了图1、图2所示的实验。下列叙述中不正确的是( )
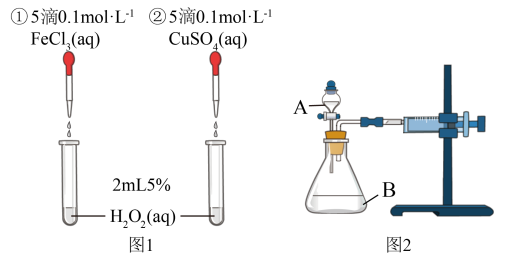

| A.图2中的A为分液漏斗 |
| B.图2实验可通过测定相同状况下产生的气体体积与反应时间来比较反应速率 |
| C.若图1实验中反应速率为①>②,则Fe3+对H2O2分解的催化效果一定比Cu2+好 |
| D.图1实验可通过观察产生气泡的快慢来比较反应速率 |
您最近一年使用:0次
2019-12-16更新
|
512次组卷
|
11卷引用:福建省南安市侨光中学2019-2020学年高二上学期第二次阶段考试化学试题
福建省南安市侨光中学2019-2020学年高二上学期第二次阶段考试化学试题(已下线)2011-2012学年江苏省启东中学高二上学期第二次月考化学(理)试卷2016-2017学年江西省宜春市奉新一中高二上月考二化学卷浙江省温州市求知中学2018-2019学年高二下学期第二次月考化学试题(已下线)【浙江新东方】43浙江省磐安县第二中学2019-2020学年高二上学期期中考试化学试题(已下线)考点12 化学反应速率化学平衡——《备战2020年高考精选考点专项突破题集》浙江省杭州地区七校2019-2020学年高二上学期期中考试理综化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第3节 化学反应的速率 高效手册黑龙江省哈尔滨市第六中学2020-2021学年高二下学期开学考试化学试题(已下线)专题25 化学实验综合性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
名校
8 . 碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)查阅资料得知,反应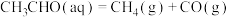 在含有少量
在含有少量 的溶液中分两步进行:第I步反应为
的溶液中分两步进行:第I步反应为 (慢反应),第II步为快反应。增大
(慢反应),第II步为快反应。增大 的浓度
的浓度___________ (填“能”或“不能”)明显增大总反应的平均速率,理由为______________________________ 。
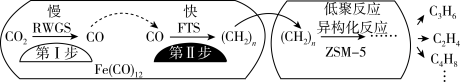
(2)用催化剂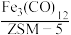 催化
催化 加氢合成乙烯的反应,所得产物含
加氢合成乙烯的反应,所得产物含 、
、 、
、 等副产物,反应过程如图。
等副产物,反应过程如图。
催化剂中添加 、K、
、K、 助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得
助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得 转化率和各产物的物质的量分数如表。
转化率和各产物的物质的量分数如表。
欲提高单位时间内乙烯的产量,在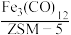 中添加
中添加__________ 助剂效果最好;加入助剂能提高单位时间内乙烯产量的根本原因是__________ 。
a.明显降低了该体系中所有反应的活化能
b.降低了生成乙烯反应的焓变值使反应趋势增大
c.降低了 转化率
转化率
d.明显降低了生成乙烯反应的活化能,对其他反应几乎无影响
(3)在一密闭容器中,起始时向该容器中充入 和
和 且
且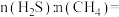 2:1,发生反应:
2:1,发生反应:
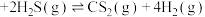 。0.11
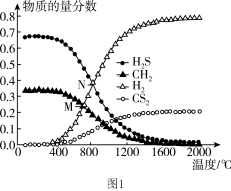
。0.11 时,温度变化对平衡时产物的物质的量分数的影响如图1所示:为提高
时,温度变化对平衡时产物的物质的量分数的影响如图1所示:为提高 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是__________ (列举一条)。
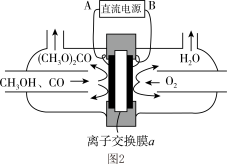
(4)合成碳酸二甲酯的工作原理如图2所示。阳极的电极反应式为__________ ,离子交换膜a为__________ (填“阳膜”、“阴膜”)。
(1)查阅资料得知,反应
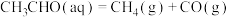 在含有少量
在含有少量 的溶液中分两步进行:第I步反应为
的溶液中分两步进行:第I步反应为 (慢反应),第II步为快反应。增大
(慢反应),第II步为快反应。增大 的浓度
的浓度(2)用催化剂
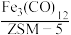 催化
催化 加氢合成乙烯的反应,所得产物含
加氢合成乙烯的反应,所得产物含 、
、 、
、 等副产物,反应过程如图。
等副产物,反应过程如图。
催化剂中添加
 、K、
、K、 助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得
助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得 转化率和各产物的物质的量分数如表。
转化率和各产物的物质的量分数如表。助剂 |
| 各产物在所有产物中的占比(%) | ||
|
| 其他 | ||
| 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
| 9.8 | 80.7 | 12.5 | 6.8 |
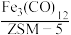 中添加
中添加a.明显降低了该体系中所有反应的活化能
b.降低了生成乙烯反应的焓变值使反应趋势增大
c.降低了
 转化率
转化率d.明显降低了生成乙烯反应的活化能,对其他反应几乎无影响
(3)在一密闭容器中,起始时向该容器中充入
 和
和 且
且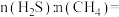 2:1,发生反应:
2:1,发生反应:
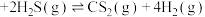 。0.11
。0.11 时,温度变化对平衡时产物的物质的量分数的影响如图1所示:为提高
时,温度变化对平衡时产物的物质的量分数的影响如图1所示:为提高 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是
(4)合成碳酸二甲酯的工作原理如图2所示。阳极的电极反应式为

您最近一年使用:0次
名校
9 . 对于二氧化硫与氧气化合生成三氧化硫的反应,下列说法错误的是
| A.降低温度会使反应速率降低 |
| B.使用合适的催化剂能使反应速率加大 |
C.增大压强能使 完全转化为 完全转化为 |
D.达到平衡状态时,仍有 与 与 反应生成 反应生成 |
您最近一年使用:0次
2023-04-19更新
|
132次组卷
|
2卷引用:福建省福州第三中学2022-2023学年高一下学期3月月考化学试题
名校
解题方法
10 . 完成下列问题
(1)向某体积固定的密闭容器中加入0.3molA、0.1molC和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。
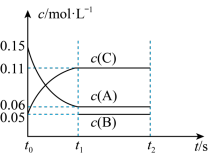
已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
①若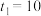 ,则
,则 内反应速率
内反应速率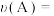
_______ 。
②写出该反应的化学方程式:________ 。
(2)已知部分化学键的键能如表:
①已知生成1mol 放出46kJ热量,则
放出46kJ热量,则
____ 。
②已知工业合成氨反应 ,在恒温(200℃)、恒容条件下,下列描述能作为判断t时刻合成氨反应达到化学平衡状态的依据有
,在恒温(200℃)、恒容条件下,下列描述能作为判断t时刻合成氨反应达到化学平衡状态的依据有____ (填序号)。
A.t时刻N2、H2、NH3的浓度不再改变
B.t时刻及其前后容器内气体的密度不再改变
C.t时刻及其前后容器内气体的平均相对分子质量相等
D.t时刻断裂的H−H键数目和生成的N−H键数目相等
③不同催化剂下合成氨反应的历程如下图所示,吸附在催化剂表面的物质用“*”表示。催化剂的催化效果更好的是____ (填“A”或“B”)。

(1)向某体积固定的密闭容器中加入0.3molA、0.1molC和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。
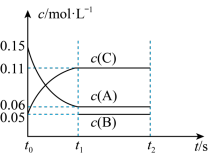
已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
①若
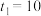 ,则
,则 内反应速率
内反应速率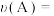
②写出该反应的化学方程式:
(2)已知部分化学键的键能如表:
| 化学键 | N≡N | H−H | N−H |
键能/( ) ) | 946 | 436 | a |
 放出46kJ热量,则
放出46kJ热量,则
②已知工业合成氨反应
 ,在恒温(200℃)、恒容条件下,下列描述能作为判断t时刻合成氨反应达到化学平衡状态的依据有
,在恒温(200℃)、恒容条件下,下列描述能作为判断t时刻合成氨反应达到化学平衡状态的依据有A.t时刻N2、H2、NH3的浓度不再改变
B.t时刻及其前后容器内气体的密度不再改变
C.t时刻及其前后容器内气体的平均相对分子质量相等
D.t时刻断裂的H−H键数目和生成的N−H键数目相等
③不同催化剂下合成氨反应的历程如下图所示,吸附在催化剂表面的物质用“*”表示。催化剂的催化效果更好的是

您最近一年使用:0次




