名校
1 . 在恒容密闭容器中,用铜铬的氧化物作催化剂,用一定量的HCl(g)和O2制取Cl2的原理为:4HCl(g)+O2(g)  2Cl2(g)+2H2O(g) ΔH<0。下列有关说法不正确的是
2Cl2(g)+2H2O(g) ΔH<0。下列有关说法不正确的是
 2Cl2(g)+2H2O(g) ΔH<0。下列有关说法不正确的是
2Cl2(g)+2H2O(g) ΔH<0。下列有关说法不正确的是| A.平衡前,随着反应的进行,容器内压强变小 |
| B.平衡时,其他条件不变,分离出H2O(g),逆反应速率减小 |
| C.平衡时,其他条件不变,升高温度平衡常数增大 |
| D.其他条件不变,使用不同催化剂,HCl(g)的转化率不变 |
您最近一年使用:0次
2017-03-11更新
|
370次组卷
|
6卷引用:上海市黄浦区2016届高三4月第二次模拟考试化学试题
解题方法
2 . 亚氯酸钠(NaClO2)是一种性能优良的漂白剂,但在酸性溶液发生分解:
5HClO2→4ClO2+H++Cl-+2H2O.
向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为pH相同的稀硫酸,开始时反应缓慢,稍后产生气体速度较快,速度变化的原因是
5HClO2→4ClO2+H++Cl-+2H2O.
向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为pH相同的稀硫酸,开始时反应缓慢,稍后产生气体速度较快,速度变化的原因是
| A.逸出ClO2使生成物浓度降低 | B.酸使HClO2的分解加速 |
| C.溶液中的H+起催化作用 | D.溶液中的Cl-起催化作用 |
您最近一年使用:0次
2014高三·全国·专题练习
3 . 某反应在反应过程中的能量变化如图所示(图中E1表示反应物总能量,E2表示生成物总能量)。下列有关叙述正确的是( )
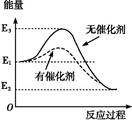

| A.该反应为吸热反应 |
| B.使用催化剂没有改变反应的反应热 |
| C.反应热等于E3-E2 |
| D.催化剂只对正反应有催化作用,对逆反应无催化作用 |
您最近一年使用:0次
13-14高三上·上海宝山·期末
解题方法
4 . 已知反应:3I-(aq)+S2O82-(aq) I3-(aq)+2SO42-(aq)+Q
I3-(aq)+2SO42-(aq)+Q
(1)写出反应的平衡常数表达式:K=______________ 。
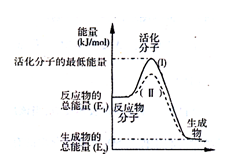
(2)如图表示反应过程中有关物质的能量,则反应过程中的Q_____ 0(填>、<、=);(I)、(II)两曲线中,使用催化剂的是______ 曲线。
(3)反应的速率可以用I3-与加入的淀粉溶液反应显蓝色的时间t来度量,t越小,反应速率越大。下表是在20℃进行实验时所记录的数据
从表中数据分析,该实验的目的是___________________________________________ ;
表中显色时间t1=_____ s;最终得出的结论是__________________________________ 。
 I3-(aq)+2SO42-(aq)+Q
I3-(aq)+2SO42-(aq)+Q(1)写出反应的平衡常数表达式:K=
(2)如图表示反应过程中有关物质的能量,则反应过程中的Q

(3)反应的速率可以用I3-与加入的淀粉溶液反应显蓝色的时间t来度量,t越小,反应速率越大。下表是在20℃进行实验时所记录的数据
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-)/mol·L-1 | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
从表中数据分析,该实验的目的是
表中显色时间t1=
您最近一年使用:0次
13-14高三下·广东·阶段练习
解题方法
5 . 下列实验操作或事实与预期实验目的或所得结论一致的是
| 选项 | 实验操作或事实 | 实验目的或结论 |
| A | 取少量试液于试管中,加入用HNO3酸化的BaCl2溶液,产生白色沉淀 | 说明试液中一定含有SO42- |
| B | 分别向两支试管中加入等体积、等浓度的过氧化氢溶液,再在其中一支试管中加入少量MnO2 | 研究催化剂对过氧化氢分解速率的影响 |
| C | 将NaHCO3与HCl两种溶液相互滴加 | 可以鉴别这两种溶液 |
| D | C2H5Br与AgNO3溶液混合加热 | 检验C2H5Br中的溴元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



