名校
1 . 炼油、石化等工业会产生含硫(-2价)废水,处理的方法有沉淀法、氧化法。
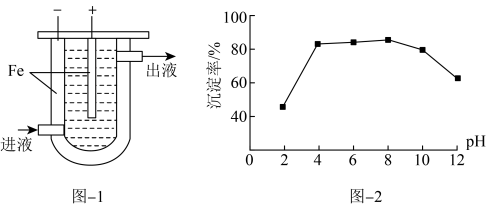
Ⅰ.沉淀法。用如下图-1装置可以将废水中的硫转化为FeS沉淀。控制其他条件一定,测得出口处硫转化为FeS的沉淀率与溶液pH的关系如题图-2所示。
(2)该装置沉淀废水中的硫(-2价)的原理可描述为_______ 。
(3) 时,pH越大,硫转化为FeS的沉淀率越低,可能的原因是_______。
时,pH越大,硫转化为FeS的沉淀率越低,可能的原因是_______。
Ⅱ.氧化法。 氧化法、
氧化法、 氧化法、催化氧化法等可以将含硫废水中硫元素氧化。
氧化法、催化氧化法等可以将含硫废水中硫元素氧化。
i. 氧化法:向含
氧化法:向含 的废水中,加入一定量的
的废水中,加入一定量的 溶液,控制溶液的pH为5,可以生成S沉淀。
溶液,控制溶液的pH为5,可以生成S沉淀。
(4)写出该反应的离子方程式:_______ 。
ii. 氧化法:向含
氧化法:向含 的废水中,加入
的废水中,加入 溶液,其他条件一定,测得硫(-2价)的去除率、S(单质)的生成率与所加
溶液,其他条件一定,测得硫(-2价)的去除率、S(单质)的生成率与所加 溶液体积的关系如题图-3所示。
溶液体积的关系如题图-3所示。
(6)当所加 溶液体积大于9mL时,所加
溶液体积大于9mL时,所加 溶液越多,S生成率越低,原因是
溶液越多,S生成率越低,原因是____ 。
iii.催化氧化法: 苯胺(
苯胺( 为催化剂、聚苯胺为催化剂载体)可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如题图-4所示。
为催化剂、聚苯胺为催化剂载体)可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如题图-4所示。_______ 。
(8)催化剂使用一段时间后催化效率会下降,结合图中相关信息,分析可能原因为_______ ,要使催化剂恢复催化效率,处理的方法是用氯仿( )浸取催化剂,再干燥即可。
)浸取催化剂,再干燥即可。
Ⅰ.沉淀法。用如下图-1装置可以将废水中的硫转化为FeS沉淀。控制其他条件一定,测得出口处硫转化为FeS的沉淀率与溶液pH的关系如题图-2所示。
A.负极: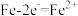 | B.阳极: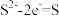 |
C.正极: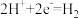 | D.阴极: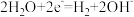 |
(2)该装置沉淀废水中的硫(-2价)的原理可描述为
(3)
 时,pH越大,硫转化为FeS的沉淀率越低,可能的原因是_______。
时,pH越大,硫转化为FeS的沉淀率越低,可能的原因是_______。A.pH越大, 越高, 越高, 与 与 结合转化为 结合转化为 逸出 逸出 |
B.pH越大, 越低,废水中 越低,废水中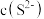 低,则FeS的沉淀率越低 低,则FeS的沉淀率越低 |
C.pH越大,废水中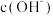 越高, 越高, 与 与 生成 生成 ,导致 ,导致 浓度越小,废水中 浓度越小,废水中 与 与 结合FeS沉淀的硫的量越少 结合FeS沉淀的硫的量越少 |
D.pH越大,废水中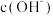 越低,废水中 越低,废水中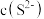 低, 低, 与 与 结合FeS沉淀量越少 结合FeS沉淀量越少 |
Ⅱ.氧化法。
 氧化法、
氧化法、 氧化法、催化氧化法等可以将含硫废水中硫元素氧化。
氧化法、催化氧化法等可以将含硫废水中硫元素氧化。i.
 氧化法:向含
氧化法:向含 的废水中,加入一定量的
的废水中,加入一定量的 溶液,控制溶液的pH为5,可以生成S沉淀。
溶液,控制溶液的pH为5,可以生成S沉淀。(4)写出该反应的离子方程式:
ii.
 氧化法:向含
氧化法:向含 的废水中,加入
的废水中,加入 溶液,其他条件一定,测得硫(-2价)的去除率、S(单质)的生成率与所加
溶液,其他条件一定,测得硫(-2价)的去除率、S(单质)的生成率与所加 溶液体积的关系如题图-3所示。
溶液体积的关系如题图-3所示。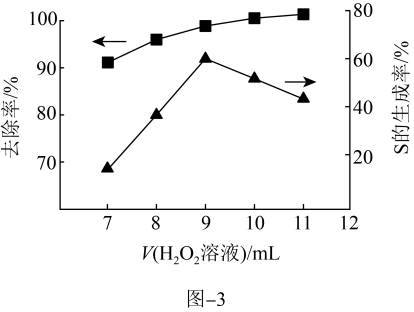
A.加 溶液就是将 溶液就是将 氧化为单质S 氧化为单质S |
B.随着 溶液的不断加入,废水中硫元素的去除率一直在升高 溶液的不断加入,废水中硫元素的去除率一直在升高 |
C. 溶液加入量越多,废水中含硫量越低 溶液加入量越多,废水中含硫量越低 |
D. 在处理一定量的废水中,其加入量不同氧化产物可能有差异 在处理一定量的废水中,其加入量不同氧化产物可能有差异 |
(6)当所加
 溶液体积大于9mL时,所加
溶液体积大于9mL时,所加 溶液越多,S生成率越低,原因是
溶液越多,S生成率越低,原因是iii.催化氧化法:
 苯胺(
苯胺( 为催化剂、聚苯胺为催化剂载体)可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如题图-4所示。
为催化剂、聚苯胺为催化剂载体)可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如题图-4所示。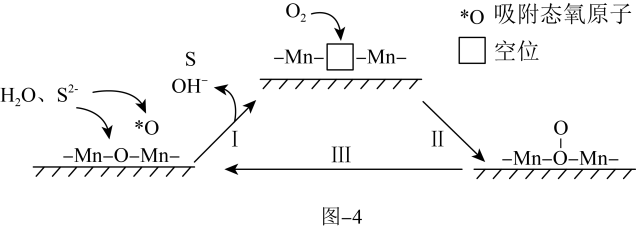
(8)催化剂使用一段时间后催化效率会下降,结合图中相关信息,分析可能原因为
 )浸取催化剂,再干燥即可。
)浸取催化剂,再干燥即可。
您最近一年使用:0次
解题方法
2 . Ⅰ.二氧化硫可用于“接触法制硫酸”,核心反应是2SO2+O2 2SO3,因SO2在催化剂表面与O2接触而得名,反应过程示意图如下:
2SO3,因SO2在催化剂表面与O2接触而得名,反应过程示意图如下:
Ⅱ.也可以用电化学原理,使用SO2制备硫酸,同时精制粗铜,装置如图所示。电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触,质子交换膜只允许H+通过。___________ ,与___________ (填“精铜”或“粗铜”)连接;
(3)假设粗铜中含有铁、锌杂质,工作一段时间后CuSO4溶液中的Cu2+浓度___________ (填“不变”或“增大”“减小”)。
 2SO3,因SO2在催化剂表面与O2接触而得名,反应过程示意图如下:
2SO3,因SO2在催化剂表面与O2接触而得名,反应过程示意图如下: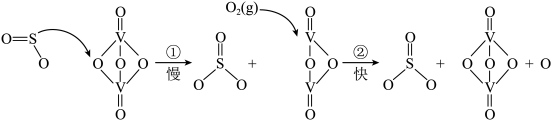
| A.SO2和SO3都属于酸性氧化物,通到BaCl2溶液中都会产生白色沉淀 |
| B.增大O2的浓度可以明显提高SO3的生成速率 |
| C.图示过程中既有V-O键的断裂又有V-O键的形成 |
| D.V2O5的作用是降低该反应的活化能,提高SO2的平衡转化率 |
Ⅱ.也可以用电化学原理,使用SO2制备硫酸,同时精制粗铜,装置如图所示。电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触,质子交换膜只允许H+通过。
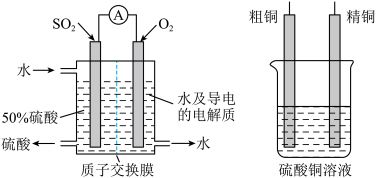
(3)假设粗铜中含有铁、锌杂质,工作一段时间后CuSO4溶液中的Cu2+浓度
您最近一年使用:0次
3 . 化学在治理空气污染方面发挥着重要的作用,将污染气体吸收或转化为对环境友好的气体是环境科学研究的热点。
Ⅰ、工业制硫酸中尾气SO2的处理。
1.SO2分子的空间结构为_____ ;SO2的键角_____ H2O(选填“>”或“<”)
2.下图是工业制硫酸中的转化器,有关说法正确的是_____。(不定项)
利用活性炭催化可去除尾气中SO2,并使其“热再生”,机理如下图1(*代表吸附态)。_____ 。
Ⅱ、N2O的转化
在Fe+催化作用下与CO发生反应:N2O(g)+CO(g) N2(g)+CO2(g)
N2(g)+CO2(g)
4.该反应分两步进行,第一步:Fe++N2O FeO++N2,则第二步反应为
FeO++N2,则第二步反应为_____ 。已知第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第一步反应的活化能_____ (选填“>”“<”或“=”)第二步反应的活化能。
Ⅰ、工业制硫酸中尾气SO2的处理。
1.SO2分子的空间结构为
2.下图是工业制硫酸中的转化器,有关说法正确的是_____。(不定项)
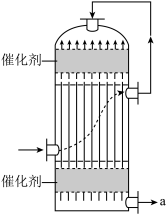
| A.该装置能充分利用热能 |
| B.进入转化器气体要净化操作 |
| C.温度475℃,此时SO2转化率最大 |
| D.该装置a端出来的气体只有SO3 |
利用活性炭催化可去除尾气中SO2,并使其“热再生”,机理如下图1(*代表吸附态)。
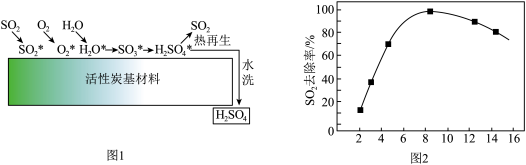
Ⅱ、N2O的转化
在Fe+催化作用下与CO发生反应:N2O(g)+CO(g)
 N2(g)+CO2(g)
N2(g)+CO2(g)4.该反应分两步进行,第一步:Fe++N2O
 FeO++N2,则第二步反应为
FeO++N2,则第二步反应为
您最近一年使用:0次
解题方法
4 . 在铜、银催化下,乙烯与氧气反应生成环氧乙烷( )和乙醛,下图是该反应的部分历程。
)和乙醛,下图是该反应的部分历程。

(2)鉴别以上产物乙醛和环氧乙烷可以用___________。
| A.原子发射光谱 | B.原子吸收光谱 | C.核磁共振氢谱 | D.红外光谱 |
(3)以下电子排布式和价电子轨道表示式中,正确且对应微粒为基态原子的是___________。
A.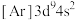 | B.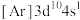 |
C. | D.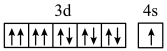 |
(4)已知
 的熔点为1235℃,
的熔点为1235℃, 的熔点为1130℃,二者晶体结构类似,且熔点都较高,但
的熔点为1130℃,二者晶体结构类似,且熔点都较高,但 熔点比
熔点比 高,其原因是
高,其原因是(5)
 晶胞结构如图所示,其中
晶胞结构如图所示,其中 代表的原子是
代表的原子是 ,晶胞参数为a pm,则阿伏加德罗常数值
,晶胞参数为a pm,则阿伏加德罗常数值
 和a的代数式表示)
和a的代数式表示)
 可以形成一种配位化合物,其结构如下图所示。以下说法正确的是___________。
可以形成一种配位化合物,其结构如下图所示。以下说法正确的是___________。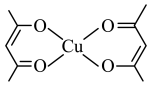
A. 的配位数是2 的配位数是2 |
| B.此配合物中存在配位键、极性键、非极性键 |
| C.配体中O原子提供空轨道 |
D. 提供孤电子对 提供孤电子对 |
(7)已知:常温下,①
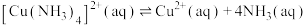
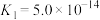 ;
;②


则常温下
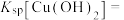
您最近一年使用:0次
5 . 与氨气相关的化学变化是氮循环和转化的重要一环,对生产、生活有重要的价值。
(1)下图转化途径中属于“固氮”的是___________。

(2)合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中 表示物质吸附在催化剂表面时的状态)
表示物质吸附在催化剂表面时的状态)

①由图可知合成氨反应 的
的
___________  ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤___________ 。(填写编号)
②若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是___________ 。
A.升高温度,使单位体积内活化分子百分数增加
B.增加反应物的浓度,使单位体积内活化分子百分数增加
C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加
D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加
(3)氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用 的燃烧反应(
的燃烧反应( )能设计成燃料电池,其工作原理如图所示。电极
)能设计成燃料电池,其工作原理如图所示。电极 为
为___________ (选填“正”或“负”)极;电极 的电极反应式为
的电极反应式为___________ ;当正负极共消耗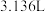 (标准状况)气体时,通过负载的电子数为
(标准状况)气体时,通过负载的电子数为___________ 个。

合成氨厂的可用于合成重要化工原料 ,主要反应为:
,主要反应为: ,向两个容积固定为
,向两个容积固定为 的密闭容器中分别充入比例相同,但总量不同的
的密闭容器中分别充入比例相同,但总量不同的 和气体,
和气体, 的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
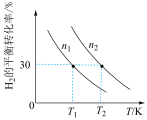
(4)①若 时,向容器中充入
时,向容器中充入 气体(
气体( 和
和 ),反应至
),反应至 时达到平衡,则
时达到平衡,则 内
内 的平均反应速率
的平均反应速率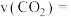
___________ 。
②由上图可判断该反应是___________ (选填“吸热”或“放热”)反应,在___________ (填“较高”或“较低”)温度下有利于该反应自发进行。
③判断图中 、
、 相对大小,并说明理由。
相对大小,并说明理由。___________ 。
(1)下图转化途径中属于“固氮”的是___________。

| A.④⑤⑥ | B.①③④ | C.①⑤⑦ | D.②⑧⑨ |
(2)合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中
 表示物质吸附在催化剂表面时的状态)
表示物质吸附在催化剂表面时的状态)
①由图可知合成氨反应
 的
的
 ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤②若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是
A.升高温度,使单位体积内活化分子百分数增加
B.增加反应物的浓度,使单位体积内活化分子百分数增加
C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加
D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加
(3)氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用
 的燃烧反应(
的燃烧反应( )能设计成燃料电池,其工作原理如图所示。电极
)能设计成燃料电池,其工作原理如图所示。电极 为
为 的电极反应式为
的电极反应式为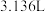 (标准状况)气体时,通过负载的电子数为
(标准状况)气体时,通过负载的电子数为
合成氨厂的可用于合成重要化工原料
 ,主要反应为:
,主要反应为: ,向两个容积固定为
,向两个容积固定为 的密闭容器中分别充入比例相同,但总量不同的
的密闭容器中分别充入比例相同,但总量不同的 和气体,
和气体, 的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
(4)①若
 时,向容器中充入
时,向容器中充入 气体(
气体( 和
和 ),反应至
),反应至 时达到平衡,则
时达到平衡,则 内
内 的平均反应速率
的平均反应速率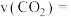
②由上图可判断该反应是
③判断图中
 、
、 相对大小,并说明理由。
相对大小,并说明理由。
您最近一年使用:0次
6 . “氢经济”是“双碳”转型中非常关键的一环。大量安全制氢是关键技术之一。
方法一:工业上常用甲烷、水蒸气重整制备氢气,体系中发生如下反应:
反应①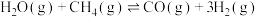
反应②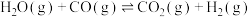
(1)下列操作中,能提高 平衡转化率的是_____。(双选)
平衡转化率的是_____。(双选)
(2)恒温条件下,1L密闭容器中, 和
和 反应达平衡时,
反应达平衡时, 的转化率为
的转化率为 ,
, 的物质的量为
的物质的量为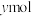 ,则反应①的平衡常数
,则反应①的平衡常数
_____ 。(用 、
、 表示)
表示)
方法二:用与 制备
制备 可以同时实现资源化利用,其反应历程如下:
可以同时实现资源化利用,其反应历程如下:
反应①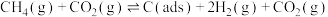
反应②
已知: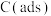 为吸附型活性炭。
为吸附型活性炭。
(3)使用不同催化剂时,相同时间内测得 的转化率随温度的变化如下图所示:
的转化率随温度的变化如下图所示:

催化效果最佳的是催化剂_____ (选填“Ⅰ”、“Ⅱ”或“Ⅲ”),b点的
_____  (选填“>”、“<”或“=”),c点转化率比a点低的可能原因是
(选填“>”、“<”或“=”),c点转化率比a点低的可能原因是_____ 。(任写一点)
方法一:工业上常用甲烷、水蒸气重整制备氢气,体系中发生如下反应:
反应①
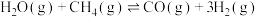
反应②
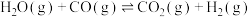
(1)下列操作中,能提高
 平衡转化率的是_____。(双选)
平衡转化率的是_____。(双选)A.增大 的浓度 的浓度 | B.分离出 |
| C.恒温恒压下通入惰性气体 | D.加入催化剂 |
(2)恒温条件下,1L密闭容器中,
 和
和 反应达平衡时,
反应达平衡时, 的转化率为
的转化率为 ,
, 的物质的量为
的物质的量为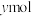 ,则反应①的平衡常数
,则反应①的平衡常数
 、
、 表示)
表示)方法二:用与
 制备
制备 可以同时实现资源化利用,其反应历程如下:
可以同时实现资源化利用,其反应历程如下:反应①
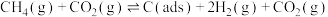
反应②

已知:
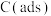 为吸附型活性炭。
为吸附型活性炭。(3)使用不同催化剂时,相同时间内测得
 的转化率随温度的变化如下图所示:
的转化率随温度的变化如下图所示:
催化效果最佳的是催化剂

 (选填“>”、“<”或“=”),c点转化率比a点低的可能原因是
(选填“>”、“<”或“=”),c点转化率比a点低的可能原因是
您最近一年使用:0次
7 . CO2和CH4都是温室气体。一定条件下,CH4和CO2以镍合金为催化剂,发生反应:CO2(g)+CH4(g) 2CO(g)+2H2(g)。完成下列填空。
2CO(g)+2H2(g)。完成下列填空。
(1)甲烷分子的空间构型是_______ ,干冰的晶体类型是_______ 。
(2)该反应的化学平衡常数表达式为K=_______ 。不同温度下,K的数值如下:
该反应的逆反应是_______ 反应(填“吸热”或“放热”)。
(3)T1°C时,科研人员探究等质量的三种催化剂(图中用I、II、III表示)在相同条件下的催化效果。在1L恒容容器中,分别充入1molCO2和2molCH4,测得H2物质的量随时间变化如图所示。
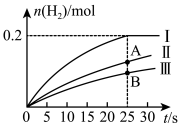
①使用催化剂I时,0~25秒间CO2的平均反应速率v(CO2)=_______ mol·L-1·s-1;CH4的平衡浓度是_______ mol·L-1。
②如果不考虑催化剂价格,则使用催化剂_______ (填“I”、“I”或“III”)的效果最好。状态A与B生成H2的速率大小关系是v(A)_______ v(B)(填“>”、“<”或“=”)。
③有利于提高CO2转化率的措施是_______ (填字母)。
a.使用更高效的催化剂
b.升高温度
c.增大压强
d.增大CH4与CO2的投料比
 2CO(g)+2H2(g)。完成下列填空。
2CO(g)+2H2(g)。完成下列填空。(1)甲烷分子的空间构型是
(2)该反应的化学平衡常数表达式为K=
| 温度 | 200°C | 250°C | 300°C |
| K | 56 | 64 | 80 |
(3)T1°C时,科研人员探究等质量的三种催化剂(图中用I、II、III表示)在相同条件下的催化效果。在1L恒容容器中,分别充入1molCO2和2molCH4,测得H2物质的量随时间变化如图所示。

①使用催化剂I时,0~25秒间CO2的平均反应速率v(CO2)=
②如果不考虑催化剂价格,则使用催化剂
③有利于提高CO2转化率的措施是
a.使用更高效的催化剂
b.升高温度
c.增大压强
d.增大CH4与CO2的投料比
您最近一年使用:0次
2010·上海松江·二模
解题方法
8 . 某厂用蛭石(主要成分为:MgO、Fe2O3、A12O3、SiO2)作原料生产A12O3与Fe(OH)3。
Ⅰ.工艺流程如图(只有固体A和F为纯净物):

Ⅱ.查阅资料:某些阳离子浓度为0.1mol/L时,氢氧化物沉淀时的pH为:
注:Al(OH)3pH=7.8时开始溶解,10.8时完全溶解。
请回答以下问题:
(1)写出下列物质化学式:试剂I__ ,F__ ;
(2)步骤②B生成C的离子方程式:__ ;
(3)要使固体D杂质尽量少,步聚②调节溶液的pH合理的是__ ;
A.12.4~13 B.10.8 C.3.7~5.2
(4)滤液E中存在较多的阴离子是__ ,滤液E中加入过量的NaOH溶液,充分沉淀后,检验上层清液中金属阳离子的操作步骤是__ ;
(5)固体D可用来生产合成氨的表面催化剂。如图表示无催化剂时,某合成氨的NH3的百分含量随时间变化曲线,请在图上用虚线画出该反应有催化剂时的曲线___ 。

Ⅰ.工艺流程如图(只有固体A和F为纯净物):

Ⅱ.查阅资料:某些阳离子浓度为0.1mol/L时,氢氧化物沉淀时的pH为:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 |
| 开始沉淀时的pH | 2.3 | 10.4 | 4.0 |
| 完全沉淀时的pH | 3.7 | 12.4 | 5.2 |
注:Al(OH)3pH=7.8时开始溶解,10.8时完全溶解。
请回答以下问题:
(1)写出下列物质化学式:试剂I
(2)步骤②B生成C的离子方程式:
(3)要使固体D杂质尽量少,步聚②调节溶液的pH合理的是
A.12.4~13 B.10.8 C.3.7~5.2
(4)滤液E中存在较多的阴离子是
(5)固体D可用来生产合成氨的表面催化剂。如图表示无催化剂时,某合成氨的NH3的百分含量随时间变化曲线,请在图上用虚线画出该反应有催化剂时的曲线

您最近一年使用:0次
2012·上海徐汇·二模
9 . 正丁醛可由丙烯通过下列反应制取:
CH3CH=CH2 + CO + H2 CH3CH2CH2CHO(正丁醛)反应①
CH3CH2CH2CHO(正丁醛)反应①
同时发生副反应:CH3CH=CH2 +CO + H2 (CH3)2CHCHO(异丁醛)反应②
(CH3)2CHCHO(异丁醛)反应②
CH3CH=CH2 + H2 CH3CH2CH3反应③
CH3CH2CH3反应③
三个反应在不同温度时的平衡常数见下表。回答问题:
(1)423K时,如果反应在恒容密闭容器中发生,当反应达到平衡时,下列说法错误的是_____ (填序号)。
a.c(CO):c( H2)一定等于1:1
b.反应混合物的密度保持不变
c.丙烯转化率达到最大值
d.单位时间内,n(CO)消耗= n(正丁醛)生成
(2)当反应达到平衡后,若将反应体系的温度从298 K提高到423 K,再次达到平衡后,在生成物中,__________ (填物质名称)的摩尔百分含量降低。
(3)若反应在298K进行,根据平衡常数作出的推测正确的是______ 。
a.反应③的反应速率最大 b.达到平衡后生成物中丙烷的体积百分含量最高
c.反应②达到平衡所需时间最长 d.298K时只有反应③向正反应方向进行
(4)使用催化剂后,单位时间里正丁醛的产量大大提高,反应体系产物中正/异醛比增大。导致这种情况出现的原因是____________________________ 。
CH3CH=CH2 + CO + H2
 CH3CH2CH2CHO(正丁醛)反应①
CH3CH2CH2CHO(正丁醛)反应①同时发生副反应:CH3CH=CH2 +CO + H2
 (CH3)2CHCHO(异丁醛)反应②
(CH3)2CHCHO(异丁醛)反应②CH3CH=CH2 + H2
 CH3CH2CH3反应③
CH3CH2CH3反应③三个反应在不同温度时的平衡常数见下表。回答问题:
| 温度/K | 反应① | 反应② | 反应③ |
| 298 | 2.96×109 | 2.53×109 | 1.32×1015 |
| 423 | 1.05×102 | 5.40×102 | 2.52×102 |
(1)423K时,如果反应在恒容密闭容器中发生,当反应达到平衡时,下列说法错误的是
a.c(CO):c( H2)一定等于1:1
b.反应混合物的密度保持不变
c.丙烯转化率达到最大值
d.单位时间内,n(CO)消耗= n(正丁醛)生成
(2)当反应达到平衡后,若将反应体系的温度从298 K提高到423 K,再次达到平衡后,在生成物中,
(3)若反应在298K进行,根据平衡常数作出的推测正确的是
a.反应③的反应速率最大 b.达到平衡后生成物中丙烷的体积百分含量最高
c.反应②达到平衡所需时间最长 d.298K时只有反应③向正反应方向进行
(4)使用催化剂后,单位时间里正丁醛的产量大大提高,反应体系产物中正/异醛比增大。导致这种情况出现的原因是
您最近一年使用:0次



