名校
解题方法
1 . 2SO2(g)+O2(g) ⇌2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是( )
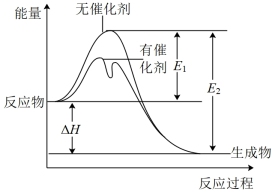

| A.该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数 |
| B.0℃、101kPa下,将1molSO2(g)和0.5molO2(g)置于密闭容器中充分反应生成SO3(g)放热akJ,其热化学方程式为2SO2(g)+O2(g) ⇌2SO3(g) ΔH=-2akJ·mol-l |
| C.该反应中,反应物的总键能小于生成物的总键能 |
| D.ΔH=E1-E2,使用催化剂改变活化能,但不改变反应热 |
您最近一年使用:0次
2020-05-11更新
|
384次组卷
|
25卷引用:2018-2019学年同步单元双基双测AB卷:第二单元化学反应速率与化学平衡单元测试B卷
(已下线)2018-2019学年同步单元双基双测AB卷:第二单元化学反应速率与化学平衡单元测试B卷四川省成都市实验中学2018-2019学年高二上学期期中模拟考试化学试题【全国百强校】河南省信阳市高级中学2018-2019学年高二上学期10月月考化学试题1河北省唐山市第一中学2018-2019学年高二上学期10月月考化学试题安徽省合肥市一六八中学2018-2019学年高二上学期期中考试化学试题江西省上饶市“山江湖”协作体2019-2020学年高二上学期期中化学(统招班)试题江西省宜春九中(外国语学校)2019-2020学年高二上学期期中考试化学试题广东省梅州市水寨中学2019-2020学年高二上学期期中考试化学试题湖北省随州一中2019-2020学年高二上学期期中考试化学试题河北省唐山市遵化市第一中学2019-2020学年高二上学期第一次月考化学试题黑龙江省大庆中学2020-2021学年高二10月月考化学试题安徽省池州市第一中学2020-2021学年高二上学期9月月考化学试题广东实验中学附属天河学校2020--2021学年高二上学期期中考试化学试题江西省九江市浔阳区九江市第七中学2020-2021学年高二上学期期中考试化学试题辽宁师范大学附属中学2021-2022学年高二上学期10月月考化学试题湖南省(长郡中学、株洲市第二中学)、江西省(九江一中)等十四校2018届高三第一次联考化学试题四川省成都市外国语学校2019届高三上学期开学考试化学试题安徽省阜阳市第三中学2018-2019学年高一下学期第二次调研考试化学试题福建省泉州第十六中学2020届高三上学期期中考试化学试题【全国百强校】安徽省六安市第一中学2020届高三下学期自测(二)化学试题(已下线)考点06 化学能与热能-2020年高考化学命题预测与模拟试题分类精编湖北省武汉市第十一中学2019-2020学年高一下学期期中测试化学试题河北省石家庄市第二中学本部2019-2020学年高一下学期期末结业考试化学试题重庆市巴蜀中学2018-2019学年高一下学期末考试化学试题新疆维吾尔自治区喀什第二中学2022-2023学年高二上学期第一次月考化学试题
解题方法
2 . 2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
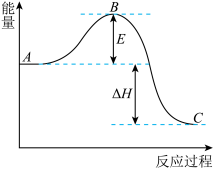
(1)该反应通常用V2O5作催化剂加快反应的进行,加V2O5会使图中B点______ (填“升高”或“降低”)。
(2)E的大小对该反应的反应热有无影响_______ 。
(3)图中A表示SO2(g)和O2(g)的_________ 。
(4)图中△H的意义是__________ 。
(5)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物,四价钒化合物再被氧气氧化。写出该催化过程实际发生反应的化学方程式_____ ,_____ ;
(6)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=________ 。
 2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
(1)该反应通常用V2O5作催化剂加快反应的进行,加V2O5会使图中B点
(2)E的大小对该反应的反应热有无影响
(3)图中A表示SO2(g)和O2(g)的
(4)图中△H的意义是
(5)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物,四价钒化合物再被氧气氧化。写出该催化过程实际发生反应的化学方程式
(6)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=
您最近一年使用:0次
13-14高一下·浙江·期中
名校
解题方法
3 . 为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位同学分别设计了如下四个实验,你认为结论不正确的是。
| A.将铜片放入稀硫酸中,无现象。若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气生成 |
| B.将除去氧化膜的相同大小、相同质量的镁条和铝条与相同浓度盐酸反应,前者速率大于后者 |
| C.两支试管中分别加入根同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
| D.相同条件下等质量的块状和粉末状大理石与相同浓度盐酸反应时,粉末状的反应速率快 |
您最近一年使用:0次
2020-02-27更新
|
111次组卷
|
6卷引用:辽宁省盘锦市第二高级中学2020-2021学年高二上学期第一次阶段性考试化学试题
辽宁省盘锦市第二高级中学2020-2021学年高二上学期第一次阶段性考试化学试题(已下线)【新东方】 2020-5山东省济宁市微山县第二中学2019-2020学年高二下学期第一学段教学质量监测化学试题江西省贵溪市实验中学2020-2021学年高二上学期第一次月考化学试题(已下线)2014浙江效实中学高一下学期期中考试化学(4-11班)试卷云南省丘北县第二中学2018-2019学年高一下学期期末考试化学试题
11-12高二上·云南玉溪·期中
名校
4 . 下列措施不能 加快化学反应速率的是
| A.升高温度 | B.降低温度 | C.增大反应物浓度 | D.使用合适的催化剂 |
您最近一年使用:0次
2019-11-27更新
|
834次组卷
|
26卷引用:辽宁省阜新市第二高级中学2020-2021学年高二上学期第二次月考化学试题
辽宁省阜新市第二高级中学2020-2021学年高二上学期第二次月考化学试题(已下线)2011-2012学年云南省玉溪一中高二上学期期中考试化学(文)试卷(已下线)2011-2012年河北广平一中高二第二次调研考试(文)化学试卷(已下线)2011-2012年湖南株洲市南方中学高二上学期期末考试文科化学试卷2014-2015西藏拉萨中学高二上学期期中化学(文)试卷云南省中央民族大学附属中学芒市国际学校2017-2018学年高二上学期末考试化学试题【全国百强校】贵州省遵义航天高级中学2018-2019学年高二(文)上学期第一次月考化学试题吉林省汪清县第六中学2018-2019学年高二上学期第二次月考化学试题吉林省汪清县第六中学2018-2019学年高二上学期期末考试化学试题江苏省扬州市江都区大桥高级中学2019-2020学年高二上学期期中考试化学(必修)试题湖南省邵阳市新宁县第二中学2019-2020学年高二上学期期末考试化学试题河南省安阳市2019年高中学业水平测试化学试题江苏省上冈高级中学2019-2020学年高二上学期期中考试化学(必修)试题黑龙江省双鸭山市第一中学2020-2021学年高二10月月考化学试题辽宁省阜新市第二高级中学2020-2021学年高二上学期期末考试化学试题(已下线)2011-2012学年湖南省长沙市雷锋学校高二期中考试化学试卷(文科)黑龙江省伊春市第二中学2016-2017学年高一下学期期中考试(文)化学试题湖南省张家界市2015-2016学年高一下学期期末联考(B)化学试题【全国百强校】甘肃省天水市第一中学2017-2018学年高一下学期第三学段(期末)考试(文)化学试题河南省周口中英文学校2020届高三上学期期中考试化学试题湖南省益阳市第六中学2018-2019学年高一下学期期中考试化学试题北京市海淀区首都师范大学附属中学2019-2020学年高一下学期第二次月考化学试题河南省原阳县2020-2021学年高二上学期期末考试化学试题新疆维吾尔自治区乌鲁木齐市等5地2022-2023学年高二学业水平考试化学试题吉林省长春市第二十中学2020-2021学年高一下学期第一次质量检测化学试题江苏省镇江实验高级中学2020-2021学年高一下学期第一次月考化学试题
名校
5 . 已知反应:2NO(g)+Br2(g)=2NOBr(g) ΔH=-a kJ·mol-1(a>0),其反应机理如下:①NO(g)+Br2(g)=NOBr2(g) 快 ②NO(g)+NOBr2(g)=2NOBr(g) 慢
下列有关该反应的说法不正确的是
下列有关该反应的说法不正确的是
| A.该反应的速率主要取决于②的快慢 |
| B.NOBr2是该反应的催化剂 |
| C.正反应的活化能比逆反应的活化能小a kJ·mol-1 |
| D.增大Br2(g)浓度能增大单位体积内活化分子个数,加快反应速率 |
您最近一年使用:0次
2019-11-05更新
|
355次组卷
|
9卷引用:山西省长治市第二中学2019-2020学年高二上学期期中考试化学试题
山西省长治市第二中学2019-2020学年高二上学期期中考试化学试题人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第一节 化学反应速率 方法帮河北省邯郸市大名县第一中学2020-2021学年高二上学期10月月考化学(实验班)试题福建省福州市八县(市)一中2020-2021学年高二上学期期中联考化学试题山西省怀仁市2020-2021学年高二上学期期中化学试题辽宁省丹东市凤城市第一中学2021-2022学年高二上学期10月份月考化学试题山西省汾阳市汾阳中学2020-2021学年高二下学期开学考试化学试题云南省下关第一中学2023-2024学年高二上学期9月月考化学试题陕西省咸阳市兴平市西郊高级中学2023-2024学年高二上学期期中考试化学试题
名校
6 . 已知分解1 mol H2O2放出热量98kJ,在含少量I-的溶液中,H2O2分解的机理为:H2O2+I-→H2O+IO- 慢 H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法不正确的是( )
下列有关该反应的说法不正确的是( )
| A.反应速率与I-浓度有关 | B.I-也是该反应的催化剂 |
| C.反应活化能等于98 kJ/mol | D.v(H2O2)=v(H2O)=2v(O2) |
您最近一年使用:0次
2019-10-22更新
|
96次组卷
|
2卷引用:辽宁省六校协作体2019-2020学年高二上学期10月月考化学试题
11-12高二·河南安阳·阶段练习
名校
7 . 可逆反应mA(g)+nB(g)  pC(g)+qD(g)的v-t图象如下图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下图:
pC(g)+qD(g)的v-t图象如下图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下图:
①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是
 pC(g)+qD(g)的v-t图象如下图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下图:
pC(g)+qD(g)的v-t图象如下图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下图: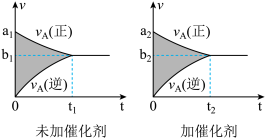
①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是
| A.②④⑤⑦ | B.①④⑥⑧ | C.②③⑤⑧ | D.①③⑥⑦ |
您最近一年使用:0次
2019-10-15更新
|
206次组卷
|
13卷引用:辽宁省普兰店市第一中学2018-2019学年高二(理)上学期期中考试化学试题
辽宁省普兰店市第一中学2018-2019学年高二(理)上学期期中考试化学试题(已下线)2012-2013学年河南省安阳一中高二第二次阶段考试化学试卷(已下线)2013-2014学年江苏省无锡江阴市高二下学期期中考试化学试卷2015-2016学年湖南省衡阳八中高二上第二次月考化学试卷黑龙江省双鸭山市第一中学2017-2018学年高二9月月考化学试题湖北省襄阳市第四中学2017-2018学年高二10月月考化学试题湖南辰溪博雅实验学校2018-2019学年高二8月月考化学试题山西省运城市河津中学2019-2020学年高二9月月考化学试题吉林省白山市抚松县第六中学2019-2020学年高二上学期期中考试化学试题【全国百强校】海南省海南中学2018届高三第五次月考化学试题【全国百强校】河北省武邑中学2019届高三上学期第一次调研考试化学试题黑龙江省哈尔滨市第一中学2021届高三上学期期中考试化学试题湖北省孝感市普通高中协作体2022-2023学年高二上学期期中联合考试化学试题
名校
8 . 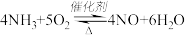 是工业上制硝酸的重要反应,下列有关说法
是工业上制硝酸的重要反应,下列有关说法错误 的是
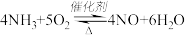 是工业上制硝酸的重要反应,下列有关说法
是工业上制硝酸的重要反应,下列有关说法| A.使用催化剂可以加快反应速率 |
| B.增大压强可以加快反应速率 |
| C.达到平衡时,V(正)=V(逆) |
| D.增大O2的浓度可以使NH3全部转变为NO |
您最近一年使用:0次
2019-08-31更新
|
445次组卷
|
12卷引用:辽宁省大连市普兰店市第一中学2019-2020学年高二上学期期末考试化学试题
辽宁省大连市普兰店市第一中学2019-2020学年高二上学期期末考试化学试题(已下线)2.4 化学反应的调控(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)(已下线)第二章检测-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)【省级联考】江苏省2019届高三下学期小高考模拟化学试题安徽省宣城市2018-2019学年高一下学期期末考试化学试题湖北省罗田第一中学2021-2022学年高二10月月考化学试题江苏省常州市武进区礼嘉中学2020-2021学年高一下学期阶段质量调研化学试题云南省通海县第一中学2021-2022学年高一下学期3月月考化学试题(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)江苏省常州市联盟学校2022-2023学年高一下学期期末考试化学试题江苏省扬州市广陵区红桥高级中学2023-2024学年高一下学期4月期中考试化学试题(已下线)专题01 化学反应与能量变化-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
名校
9 . 工业制硫酸中的一步重要反应是SO2的催化氧化:2SO2+O2⇌2SO3(正反应放热),下列有关说法正确的是
| A.升高温度只提高逆反应速率 |
| B.降低温度可提高正反应速率 |
| C.使用催化剂能显著增大反应速率 |
| D.达到化学平衡时正、逆反应速率相等且等于0 |
您最近一年使用:0次
2019-07-16更新
|
281次组卷
|
6卷引用:辽宁省阜新市第二高级中学2021-2022学年高二上学期期末考试化学试题
2014高三·全国·专题练习
名校
10 . 在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g) 2SO3(g)ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g)ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是

 2SO3(g)ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g)ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
| A.图Ⅰ研究的是t1时刻增大O2的物质的量浓度对反应速率的影响 |
| B.图Ⅱ研究的是t1时刻通入氦气增大体系压强对反应速率的影响 |
| C.图Ⅲ研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高 |
| D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 |
您最近一年使用:0次
2019-06-15更新
|
317次组卷
|
11卷引用:2015-2016学年辽宁省沈阳市东北育才学校高二上化学试卷
2015-2016学年辽宁省沈阳市东北育才学校高二上化学试卷(已下线)2013-2014湖北省荆州中学高二上学期期末考试化学试卷2015-2016学年四川省彭州中学高二上期中测试化学试卷2015-2016学年辽宁省实验中学分校高一下学期6月月考化学试卷2016-2017学年江苏省沭阳县高二下学期期中调研测试化学试卷陕西省西安市长安区第一中学2017-2018学年高二上学期第二次月考化学试题云南省会泽县茚旺高级中学2018-2019学年高二上学期12月月考化学试题重庆市第三十中学2018-2019学年高二上学期第三次月考化学试题(已下线)2014高考名师推荐化学化学平衡图像(鲁科版2019)必修第二册 第2章 化学键 化学反应规律 综合检测卷广东省佛山市顺德区郑裕彤中学2023-2024学年上学期高一10月月考化学试题



