解题方法
1 . 能量以多种不同的形式存在,并能相互转化。
I.化学反应伴随能量变化。
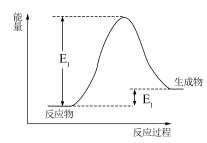
(1)NH4HCO3和CH3COOH反应过程的能量变化如图所示,___________ 代表反应活化能(填“E1”或“E2”)。
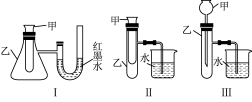
(2)某实验小组设计了三套实验装置(如图),不能用来证明“NH4HCO3和CH3COOH反应能量变化情况”的是___________ (填序号)。
(3)NH4HCO3和CH3COOH反应的离子方程式为___________ 。
II.合成氨反应为放热反应,在化工生产中具有重要意义。
(4)N2和H2在催化剂表面合成気的微观历程如图所示,用 、
、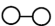 、
、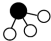 分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
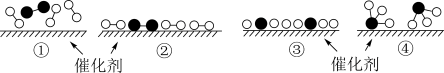
III.电池的发明是储能和供能技术的巨大进步,如图所示的原电池装置,插入电解质溶液前Cu和Fe电极质量相等。
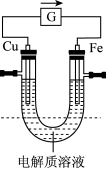
(5)电解质溶液为FeCl3时,图中箭头的方向表示___________ (填“电子”或“电流”)的流向,铁片上的电极反应式为___________ 。
(6)电解质溶液更换为X时,电极质量变化曲线如图所示。
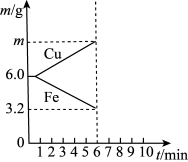
①X可以是___________ (填字母)。
A.稀硫酸 B.CuSO4溶液 C.稀盐酸 D.FeSO4溶液
②6 min时Cu电极的质量a为___________ g。
I.化学反应伴随能量变化。
(1)NH4HCO3和CH3COOH反应过程的能量变化如图所示,

(2)某实验小组设计了三套实验装置(如图),不能用来证明“NH4HCO3和CH3COOH反应能量变化情况”的是

(3)NH4HCO3和CH3COOH反应的离子方程式为
II.合成氨反应为放热反应,在化工生产中具有重要意义。
(4)N2和H2在催化剂表面合成気的微观历程如图所示,用
 、
、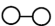 、
、 分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)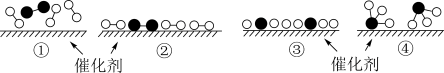
| A.反应过程存在非极性共价键的断裂和形成 |
| B.催化剂仅起到吸附N2和H2的作用,对化学反应速率没有影响 |
| C.②→③过程吸热 |
| D.反应物断键吸收的总能量小于生成物成键释放的总能量 |
III.电池的发明是储能和供能技术的巨大进步,如图所示的原电池装置,插入电解质溶液前Cu和Fe电极质量相等。

(5)电解质溶液为FeCl3时,图中箭头的方向表示
(6)电解质溶液更换为X时,电极质量变化曲线如图所示。

①X可以是
A.稀硫酸 B.CuSO4溶液 C.稀盐酸 D.FeSO4溶液
②6 min时Cu电极的质量a为
您最近一年使用:0次
解题方法
2 . 下列有关实验或操作能达到实验目的的是


| A.①证明Ksp(AgCl)>Ksp(AgI) |
| B.②装置蒸发氯化铝溶液制备无水氯化铝 |
| C.③装置用已知浓度的盐酸滴定未知浓度的NaOH溶液 |
| D.④验证二氯化锰对过氧化氢的分解能起到催化的作用 |
您最近一年使用:0次
2022-10-28更新
|
747次组卷
|
2卷引用:湖北省武汉市部分重点中学2022-2023学年高二上学期10月联考化学试题
解题方法
3 . 某化学课外兴趣小组探究过氧化钠与水的反应,探究过程如下:
(1)实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请分析脱脂棉燃烧的原因_______ 。
(2)实验2:取一支试管,向其中加入少量过氧化钠固体,然后加入少量蒸馏水,有气泡冒出,充分振荡后再滴入酚酞试液,溶液先变红后褪色。
提出问题:溶液为什么先变红,过了一会,红色又褪去了呢?
猜想:甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
查阅资料:
i.H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;
ii.NaOH溶液浓度过高,酚酞不变色或变色后迅速褪色。
设计实验方案:
①取少量褪色后的溶液于试管中,加入MnO2固体,若有气泡冒出,用_______ 检验该气体,则证明该反应过程中生成了_______ (填化学式)使溶液褪色。
②另取少量褪色后的溶液于试管中,加入蒸馏水稀释,若溶液变红,则证明溶液褪色原因可能为_______ 。
(3)为进一步探究过氧化钠与水反应的实质,运用pH传感器、温度传感器、氧气传感器等仪器进行实验探究,得到如下图象。
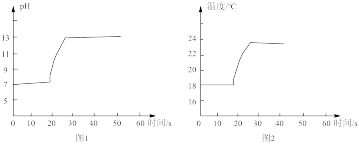
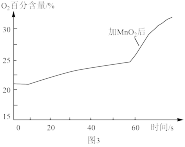
根据图象,得出结论:过氧化钠与水反应过程的方程式为_______ 、_______ 。
(1)实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请分析脱脂棉燃烧的原因
(2)实验2:取一支试管,向其中加入少量过氧化钠固体,然后加入少量蒸馏水,有气泡冒出,充分振荡后再滴入酚酞试液,溶液先变红后褪色。
提出问题:溶液为什么先变红,过了一会,红色又褪去了呢?
猜想:甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
查阅资料:
i.H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;
ii.NaOH溶液浓度过高,酚酞不变色或变色后迅速褪色。
设计实验方案:
①取少量褪色后的溶液于试管中,加入MnO2固体,若有气泡冒出,用
②另取少量褪色后的溶液于试管中,加入蒸馏水稀释,若溶液变红,则证明溶液褪色原因可能为
(3)为进一步探究过氧化钠与水反应的实质,运用pH传感器、温度传感器、氧气传感器等仪器进行实验探究,得到如下图象。


根据图象,得出结论:过氧化钠与水反应过程的方程式为
您最近一年使用:0次
名校
4 . 下列实验方案不能达到相应实验目的的是
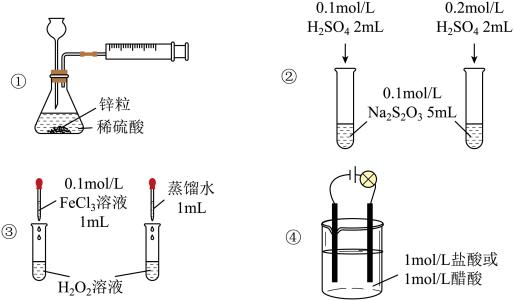

| A.用装置①定量测定化学反应速率 |
| B.用装置②探究H2SO4浓度对化学反应速率的影响 |
| C.用装置③探究催化剂对H2O2分解速率的影响 |
| D.用装置④证明醋酸为弱酸 |
您最近一年使用:0次
名校
5 . 某小组同学探究Cu和H2O2的反应。
[猜想预测]
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
[实验探究]
实验i:向装有0.5gCu的烧杯中加入20mL30%H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:____ 。
[继续探究]
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2++4NH3 [Cu(NH3)4]2+,[Cu(NH3)4]2+为深蓝色;
[Cu(NH3)4]2+,[Cu(NH3)4]2+为深蓝色;
Cu(OH)2可溶于氨水形成深蓝色溶液。
(2)实验ii中:溶液变蓝的原因是____ (用化学用语解释);经检验产生的气体为氧气,产生氧气的原因是____ 。
(3)对比实验i和iii,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。
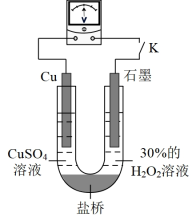
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:____ 。
利用该方法也可证明酸性增强可提高H2O2的氧化性,导致Cu溶解速率加快。
(4)实验iii有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因可能是____ 。
(5)基于以上实验,影响Cu与H2O2反应速率的因素有____ 和____ 。
[猜想预测]
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
[实验探究]
实验i:向装有0.5gCu的烧杯中加入20mL30%H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:
[继续探究]
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2++4NH3
 [Cu(NH3)4]2+,[Cu(NH3)4]2+为深蓝色;
[Cu(NH3)4]2+,[Cu(NH3)4]2+为深蓝色;Cu(OH)2可溶于氨水形成深蓝色溶液。
| 装置 | 序号 | 试剂a | 现象 |
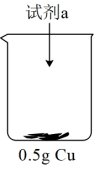 | ii | 20mL30%H2O2与4mL5mol/LH2SO4混合液 | Cu表面很快产生少量气泡,溶液逐渐变蓝,产生较多气泡 |
| iii | 20mL30%H2O2与4mL5mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物 |
(3)对比实验i和iii,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。

已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:
利用该方法也可证明酸性增强可提高H2O2的氧化性,导致Cu溶解速率加快。
(4)实验iii有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因可能是
(5)基于以上实验,影响Cu与H2O2反应速率的因素有
您最近一年使用:0次
解题方法
6 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验某无色溶液中是否含有 | 取少量该溶液于试管中,加稀硝酸酸化,再加入硝酸钡溶液 | 若有白色沉淀生成,则该溶液中一定含有 |
| B | 探究X是否属于醛类物质 | 向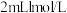 的 的 溶液,加入5滴 溶液,加入5滴 的 的 溶液,振荡后再加入 溶液,振荡后再加入 有机物X,加热 有机物X,加热 | 出现砖红色沉淀,则X可能是醛类物质 |
| C | 探究 和 和 的溶解度大小 的溶解度大小 | 向 溶液中加入一定量的 溶液中加入一定量的 溶液,充分反应后再加少量的 溶液,充分反应后再加少量的 溶液 溶液 | 若先生成白色沉淀,后产生蓝色沉淀,则证明 比 比 溶解度小 溶解度小 |
| D | 探究不同金属离于对 分解速率的影响 分解速率的影响 | 取2支试管,向2支试管中各加入 溶液,分别向试管中各加入 溶液,分别向试管中各加入 溶液和 溶液和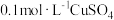 溶液 溶液 | 相同时间内产生气泡多的,则催化效果好 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 下列操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究温度对2NO2(g) ⇌N2O4(g)平衡有影响 | 将充满NO2的密闭玻璃球浸泡在热水中气体红棕色加深 |
| B | 探究催化剂对H2O2分解速率的影响 | 在相同条件下,向一支试管中加入2mL 5%的H2O2溶液和1mL H2O,向另一支试管中加入2mL 10%的H2O2溶液和1mL FeCl3溶液,观察实验现象 |
| C | 证明增大反应物浓度,能加快化学反应速率 | 将两块表面积相同的鋅粒分别放入稀硫酸和浓硫酸 |
| D | 证明KCl中存在离子键 | KCl溶于水是否导电 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 下列实验操作和现象与预期实验目的或所得结论不一致的是
| 选项 | 实验操作和现象 | 预期实验目的或所得结论 |
| A | 将酸性KMnO4溶液滴入丙烯醛中,溶液的紫红色褪去 | 不能说明丙烯醛中含有碳碳双键 |
| B | 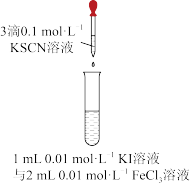 现象为溶液变红 | 证明化学反应存在一定的限度 |
| C | 相同条件下,在两支试管中各加入3mL6%的H2O2溶液,再向H2O2溶液中分别滴入1mLH2O和1mLFeCl3溶液,观察并比较H2O2的分解速率 | 探究催化剂对H2O2分解速率的影响 |
| D | 向2mL甲苯中加入3滴酸性KMnO4溶液,振荡,紫色褪去;向2mL苯中加入3滴酸性KMnO4溶液,振荡,紫色没有褪去 | 证明与苯环相连的甲基易被氧化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
21-22高二上·安徽池州·期中
名校
9 . 某研究性学习小组利用 溶液和酸性
溶液和酸性 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)通过实验A、B,可探究出_______ (填外部因素)的改变对化学反应速率的影响,其中
_______ 、
_______ ,通过实验_______ (填实验序号)可探究出温度变化对化学反应速率的影响,其中
_______ 。
(2)若 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是_______ 。忽略溶液体积的变化,利用实验B中数据计算,0~8s内,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
_______ 。
(3)该小组的一位同学通过查阅资料发现,上述实验过程中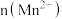 随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对
随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对 与草酸之间的反应有某种特殊作用,则该作用是
与草酸之间的反应有某种特殊作用,则该作用是_______ 。设计实验证明,分别取等体积等浓度的 和
和 混合,平均分成两份,一份中不加任何试剂,一份加入少量
混合,平均分成两份,一份中不加任何试剂,一份加入少量 固体,观察到两溶液都没有褪色,原因是:
固体,观察到两溶液都没有褪色,原因是:_______ 。

 溶液和酸性
溶液和酸性 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:| 实验序号 | 实验温度/K | 溶液颜色褪至无色所需时间/s | |||||
酸性 溶液 溶液 |  溶液 溶液 |  | |||||
 | 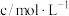 |  | 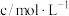 |  | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 |  |
| B |  | 2 | 0.02 | 3 | 0.1 |  | 8 |
| C | 313 | 2 | 0.02 |  | 0.1 | 1 |  |



(2)若
 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应速率
的浓度变化表示的反应速率
(3)该小组的一位同学通过查阅资料发现,上述实验过程中
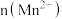 随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对
随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对 与草酸之间的反应有某种特殊作用,则该作用是
与草酸之间的反应有某种特殊作用,则该作用是 和
和 混合,平均分成两份,一份中不加任何试剂,一份加入少量
混合,平均分成两份,一份中不加任何试剂,一份加入少量 固体,观察到两溶液都没有褪色,原因是:
固体,观察到两溶液都没有褪色,原因是:
您最近一年使用:0次
2022-04-16更新
|
599次组卷
|
5卷引用:2.1.2 影响化学反应速率的因素 活化能 -2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
(已下线)2.1.2 影响化学反应速率的因素 活化能 -2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)黑龙江省鹤岗市第一中学2022-2023学年高三上学期10月月考化学试题安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题安徽省池州市贵池区2021-2022学年高二上学期期中考试化学试题(已下线)化学反应速率与化学平衡——课时2化学反应速率的影响因素
名校
解题方法
10 . 下列操作能达到实验目的的是
| 实验操作 | 实验目的 | |
| A | 相同温度下,向两支盛有相同体积不同浓度H2O2溶液的试管中分别滴入适量相同浓度的CuSO4溶液和FeCl3溶液 | 探究Cu2+、Fe3+对H2O2分解速率的影响 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 | 称取2.0gNaOH固体 |
| D | 分别取甲苯和苯与酸性KMnO4溶液反应,观察酸性KMnO4溶液的褪色情况 | 证明甲苯中的甲基能够活化苯环 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-12更新
|
744次组卷
|
4卷引用:山东省济南市历城第二中学2021-2022学年高三下学期二轮复习测评联合考试(二模) 化学试题
山东省济南市历城第二中学2021-2022学年高三下学期二轮复习测评联合考试(二模) 化学试题(已下线)化学-2022年高考考前押题密卷(湖南卷)湖北省宜昌英杰学校2021-2022学年高三上学期9月月考化学试题巩固训练12



