名校
1 . 叔丁基溴在稀的碱性水溶液中水解生成叔丁醇的反应分三步进行,反应中每一步的能量变化曲线如图所示,下列有关说法不正确的是
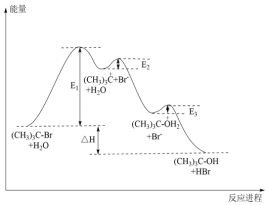

| A.叔丁基溴生成叔丁醇的反应是放热反应 |
B. 为反应催化剂 为反应催化剂 |
| C.决定叔丁基溴水解生成叔丁醇反应的速率的是第一步反应 |
D.第三步反应为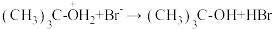 |
您最近一年使用:0次
名校
解题方法
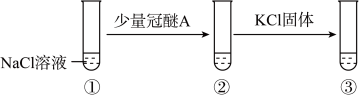
2 . 冠醚能与碱金属离子结合(如下图所示),是有机反应很好的催化剂,例如能加快酸性 溶液与环己烯(
溶液与环己烯( )的反应速率。
)的反应速率。
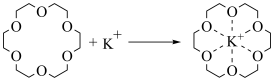
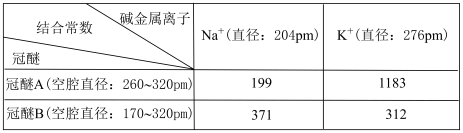
用结合常数表示冠醚与碱金属离子的结合能力,结合常数越大,两者结合能力越强。
下列说法正确的是
 溶液与环己烯(
溶液与环己烯( )的反应速率。
)的反应速率。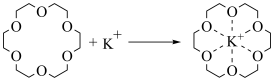
用结合常数表示冠醚与碱金属离子的结合能力,结合常数越大,两者结合能力越强。


下列说法正确的是
| A.结合常数的大小与碱金属离子直径有关,与冠醚空腔直径无关 |
B.冠醚通过与 结合将 结合将 携带进入有机相,从而加快反应速率 携带进入有机相,从而加快反应速率 |
C.如图所示的实验中 :①>②>③ :①>②>③ |
D.为加快酸性 溶液与环己烯的反应速率,选择冠醚B比冠醚A更合适 溶液与环己烯的反应速率,选择冠醚B比冠醚A更合适 |
您最近一年使用:0次
名校
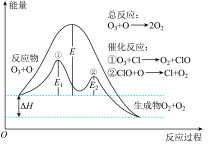
3 . 大气中的臭氧层能有效阻挡紫外线。臭氧层中 分解过程如图所示,下列说法正确的是
分解过程如图所示,下列说法正确的是
 分解过程如图所示,下列说法正确的是
分解过程如图所示,下列说法正确的是
| A.催化反应①、②和总反应均是放热反应 |
B.决定 分解反应速率的是催化反应② 分解反应速率的是催化反应② |
C. 是催化反应①正反应的活化能 是催化反应①正反应的活化能 |
D.Cl是反应的催化剂,改变了反应历程,降低了 |
您最近一年使用:0次
4 .  是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:
第一步 (快反应)
(快反应)
第二步 (慢反应)
(慢反应)
第三步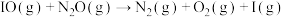 (快反应)
(快反应)
实验表明,含碘时 的分解速率方程
的分解速率方程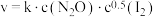 (k为速率常数)。下列表述正确的是
(k为速率常数)。下列表述正确的是
 是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:第一步
 (快反应)
(快反应)第二步
 (慢反应)
(慢反应)第三步
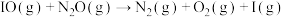 (快反应)
(快反应)实验表明,含碘时
 的分解速率方程
的分解速率方程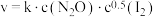 (k为速率常数)。下列表述正确的是
(k为速率常数)。下列表述正确的是| A.IO为反应的中间产物 | B.第一步对总反应速率起决定作用 |
C. 浓度与 浓度与 分解速率无关 分解速率无关 | D.第二步活化能比第三步小 |
您最近一年使用:0次
5 . 在3个容积均为 的密闭容器中分别放入
的密闭容器中分别放入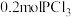 和
和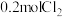 ,在不同条件下发生反应
,在不同条件下发生反应 。各容器内气体总压强随时间的变化如图所示。下列说法错误的是
。各容器内气体总压强随时间的变化如图所示。下列说法错误的是

 的密闭容器中分别放入
的密闭容器中分别放入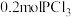 和
和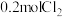 ,在不同条件下发生反应
,在不同条件下发生反应 。各容器内气体总压强随时间的变化如图所示。下列说法错误的是
。各容器内气体总压强随时间的变化如图所示。下列说法错误的是
A.实验a从反应开始至 的平均速率 的平均速率 |
| B.与实验a相比,实验b使用了催化剂,实验c是在较高温度下进行的 |
C.实验c中反应的平衡常数为 |
D.三组实验中反应的平衡转化率: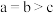 |
您最近一年使用:0次
6 . 丙烯是合成聚丙烯的单体。在催化剂作用下,丙烷脱氢生成丙烯的能量变化如图所示。下列叙述错误的是
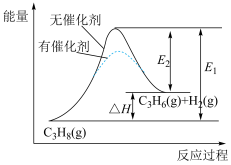

| A.上述反应的正反应是吸热反应 | B.催化剂的作用是降低反应的活化能 |
| C.升温,该反应的平衡常数K 增大 | D.使用不同催化剂,该反应的△H不同 |
您最近一年使用:0次
名校
解题方法
7 . 某实验小组在不同温度下,用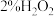 溶液与不同试剂混合,利用氧气传感器测定氧气全部放出所需时间,来探究影响H₃O₃分解的化学反应速率的因素,设计如下实验:
溶液与不同试剂混合,利用氧气传感器测定氧气全部放出所需时间,来探究影响H₃O₃分解的化学反应速率的因素,设计如下实验:
(1)从实验1、2、3可以得出,______ (填离子符号)促进 ,分解生成氧气;催化剂能增大化学反应速率的原因是
,分解生成氧气;催化剂能增大化学反应速率的原因是______ 。
(2)实验1设计的目的是______ 。
(3)实验______ (填实验序号)探究温度对 分解的影响。
分解的影响。
(4)由上述实验可知,酸______ (填“抑制”或“促进”) 分解。
分解。
(5)对于 分解反应,
分解反应, 也有一定的催化作用。为比较
也有一定的催化作用。为比较 和
和 对
对 分解的催化效果,研究小组设计了如图所示的实验。请回答相关问题:
分解的催化效果,研究小组设计了如图所示的实验。请回答相关问题:
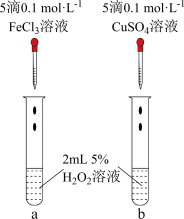
①可通过观察______ ,比较得出结论。
②若反应速率 ,有同学提出该实验不能说明
,有同学提出该实验不能说明 对
对 分解的催化效果一定比
分解的催化效果一定比 好。结合上表中的实验,你认为将
好。结合上表中的实验,你认为将______ 溶液改为______ 溶液更为合理。
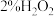 溶液与不同试剂混合,利用氧气传感器测定氧气全部放出所需时间,来探究影响H₃O₃分解的化学反应速率的因素,设计如下实验:
溶液与不同试剂混合,利用氧气传感器测定氧气全部放出所需时间,来探究影响H₃O₃分解的化学反应速率的因素,设计如下实验:| 实验序号 | 温度/℃ | 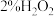 溶液的体积/mL 溶液的体积/mL | 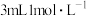 的试剂 的试剂 | 时间/s |
| 1 | 25 | 20.00 | KCl | 几乎不分解 |
| 2 | 25 | 20.00 | KI | 82 |
| 3 | 25 | 20.00 |  | 202 |
| 4 | 100 | 20.00 | KI | 65 |
| 5 | 25 | 20.00 | KI中通HCl气体,使其 | 几乎不分解 |
| 6 | 25 | 20.00 | KI中加入KOH固体,使其 | 75 |
(1)从实验1、2、3可以得出,
 ,分解生成氧气;催化剂能增大化学反应速率的原因是
,分解生成氧气;催化剂能增大化学反应速率的原因是(2)实验1设计的目的是
(3)实验
 分解的影响。
分解的影响。(4)由上述实验可知,酸
 分解。
分解。(5)对于
 分解反应,
分解反应, 也有一定的催化作用。为比较
也有一定的催化作用。为比较 和
和 对
对 分解的催化效果,研究小组设计了如图所示的实验。请回答相关问题:
分解的催化效果,研究小组设计了如图所示的实验。请回答相关问题:
①可通过观察
②若反应速率
 ,有同学提出该实验不能说明
,有同学提出该实验不能说明 对
对 分解的催化效果一定比
分解的催化效果一定比 好。结合上表中的实验,你认为将
好。结合上表中的实验,你认为将
您最近一年使用:0次
2023-11-28更新
|
37次组卷
|
2卷引用:河南省洛阳市2023-2024学年高二上期期中考试化学试题
名校
8 . 二氧化硫主要用于生产三氧化硫、硫酸、亚硫酸盐、硫代硫酸盐,也用作熏蒸剂、防腐剂、消毒剂、还原剂等。
Ⅰ.焦炭催化还原 生成
生成 的化学反应方程式为
的化学反应方程式为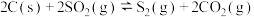 ,向1L的容密闭容器中加入2
,向1L的容密闭容器中加入2 C和1
C和1
 反应,
反应, 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。

(1)700℃时,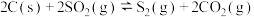 的平衡常数是
的平衡常数是_____ 。
(2)温度大于700℃后, 的转化率降低的原因是
的转化率降低的原因是_____ 。
(3)下列有关说法正确的是_____。
Ⅱ.碘离子可以作为水溶液中 歧化反应的催化剂,可能的催化过程如下。
歧化反应的催化剂,可能的催化过程如下。
i.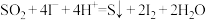
ii.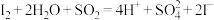
探究i、ii反应速率与 歧化反应速率的关系,实验如下:分别将18
歧化反应速率的关系,实验如下:分别将18
 饱和溶液加入到2
饱和溶液加入到2 下列试剂中,密闭放置观察现象。(已知:
下列试剂中,密闭放置观察现象。(已知: 易溶解在
易溶解在 溶液中)
溶液中)
(4)水溶液中 歧化反应方程式是:
歧化反应方程式是:_____ 。
(5)A、B、C互为对比实验,则
_____ ,
_____ ;比较A、B、C可的出的结论是_____ 。
(6)根据以上实验可知水溶液中 歧化反应的速率主要由反应
歧化反应的速率主要由反应_____ (填“i”或“i”)决定,其原因是_____ 。
Ⅰ.焦炭催化还原
 生成
生成 的化学反应方程式为
的化学反应方程式为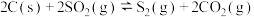 ,向1L的容密闭容器中加入2
,向1L的容密闭容器中加入2 C和1
C和1
 反应,
反应, 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。
(1)700℃时,
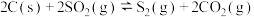 的平衡常数是
的平衡常数是(2)温度大于700℃后,
 的转化率降低的原因是
的转化率降低的原因是(3)下列有关说法正确的是_____。
A.将容器的体积缩小至0.5L,达到平衡时 的转化率增大 的转化率增大 |
B.当容器内 的浓度不在发生变化时,该反应达到平衡状态 的浓度不在发生变化时,该反应达到平衡状态 |
| C.向容器内加入一定量的焦炭,化学反应速率增大 |
| D.当容器内的气体的平均摩尔质量不变时,该反应达到平衡状态 |
Ⅱ.碘离子可以作为水溶液中
 歧化反应的催化剂,可能的催化过程如下。
歧化反应的催化剂,可能的催化过程如下。i.
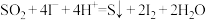
ii.
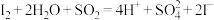
探究i、ii反应速率与
 歧化反应速率的关系,实验如下:分别将18
歧化反应速率的关系,实验如下:分别将18
 饱和溶液加入到2
饱和溶液加入到2 下列试剂中,密闭放置观察现象。(已知:
下列试剂中,密闭放置观察现象。(已知: 易溶解在
易溶解在 溶液中)
溶液中)| 序号 | A | B | C | D |
| 试剂组成 | X  | 0.4  0.2   | Y  | 0.2  0.0002   |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
(4)水溶液中
 歧化反应方程式是:
歧化反应方程式是:(5)A、B、C互为对比实验,则


(6)根据以上实验可知水溶液中
 歧化反应的速率主要由反应
歧化反应的速率主要由反应
您最近一年使用:0次
名校
解题方法
9 .  在催化剂作用下分解速率加快,反应过程中能量变化如图所示。下列说法错误的是
在催化剂作用下分解速率加快,反应过程中能量变化如图所示。下列说法错误的是
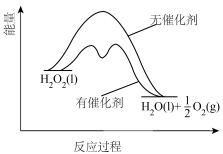
 在催化剂作用下分解速率加快,反应过程中能量变化如图所示。下列说法错误的是
在催化剂作用下分解速率加快,反应过程中能量变化如图所示。下列说法错误的是
| A.反应物的焓高于生成物的焓 |
| B.加入催化剂,增大了反应的焓变 |
| C.加入催化剂,增大了反应物的活化分子百分数 |
D. 分解的反应可表示为 分解的反应可表示为  |
您最近一年使用:0次
2023-11-11更新
|
254次组卷
|
2卷引用:河南省开封市2023-2024学年高二上学期11月期中考试化学试题
名校
10 . 已知某反应A(g)+B(g)=C(g)+D(g),反应过程中的能量变化如图所示,回答下列问题。
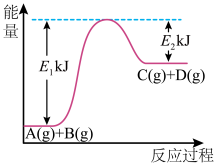
(1)该反应是___________ (填“吸热”或“放热”)反应,该反应的ΔH=___________ kJ/mol (用含E1、E2的代数式表示),1 mol气体A和1 mol气体B具有的总能量比1 mol气体C和1 mol气体D具有的总能量___________ (填“一定高”“一定低”或“高低不一定”)。
(2)若在反应体系中加入催化剂使反应速率增大,则E2的变化是:E2___________ ,ΔH___________ (填“增大”“减小”或“不变”)。

(1)该反应是
(2)若在反应体系中加入催化剂使反应速率增大,则E2的变化是:E2
您最近一年使用:0次



