1 . 下列生产生活中需要增大化学反应速率的是
 |  |  |  |
| A.铁桥生锈 | B.牛奶变质 | C.塑料老化 | D.高炉炼铁 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 废弃物回收再利用是环境保护的重要课题。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)、锌灰(主要成分为Zn、ZnO,杂质为Fe及其氧化物)回收Cu并制备ZnO,其部分实验过程如下图所示:
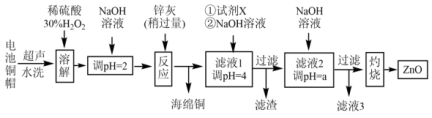
(1)铜帽溶解前需剪碎,其目的是_______ ,写出“溶解”过程中主要化学方程式_______ ,此过程不能加热的原因是_______ 。
(2)“反应”步骤为确定锌灰用量,以碘量法测定溶液中Cu2+含量:向含Cu2+待测液中加入过量KI溶液,再用Na2S2O3标准溶液滴定生成的 至终点,滴定原理如下:2Cu2++4I-=2CuI(白色)↓+I2;
至终点,滴定原理如下:2Cu2++4I-=2CuI(白色)↓+I2; 。
。
①滴定选用的指示剂为_______ ,滴定终点的现象是_______ 。
②若待测液中H2O2没有除尽,所测Cu2+含量将_______ (填“偏高”、“偏低”或“不变”)。
(3)已知:①滤液1中主要含有的金属离子有Zn2+、Fe2+;
②pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-;
③几种金属离子生成氧氧化物沉淀pH见下表。
利用滤液1制取ZnO,试剂X为_______ (填序号A.30% H2O2;B.1.0 mol/LHNO3),a的范围是_______ 。

(1)铜帽溶解前需剪碎,其目的是
(2)“反应”步骤为确定锌灰用量,以碘量法测定溶液中Cu2+含量:向含Cu2+待测液中加入过量KI溶液,再用Na2S2O3标准溶液滴定生成的
 至终点,滴定原理如下:2Cu2++4I-=2CuI(白色)↓+I2;
至终点,滴定原理如下:2Cu2++4I-=2CuI(白色)↓+I2; 。
。①滴定选用的指示剂为
②若待测液中H2O2没有除尽,所测Cu2+含量将
(3)已知:①滤液1中主要含有的金属离子有Zn2+、Fe2+;
②pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-;
③几种金属离子生成氧氧化物沉淀pH见下表。
| 开始沉淀pH | 沉淀完全pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
您最近半年使用:0次
解题方法
3 . 亚硫酸钠和碘酸钾在酸性溶液里反应的化学方程式是:Na2SO3+KIO3+H2SO4=Na2SO4+K2SO4+I2+H2O,该反应过程和机理较复杂,一般认为分为以下几步:
① +
+ →
→ +
+ (慢)
(慢)
② +
+ →IO-+
→IO-+ (快)
(快)
③5I-+6H++ →3I2+3H2O(快)
→3I2+3H2O(快)
④I2+ +H2O→2I-+
+H2O→2I-+ +2H2(快)
+2H2(快)
(1)根据上述条件推测,此反应的总的反应速率由___ 步反应决定。
(2)若预先加入淀粉溶液,由题述看必在___ 离子消耗完时,才会使淀粉变蓝的现象产生。
①
 +
+ →
→ +
+ (慢)
(慢)②
 +
+ →IO-+
→IO-+ (快)
(快)③5I-+6H++
 →3I2+3H2O(快)
→3I2+3H2O(快)④I2+
 +H2O→2I-+
+H2O→2I-+ +2H2(快)
+2H2(快)(1)根据上述条件推测,此反应的总的反应速率由
(2)若预先加入淀粉溶液,由题述看必在
您最近半年使用:0次
名校
解题方法
4 . 在下列过程中,需要加快化学反应速率的是
| A.钢铁腐蚀 | B.工业炼钢 | C.食物腐烂 | D.橡胶老化 |
您最近半年使用:0次
2019-01-24更新
|
568次组卷
|
2卷引用:【全国百强校】贵州省铜仁市第一中学2018-2019学年高二上学期期末考试化学试题



