| A.金属的腐蚀 | B.食物的腐败 | C.塑料的老化 | D.氨的合成 |
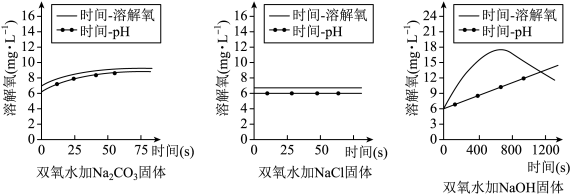
| A.Na2CO3对H2O2的分解有促进作用 | B.加入NaCl后溶液溶解氧变化不明显 |
| C.H2O2分解随pH增大而持续加快 | D.鱼浮灵使用时应根据pH控制投放量 |
 的氯化、溴化反应势能图及一段时间后产物的选择性如图,下列叙述不正确的是
的氯化、溴化反应势能图及一段时间后产物的选择性如图,下列叙述不正确的是 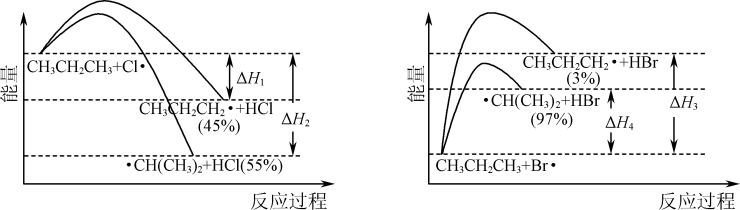
A. |
| B.升高温度,体系中n(1-氯丙烷)∶n(2-氯丙烷)的值增大 |
| C.以丙烷为原料合成丙醇时,“先溴代再水解”有利于提高2-丙醇的含量 |
| D.由图可知,丙烷中碳氢键的键能不完全相同 |
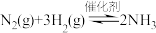 在恒容密闭容器中,初始投入量相等的条件下,得到三组实验数据如表所示:
在恒容密闭容器中,初始投入量相等的条件下,得到三组实验数据如表所示:| 实验序号 | 温度( ) ) |  浓度( 浓度( ) ) | ||||||
 |  |  |  | 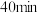 | 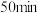 | 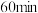 | ||
| 1 | 300 | 2.00 | 1.70 | 1.50 | 1.36 | 1.25 | 1.20 | 1.20 |
| 2 | 300 | 2.00 | 1.50 | 1.28 | 1.20 | 1.20 | 1.20 | 1.20 |
| 3 | 200 | 2.00 | 1.60 | 1.39 | 1.29 | 1.27 | 1.27 | 1.27 |
| A.当容器内的压强不再改变时,说明该可逆反应已达到化学平衡状态 |
B.实验2中,前 内以 内以 的浓度变化表示的化学反应速率为 的浓度变化表示的化学反应速率为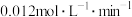 |
| C.比较实验1和2,说明实验2使用了更高效的催化剂 |
D.实验3中,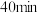 时向容器中充入一定量 时向容器中充入一定量 ,则正反应速率 ,则正反应速率 不变 不变 |
(1)下列说法不正确的是
A.实验室制备氨气时,可以用CaCl2固体干燥氨气
B.在浓氨水中加入生石灰可制备少量氨气
C.合成氨塔中,需要有热交换装置,便于能量的有效利用
D.合成氨工业中,可将氨气液化,并不断将液氨移去,利于提高NH3的产率
(2)氨是制取硝酸的重要原料。氨的催化氧化过程主要有以下两个反应:
I.4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) ΔHI
4NO(g)+6H2O(g) ΔHIII.4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) ΔHII
2N2(g)+6H2O(g) ΔHII不同温度下氨氧化的平衡常数如下(p=0.1013Mpa):
| 温度(℃) | 300 | 500 | 700 | 900 | 1100 |
| 反应I(KI) | 6.3×1041 | 1.1×1026 | 2.1×1019 | 3.8×1015 | 3.4×1011 |
| 反应II(KII) | 7.3×1056 | 7.1×1034 | 2.6×1025 | 1.5×1020 | 6.7×1016 |
A.ΔHI>0,ΔHII>0
B.如果对反应不加控制,氨和氧气反应的最终产物主要是N2
C.为使反应有利于朝生成更多的NO方向进行,不必关注热力学问题(平衡移动问题),需要关注动力学问题(反应速率问题)
D.在实际生产中,需采用高压氧化,以利于提高NO的产率
E.反应中需控制氨氧比、选择性催化剂的形状、气固相接触时间等
②在实际工业生产中,温度一般需要在750℃~850℃左右,其主要原因是
(3)已知可通过下列方法合成尿素:
第一步:2NH3(1)+CO2(g)
 H2NCOONH4(1) ΔH=-159.5kJ/mol
H2NCOONH4(1) ΔH=-159.5kJ/mol第二步:H2NCOONH4(1)
 CO(NH2)2(1)+H2O(1) ΔH=+28.5kJ/mol
CO(NH2)2(1)+H2O(1) ΔH=+28.5kJ/mol在体积为5L的密闭容器中加入1molCO2和4molNH3,在一定条件下反应进行到10min时,测得CO2和尿素的物质的量均为0.25mol,如图所示。
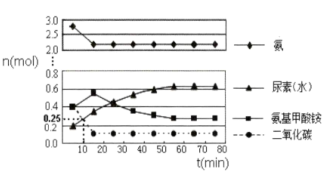
①若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则10min内第一步反应中生成H2NCOONH4(1)[氨基甲酸铵]的平均反应速率为
②反应进行15分钟后,随着时间的变化,尿素和氨基甲酸铵的物质的量变化比较明显,但氨气和二氧化碳的变化很小,其主要原因是
| A.在植物油中滴几滴酸性高锰酸钾溶液,振荡,溶液褪色,说明植物油含有酯基 |
| B.盐酸与硅酸钠溶液反应生成白色沉,证明氯的非金属性大于硅 |
| C.溶液的酸碱性对H2O2的稳定性有较大影响,如在酸性溶液中,H2O2分解较快 |
| D.任何反应都有一定限度,通过改变反应条件可对反应进行调控 |
 对烟道气进行脱硝(除氮氧化物)的SCR技术具有效率高、性能可靠的优势。SCR技术的原理为
对烟道气进行脱硝(除氮氧化物)的SCR技术具有效率高、性能可靠的优势。SCR技术的原理为 和NO在催化剂(
和NO在催化剂( )表面转化为
)表面转化为 和
和 ,反应进程中的相对能量变化如图所示。下列说法错误的是
,反应进程中的相对能量变化如图所示。下列说法错误的是
A.总反应方程式为 |
B.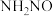 是脱硝反应的活性中间体 是脱硝反应的活性中间体 |
| C.升高温度,脱硝反应的正反应速率的增大程度大于其逆反应速率的增大程度 |
| D.决定反应速率的步骤是“H的移除” |
| A.钢铁腐蚀 | B.工业炼钢 | C.食物腐烂 | D.塑料老化 |
9 . 对H2O2的分解速率影响因素进行研究。
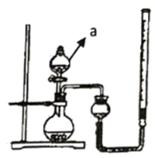
(1) A组为研究催化剂FeCl3的量对O2生成速率的影响,设计了如下三组实验方案(见下表),将表中所给的试剂按一定体积混合后进行反应。
| A | B | C |
10%H2O2/mL | 20.0 | V1 | V2 |
2 mol/LFeCl3/mL | 0 | 5.0 | 10.0 |
H2O/mL | V3 | V4 | 0 |
按要求回答下列问题:
①a装置的名称为
②若读数时发现,量气装置左端液面低于右端液面,则测得的气体体积
(2) B组在相同的温度下,利用下图甲装置对H2O2在不同条件下的分解速率进行了探究,得到乙曲线:
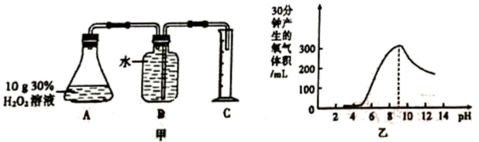
则B小组探究的是
(3)C小组利用如下装置探究100℃,H2O2在不同离子催化作用下反应24h的分解率,

实验编号 | 离子 | 加入量/(mg/L) | 分解率/% |
① | 无 | — | 2 |
② | Al3+ | 1.0 | 2 |
③ | Fe3+ | 1.0 | 15 |
④ | Cu2+ | 0.1 | 86 |
⑤ | Cr3+ | 0.1 | 96 |
则该小组实验时记录的数据应该是
| A.钢铁腐蚀 | B.食物腐败 | C.塑料老化 | D.工业合成氮 |




