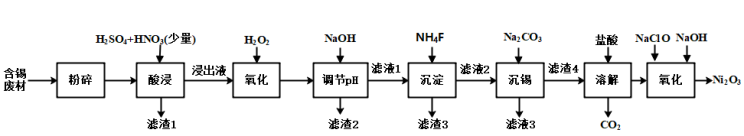
1 . 三氧化二镍(Ni2O3)是一种灰黑色、无气味、有光泽的块状物,易碎成细粉末,常用于制造高能电池。工业上以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料生产NiCl2,继而生产Ni2O3,其工艺流程如下:
已知:①下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol/L计算)。
②25℃时,Ksp(NiCO3)= 1×10-6
回答下列问题:
(1)“酸浸”过程中,l mol NiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式:_______ 。
(2)“酸浸”后的酸性溶液中加入H2O2的目的是_______ 。
(3)“沉镍”前需加NaOH控制溶液pH的范围为_______ ;“滤渣1”的主要成分有_______ 。
(4)“氧化”时生成Ni2O3的离子方程式为_______ 。
(5)保持其他条件不变,在不同温度下对含镍废料进行“酸浸”,镍的浸出率随时间变化如图。“酸浸”的最佳温度与时间分别为_______ ℃、_______ min。

(6)“沉镍”过程中,若滤液中c(Ni2+)= 2.0 mol/L,欲使100 mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤1×10-5mol/L],则需要加入Na2CO3固体的质量最少为_______ 。(不考虑 水解,计算结果保留两位小数)
水解,计算结果保留两位小数)

已知:①下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol/L计算)。
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 3.0 | 6.7 |
| 沉淀完全的pH | 3.2 | 9.0 | 4.7 | 9.2 |
回答下列问题:
(1)“酸浸”过程中,l mol NiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式:
(2)“酸浸”后的酸性溶液中加入H2O2的目的是
(3)“沉镍”前需加NaOH控制溶液pH的范围为
(4)“氧化”时生成Ni2O3的离子方程式为
(5)保持其他条件不变,在不同温度下对含镍废料进行“酸浸”,镍的浸出率随时间变化如图。“酸浸”的最佳温度与时间分别为

(6)“沉镍”过程中,若滤液中c(Ni2+)= 2.0 mol/L,欲使100 mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤1×10-5mol/L],则需要加入Na2CO3固体的质量最少为
 水解,计算结果保留两位小数)
水解,计算结果保留两位小数)
您最近半年使用:0次
2022-01-22更新
|
158次组卷
|
2卷引用: 山西省太原市2021-2022学年高三上学期期末考试化学试题
名校
解题方法
2 . 向四个体积相同的密闭容器(甲、乙、丙、丁)中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小排列顺序正确的是
甲:在500℃时,10mol SO2和6mol O2反应
乙:在500℃时,用V2O5作催化剂,10mol SO2和5mol O2反应
丙:在450℃时,8mol SO2和5mol O2反应
丁:在500℃时,8mol SO2和5mol O2反应。
甲:在500℃时,10mol SO2和6mol O2反应
乙:在500℃时,用V2O5作催化剂,10mol SO2和5mol O2反应
丙:在450℃时,8mol SO2和5mol O2反应
丁:在500℃时,8mol SO2和5mol O2反应。
| A.甲、乙、丙、丁 | B.乙、甲、丙、丁 |
| C.乙、甲、丁、丙 | D.丁、丙、乙、甲 |
您最近半年使用:0次
2021-03-04更新
|
188次组卷
|
2卷引用:山西省汾阳市汾阳中学2020-2021学年高二下学期开学考试化学试题
3 . 某兴趣小组为探究外界条件对化学反应速率的影响,设计的实验方案如下:
(1)实验时发生反应的化学方程式为___ ;为了顺利观察到KMnO4紫色褪去,起始时需要满足n(H2C2O4):n(KMnO4)≥___ 。
(2)探究反应物浓度对反应速率影响的是实验___ (填编号,下同),探究反应温度对反应速率影响的是实验___ 。
(3)测得实验①中溶液褪色的时间为30s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=___ 。
(4)实验过程中发现:在开始反应的一段时间内,反应速率较小,溶液褪色不明显;但不久反应速率明显增大,溶液很快褪色。导致上述现象的原因可能是___ 。
(5)草酸又称乙二酸,是一种二元弱酸。写出草酸在水中的第一步电离方程式:___ ,该步电离的平衡常数表达式K1=___ 。
| 实验编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/(mol•L-1) | 体积/mL | 浓度/(mol•L-1) | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.01 | 3.0 | 25 |
| ② | 0.20 | 2.0 | 0.01 | 3.0 | 25 |
| ③ | 0.20 | 2.0 | 0.01 | 3.0 | 50 |
(1)实验时发生反应的化学方程式为
(2)探究反应物浓度对反应速率影响的是实验
(3)测得实验①中溶液褪色的时间为30s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=
(4)实验过程中发现:在开始反应的一段时间内,反应速率较小,溶液褪色不明显;但不久反应速率明显增大,溶液很快褪色。导致上述现象的原因可能是
(5)草酸又称乙二酸,是一种二元弱酸。写出草酸在水中的第一步电离方程式:
您最近半年使用:0次
4 . 为了提升食品的品质,在食品加工中可合理使用添加剂。下列添加剂与反应速率有关的是
| A.着色剂 | B.调味剂 | C.防腐剂 | D.增白剂 |
您最近半年使用:0次
2020-05-01更新
|
260次组卷
|
5卷引用:山西省太原市第五中学2020-2021学年高二上学期10月月考试题
名校
解题方法
5 . 下列过程中,需要增大化学反应速率的是
| A.钢铁腐蚀 | B.食物腐败 | C.塑料老化 | D.工业合成氮 |
您最近半年使用:0次
2020-04-22更新
|
332次组卷
|
19卷引用:山西省怀仁县第八中学2016-2017学年高一(普通班)下学期期末考试化学试题
山西省怀仁县第八中学2016-2017学年高一(普通班)下学期期末考试化学试题山西省新绛县第二中学2019-2020学年高二上学期第一次考试化学试题(已下线)2010-2011学年江西省鄱阳县油墩街中学高一下学期期中考试化学试卷(已下线)2013-2014浙江省宁波市高一下学期期末考试化学试卷2014-2015学年广东省惠州市高一下学期期末考试化学文科试卷2015-2016学年青海省西宁四中高二上学期期末化学试卷2015-2016学年四川省广安二中高一下学期期中化学试卷2016-2017学年河北省武邑中学高二上入学考试化学试卷2016-2017学年河北省武邑中学高二上8.28周考化学卷2016-2017学年河北省武邑中学高二上9.21周考化学卷2016-2017学年天津市河东区高二上学期期中质检化学试卷湖北省天门市三校2016-2017学年高一下学期期中考试化学试题福建省三明市第一中学2017-2018学年高二上学期期中考试(理)化学试题【全国百强校】福建省三明市第一中学2018-2019学年高二(理)上学期期中考试化学试题江西省上饶市鄱阳县第二中学2019-2020学年高二上学期期中考试化学试题河南省周口市陈州高级中学2019-2020学年高一下学期摸底考试化学试题江苏省盐城市伍佑中学2020-2021学年高一下学期第一次阶段考试化学试题江苏省镇江实验高级中学2020-2021学年高一下学期第一次月考化学试题北京景山学校2021-2022学年高一下学期期中考试化学试题
6 . 下列生产生活中所采取的措施不能用化学反应速率解释的是
| A.有些食物的标签上注明须冷藏 | B.在糕点制作过程中添加防腐剂 |
| C.在轮胎制品中加入适量的炭黑 | D.燃煤发电时常用煤粉代替煤块 |
您最近半年使用:0次



